Clear Sky Science · pl
Oś EHMT2–MBLAC2 tłumi transkrypcję DNA rybosomalnego w odpowiedzi na uszkodzenia DNA w jąderku
Dlaczego fabryki białek w komórce potrzebują ochrony
W każdej z naszych komórek znajduje się tętniący życiem warsztat zwany jąderkiem, gdzie budowane są molekularne maszyny produkujące białka — rybosomy. Ponieważ ta „fabryka” pracuje niemal bez przerwy, jej matrycowe DNA jest pod stałym obciążeniem i może ulegać przerwaniu. Badanie opisane w tym artykule analizuje, jak komórki tymczasowo wyciszają tę fabrykę, aby naprawić uszkodzenia, oraz jak awaria tego systemu bezpieczeństwa może przyczyniać się do rozwoju raka okrężnicy.
Wrażliwy odcinek DNA
Rybosomy są składane na podstawie instrukcji zapisanych w specjalnych fragmentach DNA zwanych DNA rybosomalnym (rDNA). Sekwencje te występują wielokrotnie i są przepisywane z bardzo dużą szybkością, co czyni je szczególnie podatnymi na niebezpieczne złamania dwuniciowe. Gdy w rDNA dochodzi do takich przerwań, komórki robią więcej niż tylko „załatają” DNA: reorganizują też jąderko i czasowo zatrzymują przepisywanie rDNA na RNA. To zawieszenie zapobiega kolizjom maszynerii naprawczej z aparatem transkrypcyjnym i pomaga utrzymać liczbę oraz strukturę powtórzeń rDNA — ważną zaporę, ponieważ niestabilność rDNA wiązana jest ze starzeniem i wieloma chorobami, w tym z rakiem.
Nowy przełącznik bezpieczeństwa w jąderku
Naukowcy identyfikują białko o nazwie EHMT2, lepiej znane z modyfikowania chromatyny w innych częściach genomu, jako kluczowego gracza w tej jąderkowej reakcji bezpieczeństwa. Korzystając z systemu w komórkach ludzkich, który tnie rDNA w określonych miejscach, pokazują, że EHMT2 spieszy na krawędź jąderka, gdzie uszkodzone rDNA gromadzi się w struktury zwane czapkami. Tam EHMT2 jest niezbędne do zatrzymania produkcji rRNA po uszkodzeniu. Gdy EHMT2 jest nieobecne lub jego aktywność jest chemicznie zablokowana, komórki nadal transkrybują rDNA pomimo złamań. Zespół wyjaśnia ten efekt zdolnością EHMT2 do dodawania specyficznej chemicznej etykiety na białkach histonowych przy uszkodzonym rDNA, co sprzyja bardziej zredukowanemu, uciszonemu stanie chromatyny.
Powiązanie pauzy transkrypcyjnej z naprawą DNA
Uciszenie rDNA to tylko połowa historii; musi mu towarzyszyć skuteczna naprawa. Autorzy wykazują, że komórki pozbawione EHMT2 mają problem z naprawą złamań rDNA: fragmenty DNA utrzymują się dłużej, częściej pojawiają się małe dodatkowe jądra (znak niestabilności genomowej), a liczba kopii rDNA z czasem maleje. Co ważne, jeden z głównych szlaków naprawczych — łączenie końców bez homologii (NHEJ), które szybko skleja końce DNA — nie jest właściwie rekrutowany do jąderkowych czapek bez EHMT2, mimo że inne drogi naprawy pozostają w dużej mierze nienaruszone. W rezultacie komórki pozbawione EHMT2 stają się nadwrażliwe na uszkodzenia jąderka i tracą zdolność do tworzenia zdrowych kolonii po przecięciu rDNA.
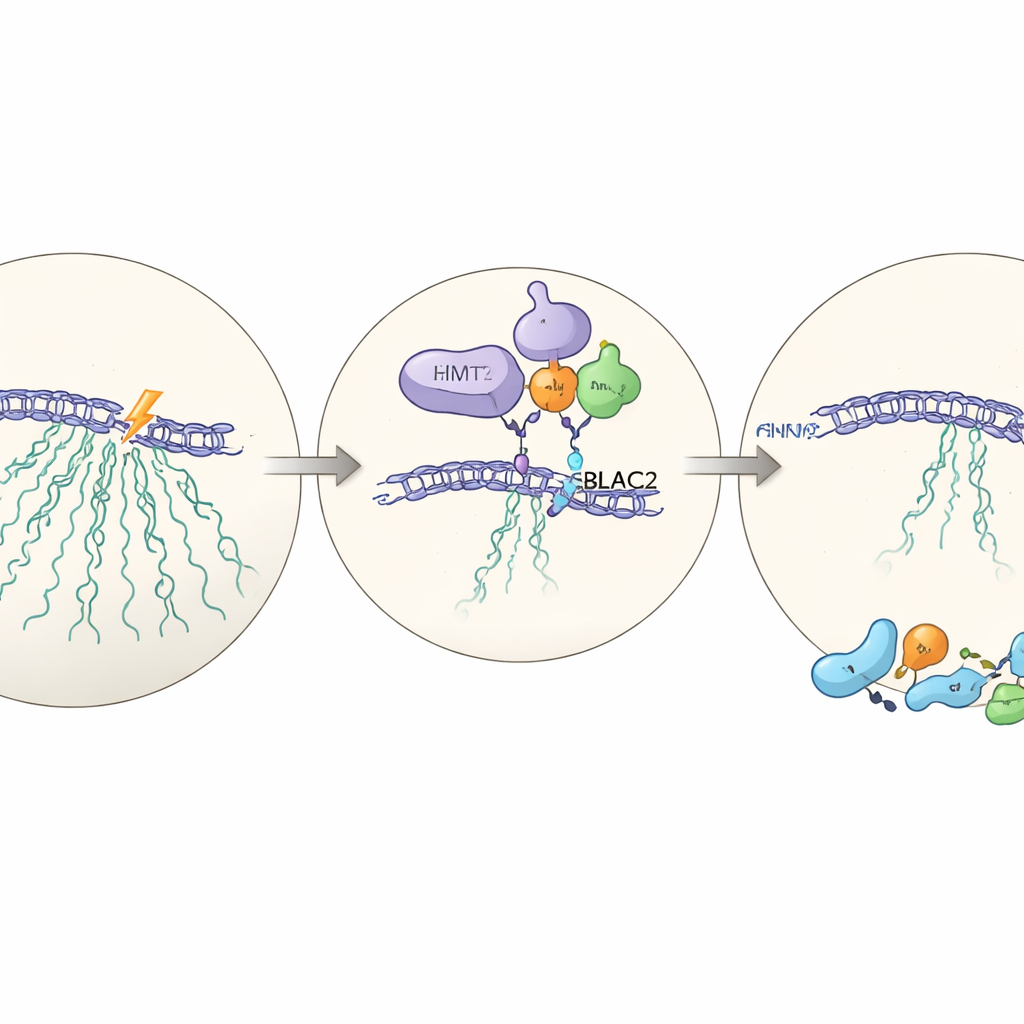
Ukryty partner: MBLAC2
Aby zrozumieć, jak EHMT2 wywiera swój wpływ, zespół przeprowadza szerokie pomiary białek w komórkach z EHMT2 i bez niego. Wśród białek, których poziom spada przy braku EHMT2, wyróżnia się jedno: MBLAC2, słabo poznana enzymatyczna cząsteczka zwykle wzbogacona w jąderku. Gdy MBLAC2 jest zredukowane przy użyciu celowanych narzędzi RNA, komórki ponownie zawodzą w wyciszaniu rDNA po uszkodzeniu i mają mniejszą przeżywalność. EHMT2 fizycznie wiąże się z MBLAC2 i stabilizuje je na poziomie białka; bez EHMT2 MBLAC2 degraduje się szybciej. Usunięcie obu białek nie pogarsza efektu bardziej niż usunięcie jednego, co sugeruje, że działają w tym samym szlaku — nowo opisanej osi EHMT2–MBLAC2, która koordynuje pauzę transkrypcyjną z efektywną naprawą.
Od uszkodzonego DNA do raka okrężnicy
Ponieważ niestabilność rDNA jest cechą wielu nowotworów, autorzy pytają, czy ta oś odgrywa rolę w raku okrężnicy, chorobie silnie zależnej od zwiększonej produkcji rybosomów. W modelach mysich i próbkach ludzkich guzów zarówno EHMT2, jak i MBLAC2 są konsekwentnie bardziej obfite w nowotworach okrężnicy niż w normalnej tkance jelita, równolegle z markerami nasilonej produkcji rybosomów. Tłumienie EHMT2 w komórkach raka okrężnicy spowalnia wzrost guzów u myszy, zmniejsza markery związane z rybosomami i obniża poziomy MBLAC2. Dane pacjentów z The Cancer Genome Atlas ujawniają, że wyższa ekspresja obu genów wiąże się z bardziej zaawansowaną chorobą i gorszym przeżyciem po radioterapii. Razem obserwacje te sugerują, że komórki nowotworowe mogą przejąć oś EHMT2–MBLAC2, by lepiej tolerować uszkodzenia rDNA i utrzymać produkcję rybosomów potrzebną do niekontrolowanego wzrostu.
Co to oznacza dla zdrowia i terapii
Dla czytelnika nietechnicznego kluczowy wniosek jest taki, że nasze komórki wyewoluowały dedykowany hamulec awaryjny wewnątrz jąderka: gdy matryca DNA dla rybosomów ulega złamaniu, EHMT2 i jego partner MBLAC2 pomagają zatrzymać fabrykę, ukierunkować naprawę i przywrócić stabilność. Gdy ten hamulec jest nadmiernie aktywny lub wykorzystywany w raku okrężnicy, wydaje się pomagać komórkom nowotworowym przetrwać stres i leczenie. Celowanie w EHMT2, MBLAC2 lub ich interakcję może w przyszłości selektywnie osłabić zdolność komórek nowotworowych do radzenia sobie z uszkodzeniami DNA rybosomalnego, zwiększając skuteczność standardowych terapii, takich jak chemioterapia i radioterapia, przy jednoczesnym oszczędzaniu tkanek zdrowych.
Cytowanie: Wang, C., Lu, Q., Cao, L. et al. The EHMT2-MBLAC2 axis suppresses ribosomal DNA transcription in response to nucleolar DNA damage. Cell Death Dis 17, 320 (2026). https://doi.org/10.1038/s41419-026-08616-1
Słowa kluczowe: uszkodzenie DNA rybosomalnego, stres jąderkowy, szlak EHMT2 MBLAC2, rak okrężnicy, naprawa DNA i transkrypcja