Clear Sky Science · ja
EHMT2–MBLAC2 軸は核小体のDNA損傷に応答してリボソームDNA転写を抑制する
細胞のタンパク質工場が守られる理由
私たちの細胞の一つ一つには核小体と呼ばれるにぎやかな工房があり、そこでタンパク質を作る分子機械であるリボソームが組み立てられます。この工場はほぼ休みなく稼働するため、その鋳型となるDNAは常に負荷にさらされ、切断が起きやすくなります。本稿で扱う研究は、細胞が損傷を修復するために一時的にこの工場を静める仕組みと、その安全装置の故障が大腸癌の促進にどう関わるかを探っています。
脆弱なDNA領域
リボソームはリボソームDNA(rDNA)と呼ばれる特別なDNA領域にコードされた指示に基づいて組み立てられます。これらの配列は多数回繰り返され、高速で転写されるため、二本鎖切断のような危険な損傷が起こりやすくなります。rDNAにそのような切断が生じると、細胞は単にDNAをつなぎ合わせるだけでなく、核小体を再編成してrDNAの転写を一時停止します。この一時停止は、修復装置と転写機構の衝突を防ぎ、rDNA繰り返し配列の数や構造を安定に保つのに役立ちます。rDNAの不安定性は老化やがんを含む多くの疾患と関連しているため、重要な防御策です。
核小体の新しい安全スイッチ
研究者らは、ゲノムの他領域でクロマチン修飾に関与することで知られるEHMT2というタンパク質を、この核小体の安全応答における重要な因子として同定しました。人由来細胞でrDNAを特定部位で切断する系を用いると、EHMT2は損傷したrDNAがキャップと呼ばれる構造に集まる核小体の縁に急行することが示されます。そこでEHMT2は損傷後のリボソームRNA産生の停止に必須です。EHMT2が欠損するかその活性が化学的に阻害されると、切断があっても細胞はrDNAの転写を続けてしまいます。研究チームはこの現象を、EHMT2が損傷したrDNA上のヒストンに特定の化学修飾を付与し、より抑制的なクロマチン状態を作る能力に起因すると辿っています。
転写の一時停止とDNA修復の連携
rDNAの静音化は物語の半分に過ぎません。続いて成功する修復が必要です。著者らはEHMT2を欠く細胞はrDNA切断を修復するのが苦手であることを見出しました。DNA断片が長く残り、小さな余剰核(ゲノム不安定性の兆候)がより頻繁に現れ、rDNAコピー数が時間とともに減少します。重要なのは、迅速にDNA末端を再連結する主要な修復経路の一つである非相同末端結合(NHEJ)が、EHMT2なしではrDNAキャップに適切に動員されないことです。他の修復経路は概ね保たれているにもかかわらず、この結果としてEHMT2欠損細胞は核小体損傷に過敏になり、rDNA切断後に健全なコロニーを形成する能力を失います。
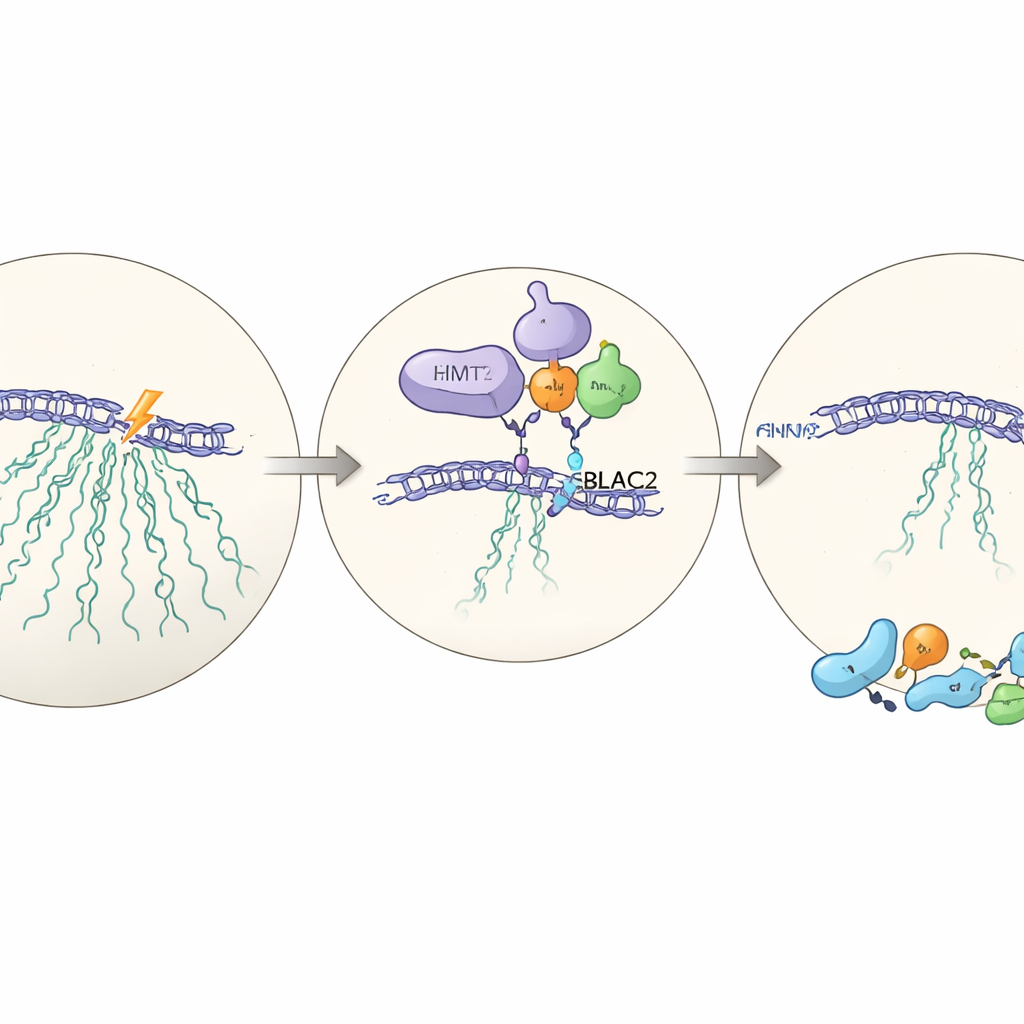
隠れた相棒:MBLAC2
EHMT2がどのように影響を及ぼすかを理解するため、チームはEHMT2の有無で大規模なタンパク質解析を行いました。EHMT2が欠けたときに減少するタンパク質の中で一際目立つのがMBLAC2です。MBLAC2は核小体に多く存在する比較的研究の少ない酵素です。MBLAC2を標的RNA手法で減らすと、細胞は損傷後に再びrDNAを沈黙させることができず、生存力も低下します。EHMT2はMBLAC2に物理的に結合してタンパク質レベルで安定化させます。EHMT2がないとMBLAC2はより速やかに分解されます。両方のタンパク質を同時に失っても、いずれか一方を失った場合より悪化しないことから、両者は同じ経路で作用していることが示唆されます。これが転写の一時停止と有効な修復を連携させる新たに記述されたEHMT2–MBLAC2軸です。
損傷したDNAから大腸癌へ
rDNA不安定性は多くの腫瘍の特徴であるため、著者らはこの軸がリボソーム生産の増強に強く依存する大腸癌で役割を果たすかを検討しました。マウスモデルとヒト腫瘍試料の両方で、EHMT2とMBLAC2は正常な結腸組織に比べて大腸腫瘍で一貫して多く存在し、リボソーム形成の指標も増加していました。大腸癌細胞でEHMT2を抑制するとマウスの腫瘍増殖が遅くなり、リボソーム関連マーカーが減少し、MBLAC2レベルも低下しました。The Cancer Genome Atlasの患者データでは、両遺伝子の発現が高いほど病期が進行し、放射線治療後の生存が悪いことと関連していました。これらの観察は、がん細胞がEHMT2–MBLAC2経路を利用してrDNA損傷に耐え、増殖に必要なリボソーム産生を維持している可能性を示唆します。
健康と治療への意味
非専門家向けに要点を言えば、細胞は核小体内に専用の非常ブレーキを進化させており、リボソームの設計図であるDNAが切断されるとEHMT2とその相棒MBLAC2が工場を一時停止させ、修復を導き、安定性を回復する助けをします。このブレーキが大腸癌で過剰に働くか悪用されると、腫瘍細胞はストレスや治療に耐えやすくなるようです。EHMT2やMBLAC2、または両者の相互作用を標的にすることで、将来の治療はがん細胞のrDNA損傷への対処能力を選択的に弱め、化学療法や放射線療法など既存治療の効果を高めつつ正常組織を温存する可能性があります。
引用: Wang, C., Lu, Q., Cao, L. et al. The EHMT2-MBLAC2 axis suppresses ribosomal DNA transcription in response to nucleolar DNA damage. Cell Death Dis 17, 320 (2026). https://doi.org/10.1038/s41419-026-08616-1
キーワード: リボソームDNA損傷, 核小体ストレス, EHMT2 MBLAC2 経路, 大腸癌, DNA修復と転写