Clear Sky Science · tr
ATC12 küçük molekülü Aurora-A/TPX2 etkileşimini engeller ve meme kanseri hücrelerinin proliferasyonunu bozar
Gelecekteki kanser tedavileri için bu araştırma neden önemli
Birçok kanser ilacı hücre bölünmesini tetikleyen enzimleri kapatmaya çalışır, ancak genellikle çok sayıda hedefe dokunup yan etkilere neden olur veya hastalarda yeterince etkili olamaz. Bu çalışma farklı bir taktiği inceliyor: bir enzimi kapatmak yerine, meme kanseri hücrelerinin büyümesine ve hayatta kalmasına yardımcı olan iki proteinin arasındaki özgül ortaklığı bozmayı amaçlıyor. Araştırmacılar, bu ortaklığa müdahale eden ve tümörlerden doğrudan alınan hücreler de dahil olmak üzere kanser hücrelerinin büyümesini yavaşlatan ATC12 adlı yeni bir küçük molekül keşfedip test ediyorlar.
Bölünen hücrelerde kritik bir ortaklık
Hücrelerimizde Aurora-A adlı bir enzim hücre bölünmesini düzenlemeye yardımcı olur. TPX2 adlı başka bir protein Aurora-A’ya bağlanır, onun hücrenin iç iskeletinde doğru konumlanmasına yardımcı olur ve stabilitesini artırır. Birlikte, tümörlerde—meme kanserleri de dahil olmak üzere—sıkça anormal derecede yüksek seviyelerde bulunan işlevsel bir çift oluştururlar. Hücre bölünmesi dışındaki rollerinde Aurora-A, bölünmeyen kanser hücrelerinin çekirdeğinde birikebilir ve tümör büyümesini ve yayılmasını destekleyen genleri artırabilir. Kanıtlar TPX2’nin de Aurora-A’nın çekirdeğe ulaşmasına yardımcı olduğunu gösteriyor. ATP ile yarışarak Aurora-A’nın aktivitesini engelleyen geleneksel ilaçlar klinik deneylerde sınırlı başarı göstermiştir; bunun bir nedeni ATP bağlanma bölgesinin birçok enzime benzemesi ve hedef dışı etkilere yol açmasıdır. Bu durum, araştırmacıları Aurora-A’nın kanserle ilişkili rollerini daha seçici şekilde baskılayacak yöntemler aramaya yönlendirdi.

Bir protein bağını koparmak için molekül tasarlamak
Ekip, bilgisayar tabanlı tarama kullanarak TPX2’nin Aurora-A’ya bağlandığı temas bölgesine sığabilecek milyonlarca satın alınabilir molekül arasında adaylar aradı. Hidrofobik cepler ve anahtar bağlanma “sıcak noktaları” gibi bu etkileşim için kritik olduğu bilinen kimyasal özelliklere odaklandılar. Başlangıçtaki büyük havuzdan 184 bileşiğe, ardından arayüzün üç boyutlu şekli ve kimyasına en iyi uyan 15 üst adayına indirgediler. Native kütle spektrometrisi kullanan laboratuvar testleri, bu moleküllerden dördünün TPX2 fragmanının Aurora-A’ya bağlanmasını zayıflatabildiğini gösterdi. Doz–yanıt deneyleri, iki bileşiği, özellikle ATC12’yi TPX2’yi Aurora-A’dan yerinden etmekte en güçlü olanlar olarak tanımladı; bu moleküller Aurora-A’nın enzim aktivitesini engellemeden etki gösterdi, yani katalitik bölge yerine ortaklığa özgü bir etkiyi işaret ediyordu.
ATC12’nin kanser hücreleri ve davranışları üzerindeki etkisi
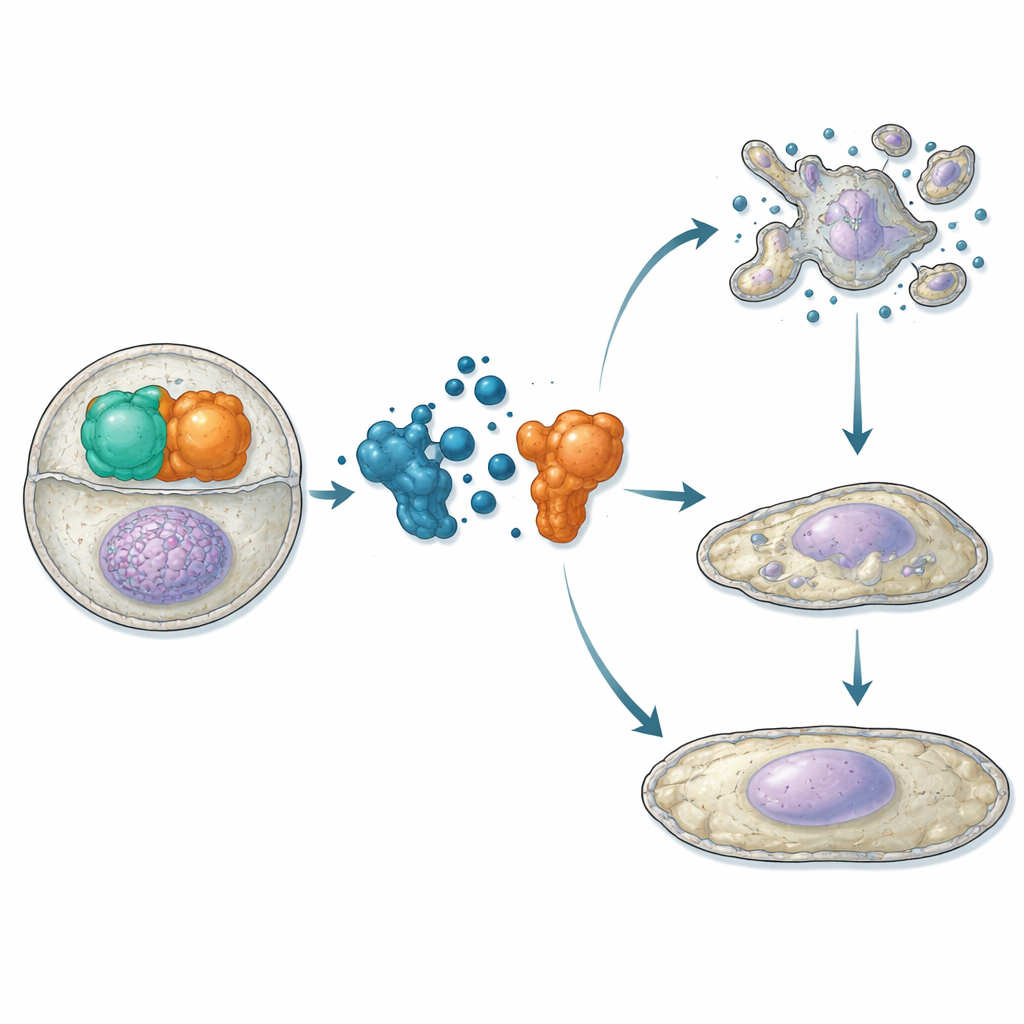
ATC12’nin Aurora-A’ya bağlandığını ve vitro ortamda TPX2 ile rekabet ettiğini gösterdikten sonra araştırmacılar canlı hücrelere geçti. Osteosarkom ve meme kanseri hücre hatlarında, yakınlık testleri ve mikroskopi kullanılarak ATC12 tedavisinin mitotik iğde ve interfaz çekirdekleri dahil Aurora-A/TPX2 etkileşimini azalttığı, bu bölgelerde Aurora-A sinyalinde azalma ile birlikte olduğu gösterildi. İki meme kanseri modelinde—MCF7 (daha az agresif, hormon reseptör pozitif) ve MDA-MB-231 (yüksek agresiflik, üçlü-negatif)—ATC12, doza bağlı olarak hücre canlılığını düşürdü; oysa etkileşimi bozmayıp kontrol görevi gören bir bileşik etkisizdi. Zaman atlamalı görüntüleme, MCF7 hücrelerinde ATC12’nin mitoz bölünmeye giren hücre oranını büyük ölçüde azalttığını, bölünenlerde mitoz süresini uzattığını ve yoğun şekilde hücre ölümü ile birlikte apoptozun biyokimyasal işaretlerini ortaya çıkardığını gösterdi. Buna karşılık, MDA-MB-231 hücreleri belirgin hücre ölümü olmadan proliferasyonun yavaşlamasını gösterdi; bunun yerine hücre döngüsü freni p21 seviyelerinde artış, çekirdek büyümesi ve senesans belirteçlerinin aktivasyonu gözlendi; bu da kalıcı bölünmeme durumuna geçişi işaret etti.
ATC12’nin 3B modellerde ve hasta kaynaklı organoidlerde test edilmesi
Tümörlerin vücuttaki davranışını daha iyi taklit etmek için bilim insanları ATC12’yi üç boyutlu kültürlerde inceledi. Meme kanseri hücreleri mamomosferler—kök-benzeri, tedaviye dirençli hücreleri zenginleştiren küresel kümeler—olarak yetiştirildiğinde, ATC12 hem MCF7 hem de MDA-MB-231 arka planlarında canlılıklarını ve boyutlarını azalttı; oysa standart bir Aurora-A kinaz inhibitörü küreleri küçültmedi. Ekip daha sonra kemoterapiye dirençli tümörlerden alınmış üçlü-negatif meme kanseri biyopsilerinden yetiştirilen organoidlere geçti. Bu hasta kaynaklı organoidlerde ATC12, düşük mikromolar aralığında etkili konsantrasyonlarla açık bir doza bağımlı şekilde hücre canlılığını azalttı. Tedavi sırasında ilacı yeniden dozlama etkiyi daha da artırdı; bu da Aurora-A/TPX2 kompleksinin sürdürülen şekilde bozulması için ATC12 seviyelerinin zaman içinde korunmasının önemli olabileceğini düşündürüyor.
Bu çalışmanın kanser terapisi için anlamı
Bu çalışma, belirli protein ortaklıklarını bozmanın kanser hücrelerini etkisiz hale getirmek için geleneksel enzim inhibitörlerinin bazı sakıncalarından kaçınarak güçlü bir yol olabileceği fikrini destekliyor. Aurora-A/TPX2 kompleksini hedefleyerek ATC12 hem bölünen hem de bölünmeyen kanser hücrelerine müdahale ediyor; tümörün genetik yapısına bağlı olarak ya hücre ölümünü ya da kalıcı senesansı tetikliyor. 3B mamomosferlerde ve tedavisi zor üçlü-negatif meme kanserlerinden elde edilen organoidlerde büyümeyi bozma yeteneği, aynı iskelet üzerine inşa edilecek rafine moleküller veya degrader’lar dahil yeni ilaçlar için ümit vaat eden bir başlangıç noktası olduğunu vurguluyor. Güç ve stabiliteyi artırmak için daha fazla optimizasyona ihtiyaç olsa da çalışma, Aurora-A/TPX2 çiftinin seçici olarak bozulmasının gelecekteki anti-kanser tedavileri için gerçekçi ve potansiyel olarak değerli bir strateji olduğunu gösteriyor.
Atıf: Boi, D., Fianco, G., Polverino, F. et al. The ATC12 small molecule inhibits the Aurora-A/TPX2 interaction and impairs the proliferation of breast cancer cells. Cell Death Dis 17, 356 (2026). https://doi.org/10.1038/s41419-026-08579-3
Anahtar kelimeler: Aurora-A, TPX2, meme kanseri, protein–protein etkileşim inhibitörü, organoidler