Clear Sky Science · pt
A pequena molécula ATC12 inibe a interação Aurora-A/TPX2 e prejudica a proliferação de células de câncer de mama
Por que esta pesquisa importa para tratamentos futuros do câncer
Muitos medicamentos contra o câncer tentam desligar enzimas que impulsionam a divisão celular, mas frequentemente atingem alvos demais e causam efeitos colaterais, ou falham em ser eficazes em pacientes. Este estudo explora uma tática diferente: em vez de desativar uma enzima, objetiva romper uma parceria específica entre duas proteínas que cooperam para ajudar células de câncer de mama a crescer e sobreviver. Os pesquisadores descobrem e testam uma nova pequena molécula, chamada ATC12, que interfere nessa parceria e desacelera o crescimento de células cancerosas, incluindo células retiradas diretamente de tumores de pacientes.
Uma parceria crucial dentro de células em divisão
Dentro de nossas células, uma enzima chamada Aurora-A ajuda a orquestrar a divisão celular. Outra proteína, TPX2, liga-se à Aurora-A, ajuda a posicioná-la corretamente no andaime intracelular e a estabilizá-la. Juntas formam um par funcional frequentemente encontrado em níveis anormalmente elevados em tumores, incluindo cânceres de mama. Além de seu papel na divisão celular, Aurora-A pode se acumular no núcleo de células cancerosas não-divisoras, onde estimula genes que favorecem o crescimento e a disseminação tumoral. Evidências sugerem que TPX2 também ajuda Aurora-A a alcançar o núcleo. Fármacos tradicionais que bloqueiam a atividade da Aurora-A competindo com ATP mostraram sucesso limitado em ensaios clínicos, em parte porque o sítio de ligação ao ATP é semelhante em muitas enzimas, levando a efeitos fora do alvo. Isso fez com que os pesquisadores buscassem formas mais seletivas de conter os papéis pró-câncer da Aurora-A.

Projetando uma molécula para romper uma ligação proteica
A equipe usou triagem computacional para vasculhar milhões de moléculas comercialmente disponíveis em busca de candidatos que pudessem se encaixar na região de contato onde TPX2 se liga à Aurora-A. Focaram em características químicas conhecidas por serem cruciais para essa interação, como bolsões hidrofóbicos e pontos de ligação “quentes” essenciais. A partir de uma grande seleção inicial, reduziram o conjunto para 184 compostos e, em seguida, para 15 candidatos principais que melhor correspondiam à forma tridimensional e à química da interface. Testes laboratoriais usando espectrometria de massa nativa mostraram que quatro dessas moléculas podiam enfraquecer a ligação de um fragmento de TPX2 à Aurora-A. Experimentos adicionais de dose–resposta identificaram dois compostos, ATC7 e especialmente ATC12, como os mais potentes em deslocar TPX2 da Aurora-A sem bloquear a atividade enzimática da Aurora-A, indicando um efeito específico sobre a parceria em vez do sítio catalítico.
Como o ATC12 afeta células cancerosas e seu comportamento
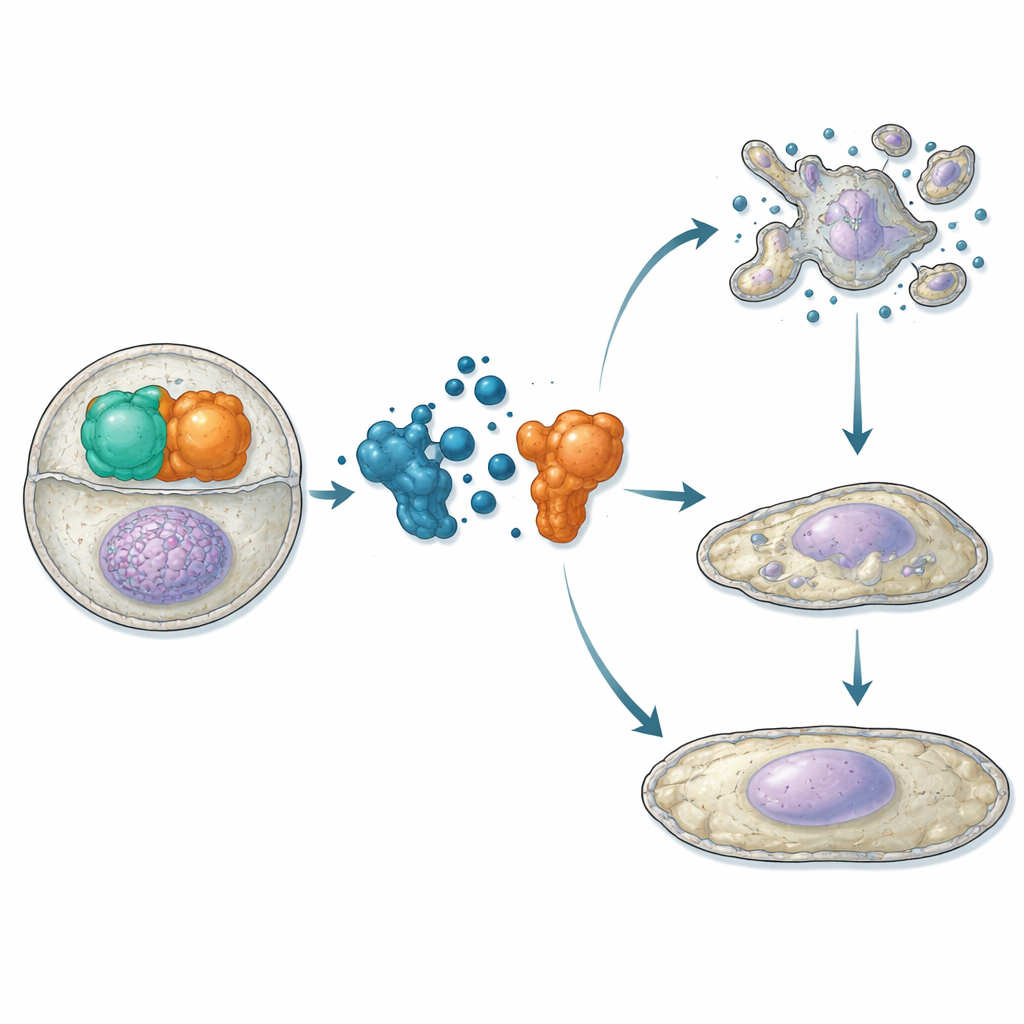
Tendo estabelecido que ATC12 se liga à Aurora-A e compete com TPX2 in vitro, os pesquisadores avançaram para células vivas. Em linhagens de osteossarcoma e câncer de mama, usaram ensaios de proximidade e microscopia para mostrar que o tratamento com ATC12 reduz a interação Aurora-A/TPX2 tanto no fuso mitótico quanto dentro de núcleos em interfase, acompanhado por diminuição do sinal de Aurora-A nesses locais. Em dois modelos de câncer de mama—MCF7 (menos agressivo, receptor hormonal–positivo) e MDA-MB-231 (altamente agressivo, triplo-negativo)—o ATC12 diminuiu a viabilidade celular de forma dependente da dose, enquanto um composto controle que não interrompia a interação não teve efeito. Imagens de lapso temporal revelaram que, em células MCF7, o ATC12 reduziu fortemente a fração de células entrando em mitose, prolongou a duração da mitose para aquelas que se dividiram e levou a morte celular extensiva com sinais bioquímicos de apoptose. Em contraste, células MDA-MB-231 mostraram proliferação mais lenta sem morte significativa; em vez disso, exibiram níveis aumentados do freio do ciclo celular p21, núcleos aumentados e ativação de marcadores de senescência, indicando uma transição para um estado não-divisor permanente.
Testando o ATC12 em modelos 3D e organoides derivados de pacientes
Para imitar melhor o comportamento de tumores no corpo, os cientistas examinaram o ATC12 em culturas tridimensionais. Quando células de câncer de mama foram cultivadas como mamossferas—aglomerados esféricos que enriquecem para células com características de célula-tronco e resistentes a terapia—o ATC12 reduziu tanto a viabilidade quanto o tamanho dessas esferas nos contextos MCF7 e MDA-MB-231, enquanto um inibidor padrão da quinase Aurora-A não diminuiu as esferas. A equipe então avançou para organoides crescidos a partir de biópsias de pacientes com câncer de mama triplo-negativo cujos tumores haviam resistido à quimioterapia. Nesses organoides derivados de pacientes, o ATC12 diminuiu a sobrevivência celular de forma claramente dependente da dose, com concentrações eficazes na faixa de micromolar baixa. Repetir a dose do fármaco no meio do tratamento potencializou ainda mais o efeito, sugerindo que manter níveis de ATC12 ao longo do tempo pode ser importante para a interrupção sustentada do complexo Aurora-A/TPX2.
O que isso significa para a terapia do câncer
Este trabalho reforça a ideia de que romper parcerias proteicas específicas pode ser uma forma potente de desarmar células cancerosas ao mesmo tempo em que evita algumas armadilhas dos inibidores enzimáticos tradicionais. Ao direcionar o complexo Aurora-A/TPX2, o ATC12 interfere tanto com células cancerosas em divisão quanto com células não-divisoras, provocando apoptose ou senescência estável dependendo do perfil genético do tumor. Sua capacidade de prejudicar o crescimento em mamossferas 3D e em organoides de cânceres de mama triplo-negativos difíceis de tratar destaca seu potencial como ponto de partida para novos fármacos, incluindo moléculas refinadas ou degradadores baseados no mesmo esqueleto. Embora sejam necessários mais ajustes para melhorar potência e estabilidade, o estudo demonstra que interromper seletivamente o par Aurora-A/TPX2 é uma estratégia realista e potencialmente valiosa para tratamentos anticâncer futuros.
Citação: Boi, D., Fianco, G., Polverino, F. et al. The ATC12 small molecule inhibits the Aurora-A/TPX2 interaction and impairs the proliferation of breast cancer cells. Cell Death Dis 17, 356 (2026). https://doi.org/10.1038/s41419-026-08579-3
Palavras-chave: Aurora-A, TPX2, câncer de mama, inibidor de interação proteína–proteína, organoides