Clear Sky Science · sv
Den lilla molekylen ATC12 hämmar interaktionen mellan Aurora-A och TPX2 och försämrar proliferation av bröstcancerceller
Varför denna forskning är viktig för framtida cancerbehandlingar
Många cancerläkemedel försöker stänga av enzymer som driver celldelning, men de träffar ofta för många mål och orsakar biverkningar, eller fungerar dåligt i patienter. Denna studie undersöker en annan strategi: i stället för att stänga av ett enzym försöker man bryta upp ett specifikt partnerskap mellan två proteiner som samarbetar för att hjälpa bröstcancerceller att växa och överleva. Forskarna hittar och testar en ny liten molekyl, kallad ATC12, som stör detta partnerskap och bromsar tillväxten av cancerceller, inklusive celler tagna direkt från patienttumörer.
En avgörande samverkan i delande celler
I våra celler hjälper ett enzym som kallas Aurora-A till att organisera celldelningen. Ett annat protein, TPX2, binder Aurora-A, hjälper till att positionera det korrekt på cellens inre skelett och stabiliserar det. Tillsammans bildar de ett funktionellt par som ofta förekommer i onormalt höga nivåer i tumörer, inklusive bröstcancer. Förutom sin roll i celldelning kan Aurora-A ansamlas i kärnan hos icke-delande cancerceller, där det aktiverar gener som gynnar tumörtillväxt och spridning. Data tyder på att TPX2 också hjälper Aurora-A att nå kärnan. Traditionella läkemedel som blockerar Aurora-A:s aktivitet genom att konkurrera med ATP har visat begränsad framgång i kliniska prövningar, delvis eftersom ATP-bindningsplatsen liknar den hos många enzymer och leder till off-target-effekter. Det har drivit forskare att söka mer selektiva sätt att dämpa Aurora-A:s cancerbefrämjande roller.

Att designa en molekyl som bryter ett proteinknut
Gruppen använde datorbaserad screening för att söka igenom miljontals köpta molekyler efter kandidater som kunde passa in i kontaktregionen där TPX2 binder Aurora-A. De fokuserade på kemiska egenskaper som är avgörande för denna interaktion, såsom hydrofoba fickor och viktiga bindnings"hot spots". Från en initial stor pool begränsades urvalet till 184 föreningar och sedan till 15 toppkandidater som bäst matchade gränssnittets tredimensionella form och kemi. Laboratorietester med native masspektrometri visade att fyra av dessa molekyler kunde försvaga bindningen av en TPX2-fragment till Aurora-A. Ytterligare dos-respons-experiment identifierade två föreningar, ATC7 och särskilt ATC12, som mest potenta för att förtränga TPX2 från Aurora-A utan att blockera Aurora-A:s enzymatiska aktivitet, vilket indikerar en specifik effekt på partnerskapet snarare än på det katalytiska stället.
Hur ATC12 påverkar cancerceller och deras beteende
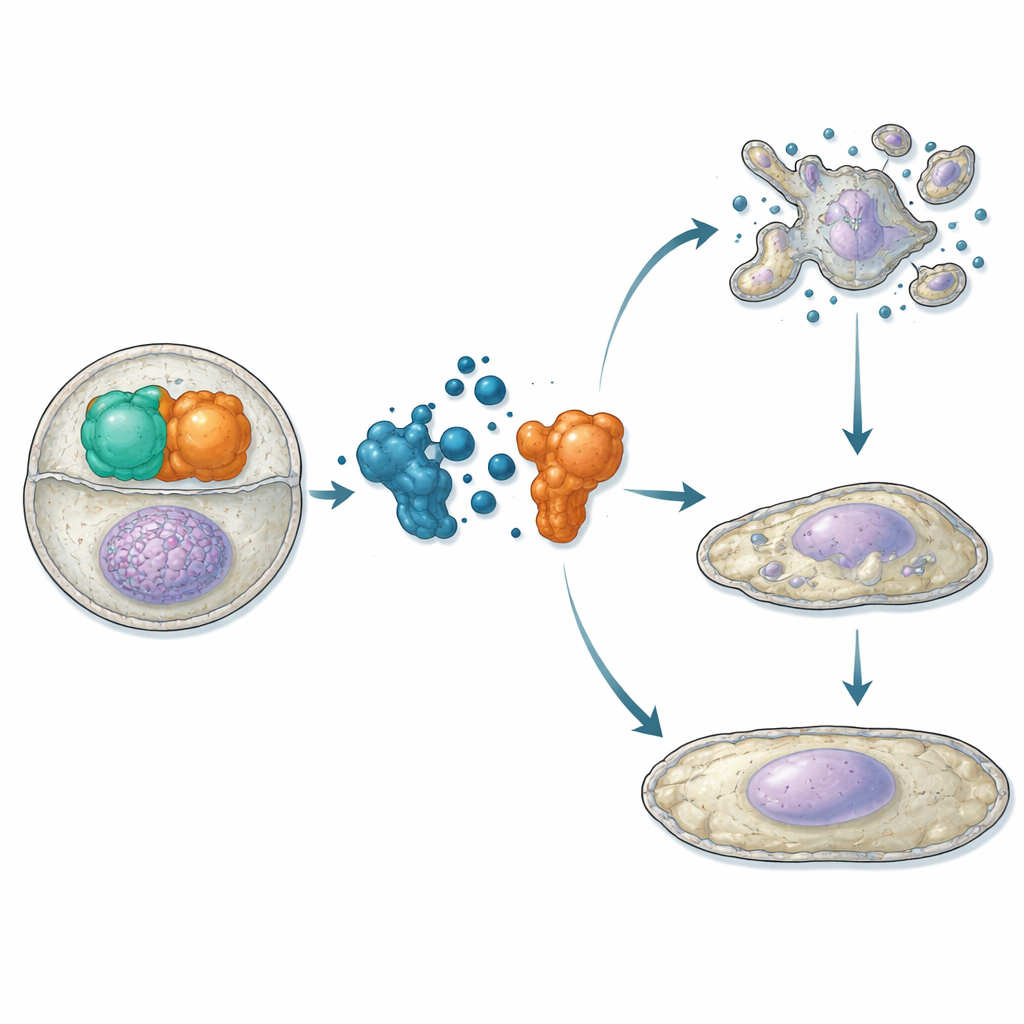
När forskarna hade fastställt att ATC12 binder Aurora-A och konkurrerar med TPX2 in vitro, gick de vidare till levande celler. I osteosarkom- och bröstcancercellinjer använde de proximetsassays och mikroskopi för att visa att ATC12-behandling minskar Aurora-A/TPX2-interaktionen både vid mitotiska spindeln och inne i interfasens kärnor, åtföljt av minskad Aurora-A-signal på dessa platser. I två bröstcancermodeller—MCF7 (mindre aggressiv, hormonreceptor-positiv) och MDA-MB-231 (mycket aggressiv, trippel-negativ)—sänkte ATC12 cellviabiliteten på ett dosberoende sätt, medan en kontrollförening som inte störde interaktionen inte hade någon effekt. Tidsförloppstagning visade att i MCF7-celler minskade ATC12 kraftigt andelen celler som går in i mitos, förlängde mitosens varaktighet för de som delade sig och ledde till omfattande celldöd med biokemiska tecken på apoptos. I kontrast visade MDA-MB-231-celler en fördröjd proliferation utan betydande död; istället uppvisade de ökade nivåer av cellcykelhämmaren p21, förstorade kärnor och aktivering av senescensmarkörer, vilket indikerar en övergång till ett permanent icke-delande tillstånd.
Test av ATC12 i 3D-modeller och patientavledda organoider
För att bättre efterlikna tumörers beteende i kroppen undersökte forskarna ATC12 i tredimensionella odlingar. När bröstcancerceller odlades som mammosphärer—sfäriska kluster som berikar för stamliknande, terapiresistenta celler—minskade ATC12 både deras viabilitet och storlek i både MCF7- och MDA-MB-231-bakgrunder, medan en standard Aurora-A-kinas-hämmare inte förminskade sfärerna. Gruppen gick sedan vidare till organoider odlade från biopsier från trippel-negativa bröstcancerpatienter vars tumörer var resistenta mot kemoterapi. I dessa patientavledda organoider minskade ATC12 cellsurvivalen tydligt i ett dosberoende förlopp, med effektiva koncentrationer i låga mikromolära området. Att upprepa dosen mitt i behandlingen förstärkte effekten, vilket antyder att bibehållna nivåer av ATC12 över tid kan vara viktiga för fortsatt störning av Aurora-A/TPX2-komplexet.
Vad detta betyder för cancerterapi
Detta arbete stödjer idén att bryta specifika proteinpartnerskap kan vara ett kraftfullt sätt att oskadliggöra cancerceller samtidigt som man undviker vissa fallgropar med traditionella enzymhämmare. Genom att rikta in sig på Aurora-A/TPX2-komplexet stör ATC12 både delande och icke-delande cancerceller, vilket framkallar antingen celldöd eller stabil senescens beroende på tumörens genetiska uppsättning. Dess förmåga att försämra tillväxt i 3D-mammosphärer och i organoider från svårbehandlade trippel-negativa bröstcancerfall framhäver dess potential som utgångspunkt för nya läkemedel, inklusive förfinade molekyler eller degraderare byggda på samma stomme. Medan ytterligare optimering krävs för att förbättra potens och stabilitet visar studien att selektiv störning av Aurora-A/TPX2-paret är en realistisk och potentiellt värdefull strategi för framtida antitumörbehandlingar.
Citering: Boi, D., Fianco, G., Polverino, F. et al. The ATC12 small molecule inhibits the Aurora-A/TPX2 interaction and impairs the proliferation of breast cancer cells. Cell Death Dis 17, 356 (2026). https://doi.org/10.1038/s41419-026-08579-3
Nyckelord: Aurora-A, TPX2, bröstcancer, hämmare av protein–protein-interaktion, organoider