Clear Sky Science · nl
Het kleine molecuul ATC12 remt de interactie tussen Aurora-A en TPX2 en belemmert de proliferatie van borstkankercellen
Waarom dit onderzoek van belang is voor toekomstige kankerbehandelingen
Veel kankergeneesmiddelen proberen enzymen die celdeling aansturen uit te schakelen, maar ze raken vaak te veel doelen en veroorzaken bijwerkingen, of ze blijken in patiënten onvoldoende effectief. Deze studie onderzoekt een andere tactiek: in plaats van een enzym uit te zetten, probeert men een specifieke samenwerking tussen twee eiwitten te verbreken die borstkankercellen helpen groeien en overleven. De onderzoekers ontdekken en testen een nieuw klein molecuul, ATC12, dat deze samenwerking verstoort en de groei van kankercellen vertraagt, inclusief cellen rechtstreeks afkomstig uit patiëntentumoren.
Een cruciale samenwerking in delende cellen
In onze cellen helpt een enzym genaamd Aurora-A de celdeling te coördineren. Een ander eiwit, TPX2, bindt aan Aurora-A, helpt het correct te positioneren op het interne celraamwerk en stabiliseert het. Samen vormen ze een functioneel paar dat vaak in abnormaal hoge niveaus voorkomt in tumoren, waaronder borstkankers. Buiten zijn rol in celdeling kan Aurora-A zich ophopen in de kern van niet-delende kankercellen, waar het genen activeert die tumorgroei en -uitzaaiing bevorderen. Bewijs suggereert dat TPX2 ook helpt Aurora-A naar de kern te brengen. Traditionele geneesmiddelen die de activiteit van Aurora-A blokkeren door te concurreren met ATP hebben beperkte klinische successen laten zien, deels omdat de ATP-bindingsplaats op veel enzymen lijkt en daardoor off-target effecten veroorzaakt. Dit heeft onderzoekers ertoe aangezet selectievere manieren te zoeken om de kankerversterkende rollen van Aurora-A te remmen.

Ontwerpen van een molecuul om een eiwitverbinding te verbreken
Het team gebruikte computergebaseerde screening om miljoenen verkrijgbare moleculen te doorzoeken op kandidaten die in het contactgebied waar TPX2 aan Aurora-A bindt zouden passen. Ze concentreerden zich op chemische kenmerken die belangrijk zijn voor deze interactie, zoals hydrofobe pockets en sleutelbindings "hot spots." Uit een aanvankelijk grote groep beperkten ze de selectie tot 184 verbindingen en vervolgens tot 15 toppers die het beste overeenkwamen met de driedimensionale vorm en chemie van het interface. Laboratoriumtests met native massaspectrometrie toonden aan dat vier van deze moleculen de binding van een TPX2-fragment aan Aurora-A konden verzwakken. Verdere dosis-responsexperimenten identificeerden twee verbindingen, ATC7 en vooral ATC12, als de krachtigste in het verdrijven van TPX2 van Aurora-A zonder de enzymatische activiteit van Aurora-A te blokkeren, wat wijst op een specifiek effect op de samenwerking in plaats van op het katalytische domein.
Hoe ATC12 kankercellen en hun gedrag beïnvloedt
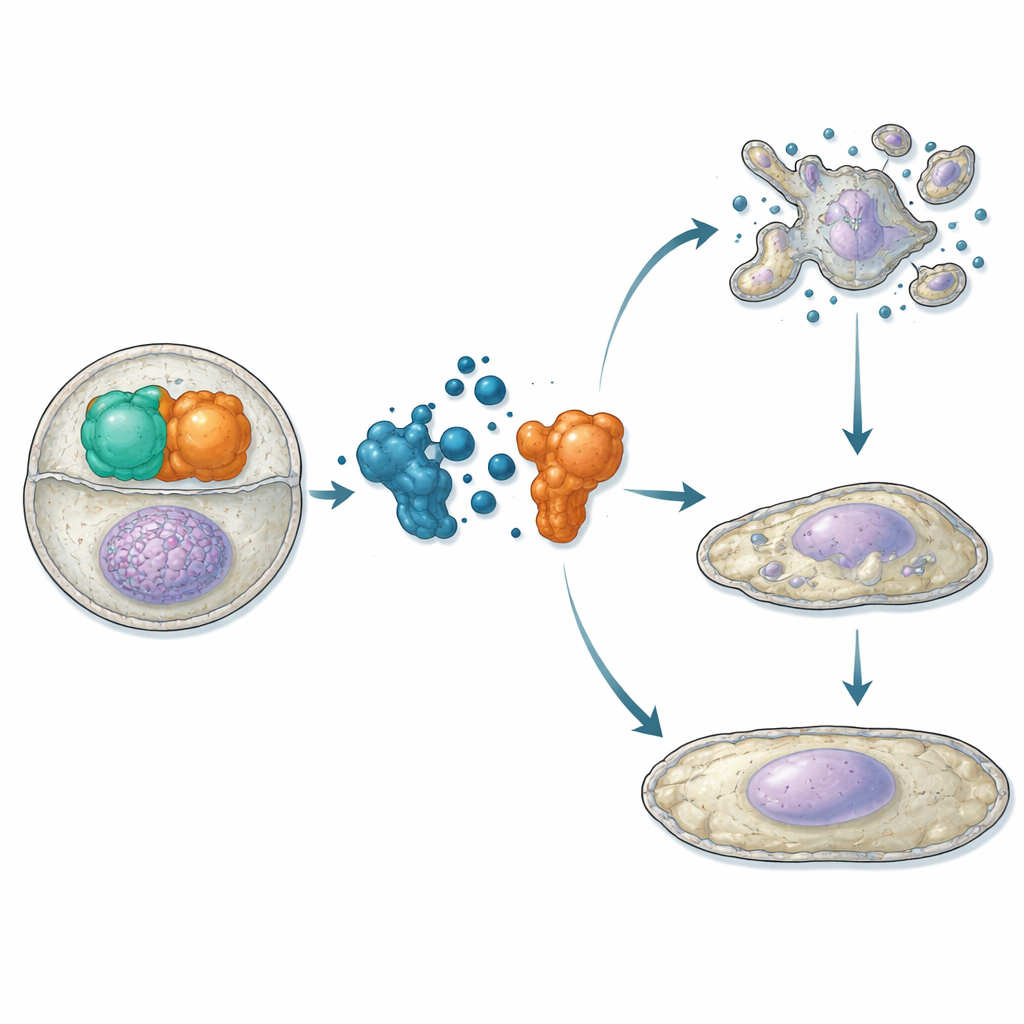
Nadat was vastgesteld dat ATC12 aan Aurora-A bindt en concurreert met TPX2 in vitro, gingen de onderzoekers naar levende cellen. In osteosarcoom- en borstkankercellijnen gebruikten ze proximiteitsassays en microscopie om te laten zien dat ATC12-behandeling de Aurora-A/TPX2-interactie vermindert zowel aan het mitotische spinnenweb als in interfase-kernen, gepaard met een afname van het Aurora-A-signaal op deze locaties. In twee borstkankermodellen—MCF7 (minder agressief, hormoonreceptor-positief) en MDA-MB-231 (zeer agressief, triple-negatief)—verlaagde ATC12 de celviabiliteit in een dosisafhankelijke manier, terwijl een controleverbinding die de interactie niet verstoorde geen effect had. Time-lapsebeelden toonden aan dat ATC12 in MCF7-cellen het aandeel cellen dat mitose inging sterk verminderde, de duur van de mitose verlengde voor degenen die wel deelden, en leidde tot uitgebreide celdood met biochemische kenmerken van apoptose. In tegenstelling daarmee toonden MDA-MB-231-cellen vertraagde proliferatie zonder significante celdood; in plaats daarvan lieten ze verhoogde niveaus van de celcyclusremmer p21 zien, vergrote kernen en activering van senescencemarkers, wat wijst op een verschuiving naar een permanente niet-delende toestand.
Testen van ATC12 in 3D-modellen en patient-afgeleide organoïden
Om het gedrag van tumoren in het lichaam beter na te bootsen, onderzochten de wetenschappers ATC12 in driedimensionale kweekmodellen. Wanneer borstkankercellen als mammosferen werden gekweekt—sferische clusters die verrijking geven voor stamachtige, therapieresistente cellen—verminderde ATC12 zowel hun levensvatbaarheid als omvang in zowel MCF7- als MDA-MB-231-achtergronden, terwijl een standaard Aurora-A-kinaseremmer de sferen niet verkleinde. Het team ging vervolgens over op organoïden gekweekt uit biopsieën van triple-negatieve borstkankerpatiënten wier tumoren resistent waren tegen chemotherapie. In deze patiënt-afgeleide organoïden verlaagde ATC12 de overleving van cellen op duidelijke dosisafhankelijke wijze, met effectieve concentraties in het lage micromolaire bereik. Het herhalen van de dosis halverwege de behandeling versterkte het effect verder, wat suggereert dat het handhaven van ATC12-niveaus in de tijd belangrijk kan zijn voor aanhoudende verstoring van het Aurora-A/TPX2-complex.
Wat dit betekent voor kankertherapie
Dit werk ondersteunt het idee dat het verbreken van specifieke eiwitsamenwerkingen een krachtige manier kan zijn om kankercellen te ontwapenen en tegelijkertijd sommige nadelen van traditionele enzymremmers te vermijden. Door het Aurora-A/TPX2-complex te richten, verstoort ATC12 zowel delende als niet-delende kankercellen en veroorzaakt het afhankelijk van de genetische samenstelling van de tumor ofwel celdood ofwel stabiele senescentie. Het vermogen om groei te remmen in 3D-mammosferen en in organoïden van moeilijk te behandelen triple-negatieve borstkankers onderstreept het potentieel als uitgangspunt voor nieuwe geneesmiddelen, inclusief verfijnde moleculen of degrader-constructies op hetzelfde skelet. Hoewel verdere optimalisatie nodig is om potentie en stabiliteit te verbeteren, toont de studie aan dat selectieve verstoring van het Aurora-A/TPX2-paar een haalbare en mogelijk waardevolle strategie is voor toekomstige anti-kankerbehandelingen.
Bronvermelding: Boi, D., Fianco, G., Polverino, F. et al. The ATC12 small molecule inhibits the Aurora-A/TPX2 interaction and impairs the proliferation of breast cancer cells. Cell Death Dis 17, 356 (2026). https://doi.org/10.1038/s41419-026-08579-3
Trefwoorden: Aurora-A, TPX2, borstkanker, remmer van eiwit–eiwitinteractie, organoïden