Clear Sky Science · es
La pequeña molécula ATC12 inhibe la interacción Aurora-A/TPX2 y dificulta la proliferación de células de cáncer de mama
Por qué esta investigación importa para futuros tratamientos contra el cáncer
Muchos fármacos contra el cáncer intentan bloquear enzimas que impulsan la división celular, pero a menudo alcanzan demasiados blancos y provocan efectos secundarios, o no funcionan bien en pacientes. Este estudio explora una táctica distinta: en lugar de apagar una enzima, busca romper una asociación específica entre dos proteínas que cooperan para ayudar a las células de cáncer de mama a crecer y sobrevivir. Los investigadores descubren y prueban una nueva molécula pequeña, llamada ATC12, que interfiere con esa asociación y ralentiza el crecimiento de células cancerosas, incluidas células tomadas directamente de tumores de pacientes.
Una asociación crucial dentro de las células en división
Dentro de nuestras células, una enzima llamada Aurora-A ayuda a coordinar la división celular. Otra proteína, TPX2, se une a Aurora-A, le ayuda a posicionarse correctamente en el armazón interno de la célula y la estabiliza. Juntas forman una pareja funcional que a menudo se encuentra en niveles anormalmente altos en tumores, incluidos los cánceres de mama. Más allá de su papel en la división celular, Aurora-A puede acumularse en el núcleo de células cancerosas no en división, donde potencia genes que favorecen el crecimiento y la diseminación tumoral. Las evidencias sugieren que TPX2 también ayuda a Aurora-A a llegar al núcleo. Los fármacos tradicionales que bloquean la actividad de Aurora-A compitiendo con el ATP han mostrado éxito limitado en ensayos clínicos, en parte porque el sitio de unión al ATP es similar en muchas enzimas, lo que conduce a efectos fuera de diana. Esto ha impulsado a los investigadores a buscar formas más selectivas de frenar los papeles promotores del cáncer de Aurora-A.

Diseñar una molécula para romper un vínculo proteico
El equipo utilizó cribado por ordenador para buscar entre millones de moléculas comercializables candidatos que pudieran encajar en la región de contacto donde TPX2 se une a Aurora-A. Se centraron en características químicas conocidas por ser cruciales para esta interacción, como bolsillos hidrofóbicos y «puntos calientes» clave de unión. A partir de una gran colección inicial, redujeron el número a 184 compuestos y luego a 15 candidatos principales que mejor coincidían con la forma tridimensional y la química de la interfaz. Pruebas de laboratorio mediante espectrometría de masas nativa mostraron que cuatro de estas moléculas podían debilitar la unión de un fragmento de TPX2 a Aurora-A. Experimentos adicionales de dosis-respuesta identificaron dos compuestos, ATC7 y especialmente ATC12, como los más potentes para desplazar a TPX2 de Aurora-A sin bloquear la actividad enzimática de Aurora-A, lo que indica un efecto específico sobre la asociación más que sobre el sitio catalítico.
Cómo afecta ATC12 a las células cancerosas y su comportamiento
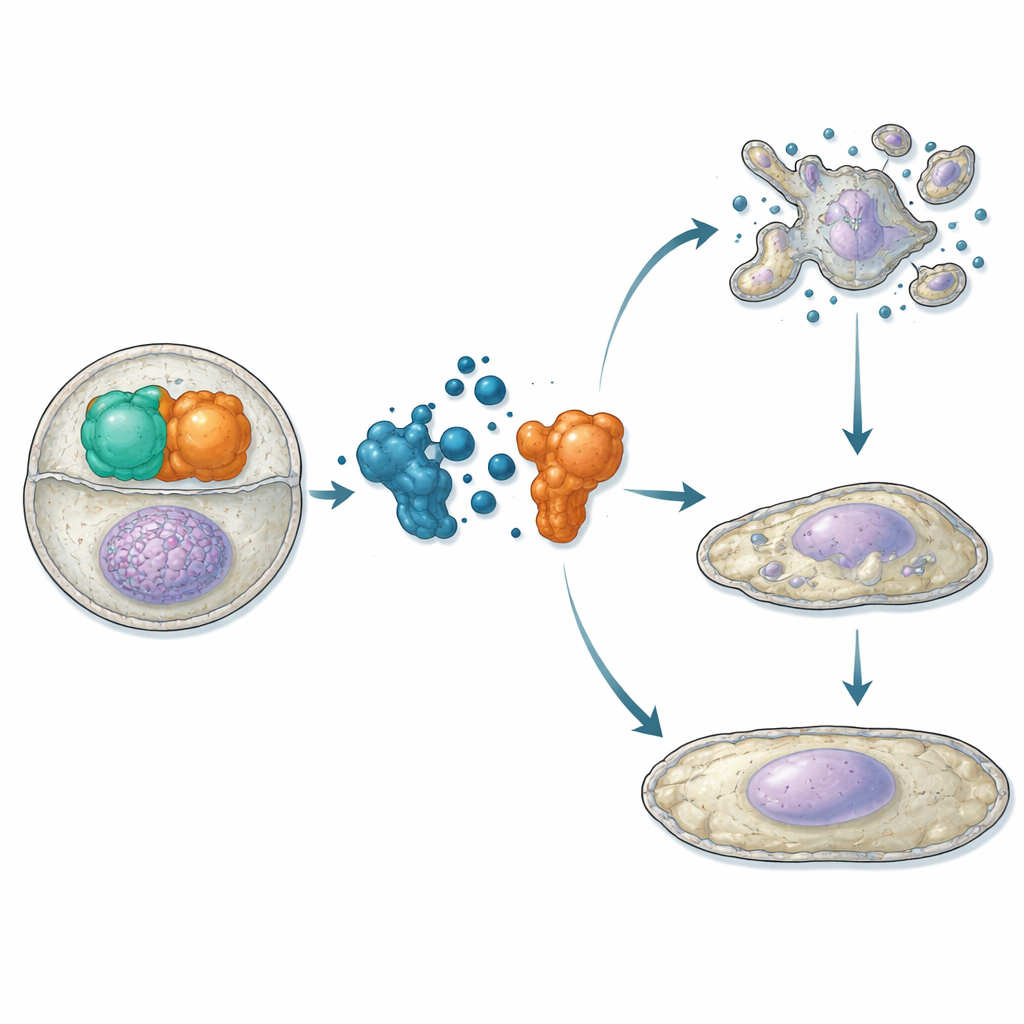
Habiendo establecido que ATC12 se une a Aurora-A y compite con TPX2 in vitro, los investigadores pasaron a células vivas. En líneas celulares de osteosarcoma y cáncer de mama, emplearon ensayos de proximidad y microscopía para mostrar que el tratamiento con ATC12 reduce la interacción Aurora-A/TPX2 tanto en el huso mitótico como dentro de los núcleos en interfase, acompañado de una señal disminuida de Aurora-A en estos lugares. En dos modelos de cáncer de mama—MCF7 (menos agresivo, positivo para receptores hormonales) y MDA-MB-231 (muy agresivo, triple negativas)—ATC12 redujo la viabilidad celular de manera dependiente de la dosis, mientras que un compuesto de control que no interrumpía la interacción no tuvo efecto. Imágenes en tiempo real revelaron que en las células MCF7 ATC12 redujo drásticamente la fracción de células que entran en mitosis, prolongó la duración de la mitosis en las que sí se dividieron y condujo a muerte celular extensa con signos bioquímicos de apoptosis. En contraste, las células MDA-MB-231 mostraron una proliferación más lenta sin muerte significativa; en su lugar exhibieron niveles aumentados del freno del ciclo celular p21, núcleos agrandados y activación de marcadores de senescencia, indicando un cambio hacia un estado no proliferativo y permanente.
Probar ATC12 en modelos 3D y organoides derivados de pacientes
Para imitar mejor el comportamiento de los tumores en el organismo, los científicos examinaron ATC12 en cultivos tridimensionales. Cuando las células de cáncer de mama se cultivaron como mamósferas—aglomerados esféricos que enriquecen células de tipo madre y resistentes a la terapia—ATC12 redujo tanto su viabilidad como su tamaño en los fondos tanto de MCF7 como de MDA-MB-231, mientras que un inhibidor estándar de la quinasa Aurora-A no redujo las esferas. El equipo pasó luego a organoides cultivados a partir de biopsias de pacientes con cáncer de mama triple negativo cuyos tumores habían resistido la quimioterapia. En estos organoides derivados de pacientes, ATC12 disminuyó la supervivencia celular de forma claramente dependiente de la dosis, con concentraciones eficaces en el rango micromolar bajo. Repetir la dosis del fármaco a mitad del tratamiento potenció aún más el efecto, lo que sugiere que mantener niveles de ATC12 a lo largo del tiempo podría ser importante para la interrupción sostenida del complejo Aurora-A/TPX2.
Qué significa esto para la terapia contra el cáncer
Este trabajo respalda la idea de que romper asociaciones proteicas específicas puede ser una forma poderosa de desactivar células cancerosas evitando algunas trampas de los inhibidores enzimáticos tradicionales. Al dirigirse al complejo Aurora-A/TPX2, ATC12 interfiere tanto con células cancerosas en división como con las no divididas, provocando ya sea muerte celular o senescencia estable según el perfil genético del tumor. Su capacidad para reducir el crecimiento en mamósferas 3D y en organoides de cánceres de mama triple negativos difíciles de tratar destaca su potencial como punto de partida para nuevos fármacos, incluidos compuestos refinados o degradadores basados en el mismo andamiaje. Aunque se necesita optimización adicional para mejorar la potencia y la estabilidad, el estudio demuestra que la interrupción selectiva de la pareja Aurora-A/TPX2 es una estrategia realista y potencialmente valiosa para futuros tratamientos anticancerígenos.
Cita: Boi, D., Fianco, G., Polverino, F. et al. The ATC12 small molecule inhibits the Aurora-A/TPX2 interaction and impairs the proliferation of breast cancer cells. Cell Death Dis 17, 356 (2026). https://doi.org/10.1038/s41419-026-08579-3
Palabras clave: Aurora-A, TPX2, cáncer de mama, inhibidor de interacción proteína–proteína, organoides