Clear Sky Science · ar
المركب الصغير ATC12 يعيق تداخل Aurora-A/TPX2 ويُضعف تكاثر خلايا سرطان الثدي
لماذا يهم هذا البحث لعلاجات السرطان المستقبلية
تحاول العديد من أدوية السرطان إيقاف الإنزيمات التي تحفز انقسام الخلايا، لكنها غالباً تصيب أهدافاً متعددة مسببة آثاراً جانبية، أو تفشل في أداء دورها جيداً لدى المرضى. يستكشف هذا البحث استراتيجية مختلفة: بدلاً من تعطيل إنزيم بالكامل، يهدف إلى تفكيك شراكة محددة بين بروتينين يتعاونان لمساعدة خلايا سرطان الثدي على النمو والبقاء. يكتشف الباحثون ويختبرون جزيئاً صغيراً جديداً اسمه ATC12، يتداخل مع هذه الشراكة ويبطئ نمو الخلايا السرطانية، بما في ذلك خلايا مأخوذة مباشرة من أورام المرضى.
شراكة حاسمة داخل الخلايا المنقسمة
داخل خلايانا، يساعد إنزيم يُدعى Aurora-A في تنظيم انقسام الخلايا. يرتبط به بروتين آخر، TPX2، يساعد على وضعه بشكل صحيح على الهيكل الخلوي الداخلي ويثبته. معاً يشكلان ثنائياً وظيفياً يوجد غالباً بمستويات مرتفعة غير طبيعية في الأورام، بما في ذلك سرطانات الثدي. إلى جانب دوره في انقسام الخلايا، يمكن أن يتراكم Aurora-A في نواة الخلايا السرطانية غير المنقسمة، حيث يعزز جينات تُفضّل نمو الورم وانتشاره. تشير الأدلة إلى أن TPX2 يساعد أيضاً Aurora-A على الوصول إلى النواة. الأدوية التقليدية التي تحجب نشاط Aurora-A عن طريق التنافس مع ATP أظهرت نجاحاً محدوداً في التجارب السريرية، جزئياً لأن موقع ربط ATP يشبه مواقع في إنزيمات عديدة، مما يؤدي إلى تأثيرات خارج الهدف. دفع هذا الباحثين للبحث عن طرق أكثر انتقائية لكبح أدوار Aurora-A المساعدة للسرطان.

تصميم جزيء يفك رابطة بروتينية
استخدم الفريق فحصاً حاسوبياً للبحث في ملايين الجزيئات القابلة للشراء عن مرشحين يمكن أن يتناسبوا مع منطقة التلامس حيث يرتبط TPX2 بـ Aurora-A. ركزوا على الميزات الكيميائية المعروفة بأنها محورية لهذا التفاعل، مثل الجيوب الكارهة للماء ونقاط الارتباط الحرجة. من مجموعة كبيرة أولية، ضيّقوا المجال إلى 184 مركباً، ثم إلى 15 مرشحاً رئيسياً تطابقوا أفضل مع الشكل ثلاثي الأبعاد وكيمياء الواجهة. أظهرت اختبارات مخبرية باستخدام مطيافية الكتلة الطبيعية أن أربعة من هذه الجزيئات يمكن أن تضعف ارتباط قطعة من TPX2 بـ Aurora-A. حددت تجارب الاستجابة للجرعة بعد ذلك مركبين، ATC7 وخاصة ATC12، كالأقوى في إزاحة TPX2 عن Aurora-A دون حجب نشاط الإنزيم لـ Aurora-A، مما يشير إلى تأثير محدد على الشراكة وليس على الموقع الحفاز.
كيف يؤثر ATC12 على الخلايا السرطانية وسلوكها
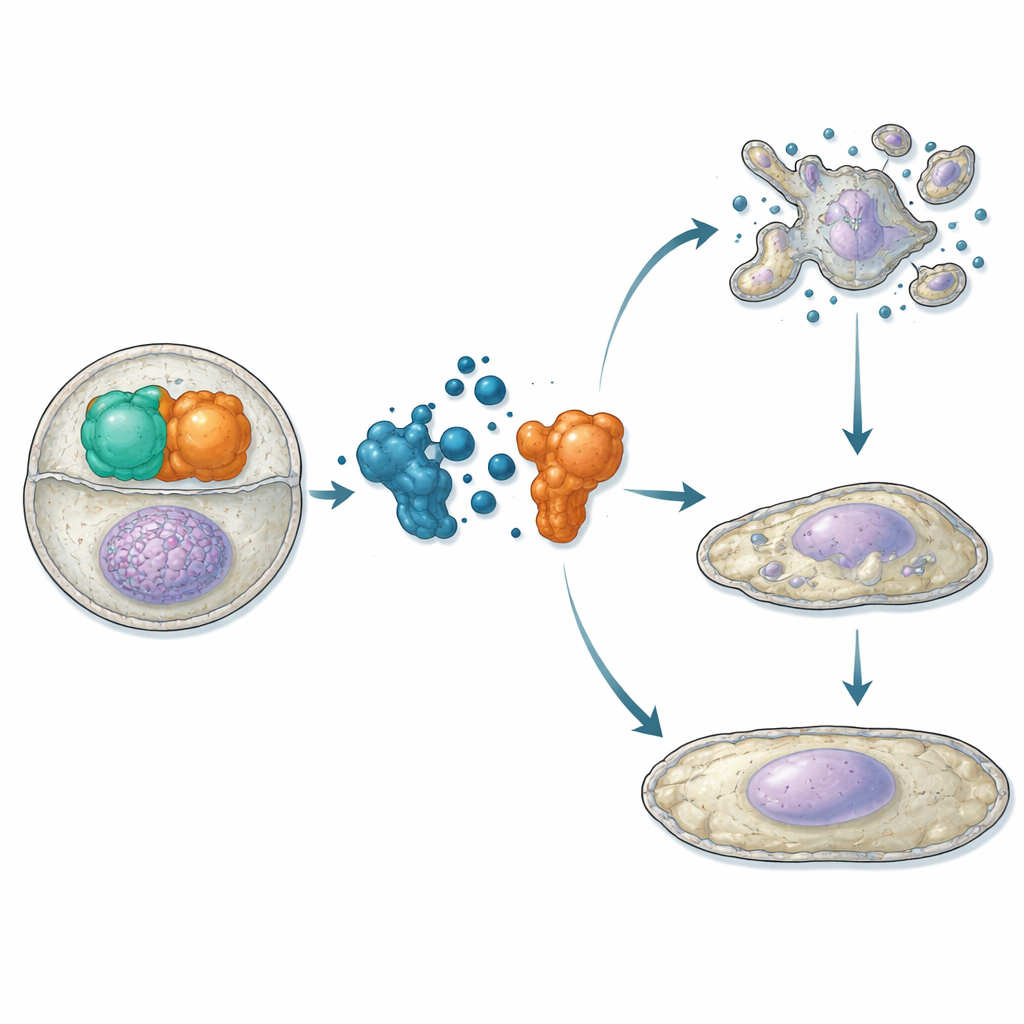
بعد إثبات أن ATC12 يرتبط بـ Aurora-A ويتنافس مع TPX2 في المختبر، انتقل الباحثون إلى الخلايا الحية. في خطوط خلايا الساركوما العظمية وسرطان الثدي، استخدموا اختبارات التقارب والمجهر لإظهار أن علاج ATC12 يقلل تداخل Aurora-A/TPX2 سواء عند المغزل الانقسامي أو داخل النوى في الطور البيني، مصحوباً بانخفاض إشارة Aurora-A في هذه المواقع. في نموذجي سرطان ثدي—MCF7 (أقل عدوانية، موجّه بالهرمونات) وMDA-MB-231 (عدواني جداً، ثلاثي السلبية)—قلّل ATC12 من قابلية بقاء الخلايا بصفة معتمدة على الجرعة، بينما لم يبدُ للمركب الضابط الذي لا يعيق التداخل أي تأثير. أظهرت تصويرات الوقت الحقيقي أن ATC12 في خلايا MCF7 خفّض كثيراً نسبة الخلايا التي تدخل الانقسام، وأطال مدة الانقسام لدى الخلايا التي انقسمت، وأدى إلى موت خلوي واسع مع علامات بيوكيميائية للموت المبرمج. بالمقابل، أظهرت خلايا MDA-MB-231 تباطؤاً في التكاثر دون موت واضح؛ بدلاً من ذلك ارتفعت مستويات مثبط دورة الخلية p21، وتضخمت النوى، وتنشيط مؤشرات الشيخوخة الخلوية، مما يدل على انتقال إلى حالة عدم انقسام دائمة.
اختبار ATC12 في نماذج ثلاثية الأبعاد وأورغانويدز مشتقة من مرضى
لمحاكاة سلوك الأورام في الجسم بشكل أفضل، فحص العلماء ATC12 في زراعة ثلاثية الأبعاد. عندما نمت خلايا سرطان الثدي ككرات ثديية—عناقيد كروية تُثري الخلايا الشبيهة بالجذع والمقاومة للعلاج—خفض ATC12 كل من قابلية بقاء هذه الكرات وحجمها في كل من خلفيتي MCF7 وMDA-MB-231، بينما لم يقلص مثبط كيناز Aurora-A القياسي هذه الكرات. ثم انتقل الفريق إلى أورغانويدز مزروعة من خزعات لمرضى سرطان ثدي ثلاثي السلبية كانت أورامهم مقاومة للعلاج الكيميائي. في هذه الأورغانويدز المأخوذة من المرضى، قلّل ATC12 بوضوح بقاء الخلايا بصفة معتمدة على الجرعة، بتركيزات فعّالة في نطاق الميكرومولار المنخفض. عزّز تكرار جرعة الدواء منتصف فترة العلاج التأثير، مما يشير إلى أن الحفاظ على مستويات ATC12 مع مرور الوقت قد يكون مهماً لتعطيل مستمر لمركب Aurora-A/TPX2.
ماذا يعني هذا لعلاج السرطان
يدعم هذا العمل فكرة أن تفكيك شراكات بروتينية محددة يمكن أن يكون وسيلة فعّالة لتعطيل الخلايا السرطانية مع تجنّب بعض إخفاقات مثبطات الإنزيم التقليدية. باستهداف مركب Aurora-A/TPX2، يتداخل ATC12 مع الخلايا السرطانية المنقسمة وغير المنقسمة على حد سواء، محدثاً إما موت الخلايا أو شيخوخة ثابتة اعتماداً على البنية الجينية للورم. تبرز قدرته على إضعاف النمو في الكرات الثلاثية الأبعاد وفي أورغانويدز مأخوذة من سرطانات ثدي ثلاثية السلبية صعبة العلاج كدليل على وعده كنقطة انطلاق لأدوية جديدة، تشمل جزيئات مصقولة أو عوامل تحلل مبنية على نفس السقالة. ورغم الحاجة لمزيد من التحسين لرفع الفعالية والثبات، تُظهر الدراسة أن تعطيل ثنائي Aurora-A/TPX2 بشكل انتقائي هو استراتيجية واقعية وذات قيمة محتملة لعلاجات مضادة للسرطان في المستقبل.
الاستشهاد: Boi, D., Fianco, G., Polverino, F. et al. The ATC12 small molecule inhibits the Aurora-A/TPX2 interaction and impairs the proliferation of breast cancer cells. Cell Death Dis 17, 356 (2026). https://doi.org/10.1038/s41419-026-08579-3
الكلمات المفتاحية: Aurora-A, TPX2, سرطان الثدي, مثبط تداخل بروتين–بروتين, أورغانويدز