Clear Sky Science · pl
Mała cząsteczka ATC12 hamuje interakcję Aurora-A/TPX2 i ogranicza proliferację komórek raka piersi
Dlaczego te badania mają znaczenie dla przyszłych terapii przeciwnowotworowych
Wiele leków przeciwnowotworowych stara się wyłączyć enzymy napędzające podział komórek, ale często atakują zbyt wiele celów i powodują skutki uboczne, albo nie działają dobrze u pacjentów. W tym badaniu rozważana jest inna taktyka: zamiast wyłączać enzym, celem jest zerwanie konkretnego partnerstwa między dwoma białkami, które współpracują, aby pomagać komórkom raka piersi rosnąć i przeżyć. Naukowcy odkrywają i testują nową małą cząsteczkę nazwaną ATC12, która zakłóca to partnerstwo i spowalnia wzrost komórek nowotworowych, w tym komórek pobranych bezpośrednio z guzów pacjentów.
Kluczowe partnerstwo wewnątrz dzielących się komórek
W naszych komórkach enzym Aurora-A pomaga koordynować podział komórkowy. Inne białko, TPX2, wiąże się z Aurora-A, pomaga właściwie je umiejscowić na wewnętrznym szkielecie komórki i stabilizuje je. Razem tworzą funkcjonalny duet, który często występuje w nadmiarze w guzach, w tym w raku piersi. Poza rolą w podziale komórek, Aurora-A może gromadzić się w jądrze komórek nowotworowych niepodzielających się, gdzie zwiększa aktywność genów sprzyjających wzrostowi i rozsiewowi guza. Dowody sugerują, że TPX2 także pomaga Aurora-A dotrzeć do jądra. Tradycyjne leki blokujące aktywność Aurora-A przez konkurencję z ATP wykazały ograniczone powodzenie w badaniach klinicznych, częściowo dlatego, że miejsce wiązania ATP wygląda podobnie w wielu enzymach, co prowadzi do efektów pozacelowych. To skłoniło badaczy do poszukiwania bardziej selektywnych sposobów tłumienia nowotworowych funkcji Aurora-A.

Projektowanie cząsteczki do przerwania wiązania białek
Zespół wykorzystał komputacyjne przesiewanie, aby przejrzeć miliony dostępnych do kupienia cząsteczek i znaleźć kandydatów, którzy mogliby wpasować się w region kontaktowy, gdzie TPX2 łączy się z Aurora-A. Skupili się na cechach chemicznych uznanych za kluczowe dla tej interakcji, takich jak hydrofobowe kieszenie i istotne „gorące miejsca” wiążące. Z dużej początkowej puli wyselekcjonowano 184 związki, a następnie 15 najlepszych kandydatów, które najlepiej odpowiadały trójwymiarowemu kształtowi i chemii interfejsu. Testy laboratoryjne z użyciem natywnej spektrometrii mas wykazały, że cztery z tych cząsteczek mogą osłabić wiązanie fragmentu TPX2 z Aurora-A. Dalsze eksperymenty zależności dawka–odpowiedź zidentyfikowały dwa związki, ATC7 i szczególnie ATC12, jako najsilniejsze w wypieraniu TPX2 z Aurora-A bez blokowania aktywności enzymatycznej Aurora-A, co sugeruje specyficzny efekt na partnerstwo, a nie na miejsce katalityczne.
Jak ATC12 wpływa na komórki nowotworowe i ich zachowanie
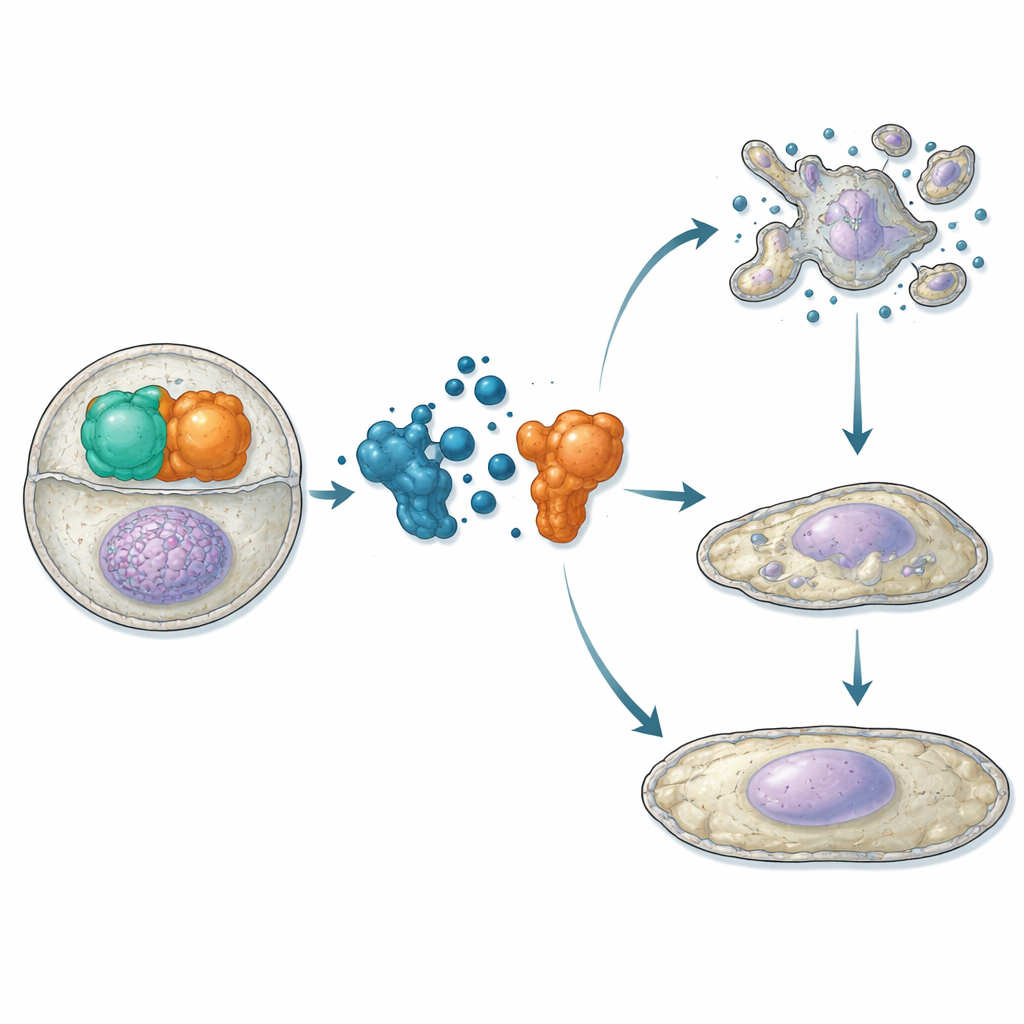
Po ustaleniu, że ATC12 wiąże Aurora-A i konkuruje z TPX2 in vitro, badacze przeszli do badań w żywych komórkach. W liniach osteosarcoma i raka piersi zastosowali testy bliskości i mikroskopię, aby pokazać, że leczenie ATC12 zmniejsza interakcję Aurora-A/TPX2 zarówno na wrzecionie podziałowym, jak i w jądrach komórek w interfazie, towarzyszy temu zmniejszenie sygnału Aurora-A w tych lokalizacjach. W dwóch modelach raka piersi — MCF7 (mniej agresywne, receptorowo dodatnie) i MDA-MB-231 (bardzo agresywne, potrójnie negatywne) — ATC12 obniżało przeżywalność komórek w sposób zależny od dawki, podczas gdy związek kontrolny, który nie zakłócał interakcji, nie miał efektu. Obrazowanie w czasie ujawniło, że w komórkach MCF7 ATC12 znacząco zmniejszał odsetek komórek wchodzących w mitoza, wydłużał czas trwania mitozy u tych, które się dzieliły, i prowadził do masowej śmierci komórek z biochemicznymi cechami apoptozy. Natomiast komórki MDA-MB-231 wykazywały spowolnioną proliferację bez istotnej śmierci; zamiast tego obserwowano podwyższone poziomy hamulca cyklu komórkowego p21, powiększone jądra i aktywację markerów starzenia, co wskazuje na przejście w trwały stan niepodziału.
Testy ATC12 w modelach 3D i organoidach pochodzenia pacjenta
Aby lepiej odtworzyć zachowanie guzów w organizmie, naukowcy przebadali ATC12 w hodowlach trójwymiarowych. Gdy komórki raka piersi były hodowane jako mammosfery — kuliste skupiska wzbogacające komórki o cechach podobnych do komórek macierzystych, opornych na terapię — ATC12 zmniejszał zarówno ich przeżywalność, jak i rozmiar w modelach MCF7 i MDA-MB-231, podczas gdy standardowy inhibitor kinazy Aurora-A nie powodował kurczenia się sfer. Zespół następnie przeszedł do organoidów hodowanych z biopsji potrójnie negatywnych raków piersi od pacjentów, których guzy były oporne na chemioterapię. W tych organoidach pochodzenia pacjenta ATC12 zmniejszał przeżycie komórek w wyraźnie zależny od dawki sposób, przy skutecznych stężeniach w niskim zakresie mikromolarnym. Powtórne podanie dawki leku w połowie terapii dodatkowo wzmocniło efekt, co sugeruje, że utrzymanie poziomów ATC12 w czasie może być ważne dla trwałego rozbicia kompleksu Aurora-A/TPX2.
Co to oznacza dla terapii przeciwnowotworowej
Praca ta wspiera koncepcję, że rozbijanie specyficznych partnerstw białkowych może być skuteczną drogą do unieszkodliwienia komórek nowotworowych, unikając jednocześnie niektórych pułapek tradycyjnych inhibitorów enzymów. Celując w kompleks Aurora-A/TPX2, ATC12 zakłóca zarówno komórki dzielące się, jak i niedzielące, prowokując albo śmierć komórki, albo stabilne starzenie w zależności od profilu genetycznego guza. Jego zdolność do ograniczania wzrostu w 3D mammosferach i w organoidach z trudnych do leczenia potrójnie negatywnych raków piersi podkreśla jego obiecujący potencjał jako punkt wyjścia do nowych leków, w tym do wyszlifowanych cząsteczek lub degraderów opartych na tej samej szkielecie chemicznym. Choć potrzebna jest dalsza optymalizacja w celu poprawy mocy i stabilności, badanie pokazuje, że selektywne rozdzielenie pary Aurora-A/TPX2 jest realistyczną i potencjalnie wartościową strategią dla przyszłych terapii przeciwnowotworowych.
Cytowanie: Boi, D., Fianco, G., Polverino, F. et al. The ATC12 small molecule inhibits the Aurora-A/TPX2 interaction and impairs the proliferation of breast cancer cells. Cell Death Dis 17, 356 (2026). https://doi.org/10.1038/s41419-026-08579-3
Słowa kluczowe: Aurora-A, TPX2, rak piersi, inhibitor interakcji białko–białko, organoidy