Clear Sky Science · ru
Малое молекула ATC12 ингибирует взаимодействие Aurora-A/TPX2 и нарушает пролиферацию клеток рака молочной железы
Почему это исследование важно для будущих методов лечения рака
Многие противораковые препараты пытаются отключить ферменты, управляющие делением клеток, но часто поражают слишком много мишеней и вызывают побочные эффекты или плохо действуют у пациентов. В этом исследовании рассматривается другой подход: вместо полного выключения фермента авторы стремятся разрушить специфическое взаимодействие между двумя белками, которые совместно способствуют росту и выживанию клеток рака молочной железы. Исследователи обнаружили и протестировали новую малую молеку — ATC12, которая мешает этому партнерству и замедляет рост раковых клеток, включая клетки, взятые непосредственно из опухолей пациентов.
Ключевое партнерство в делящихся клетках
Внутри наших клеток фермент Aurora-A помогает координировать деление клеток. Другой белок, TPX2, связывается с Aurora-A, помогает правильно позиционировать его на внутриклеточном каркасе и стабилизирует его. Вместе они образуют функциональную пару, уровни которой часто повышены в опухолях, включая рак молочной железы. Помимо роли в делении, Aurora-A может накапливаться в ядре неделящихся раковых клеток, где он усиливает активность генов, благоприятствующих росту и метастазированию опухоли. Есть свидетельства, что TPX2 также способствует доставке Aurora-A в ядро. Традиционные препараты, блокирующие активность Aurora-A конкурируя с ATP, показали ограниченный успех в клинических испытаниях, отчасти потому, что сайт связывания ATP похож у многих ферментов, что приводит к внецелевым эффектам. Это побудило исследователей искать более селективные способы подавления онкогенных ролей Aurora-A.

Проектирование молекулы для разрыва белкового контакта
Команда использовала компьютерный скрининг, чтобы просмотреть миллионы доступных для покупки молекул в поисках кандидатов, способных поместиться в контактную область, где TPX2 связывается с Aurora-A. Они сосредоточились на химических характеристиках, известных как важные для этого взаимодействия — гидрофобных карманах и ключевых «горячих точках» связывания. Из первоначально большой подборки они сузили список до 184 соединений, а затем до 15 лучших кандидатов, которые наилучшим образом соответствовали трехмерной форме и химии интерфейса. Лабораторные тесты с использованием нативной масс-спектрометрии показали, что четыре из этих молекул могут ослаблять связывание фрагмента TPX2 с Aurora-A. Дальнейшие эксперименты с зависимостью эффекта от дозы выявили два соединения, ATC7 и особенно ATC12, как наиболее активные в вытеснении TPX2 из Aurora-A без блокирования ферментативной активности Aurora-A, что указывает на специфическое влияние на взаимодействие, а не на каталитический сайт.
Как ATC12 влияет на раковые клетки и их поведение
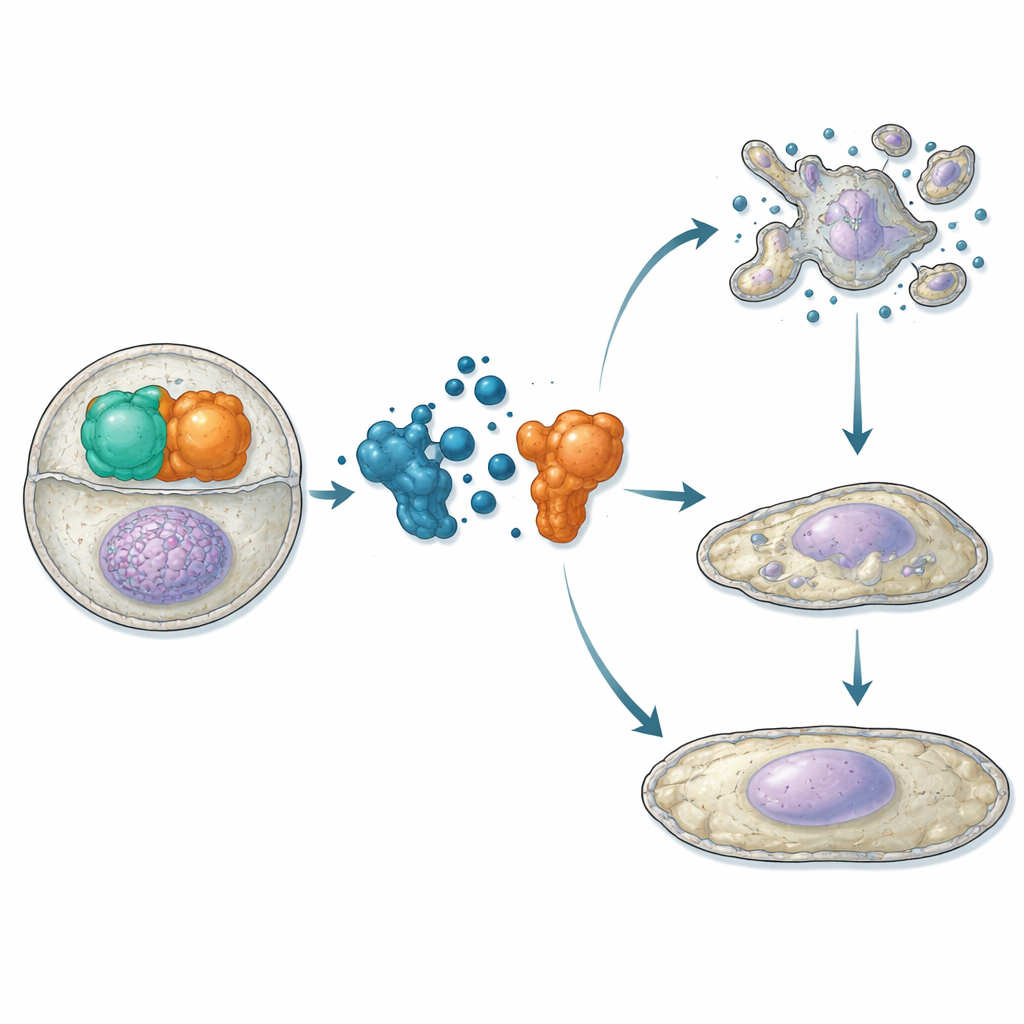
Установив, что ATC12 связывается с Aurora-A и конкурирует с TPX2 in vitro, исследователи перешли к живым клеткам. В линиях остеосаркомы и рака молочной железы с помощью тестов близости и микроскопии они показали, что лечение ATC12 уменьшает взаимодействие Aurora-A/TPX2 как на митотическом веретене, так и внутри ядер интерфазных клеток, сопровождаясь снижением сигнала Aurora-A в этих местах. В двух моделях рака молочной железы — MCF7 (менее агрессивная, гормонально-рецептор-положительная) и MDA-MB-231 (высокоагрессивная, тройной отрицательной) — ATC12 снизил жизнеспособность клеток в зависимости от дозы, тогда как контрольное соединение, не разрушающее взаимодействие, не оказывало эффекта. Временная съёмка показала, что в клетках MCF7 ATC12 значительно уменьшал долю клеток, входящих в митоз, удлинял продолжительность митоза у тех, кто всё же делился, и вызывал массовую гибель клеток с биохимическими признаками апоптоза. Напротив, в клетках MDA-MB-231 наблюдалось замедление пролиферации без значительной гибели; вместо этого повышались уровни тормоза клеточного цикла p21, ядра увеличивались, и активировались маркеры сенесценции, указывая на переход в стабильное состояние прекращения деления.
Тестирование ATC12 в 3D-моделях и органоидах, полученных от пациентов
Чтобы лучше имитировать поведение опухолей в организме, учёные исследовали ATC12 в трехмерных культурах. Когда клетки рака молочной железы выращивали в виде маммосфер — сферических кластеров, обогащённых стволоподобными, устойчивыми к терапии клетками — ATC12 уменьшал их жизнеспособность и размер как в линиях MCF7, так и в MDA-MB-231, тогда как стандартный ингибитор киназы Aurora-A не сокращал сферы. Команда затем перешла к органоидам, выращенным из биопсий пациентов с тройным отрицательным раком молочной железы, опухоли которых были резистентны к химиотерапии. В этих органоидах, полученных от пациентов, ATC12 снижал выживаемость клеток в явной зависимости от дозы, с эффективными концентрациями в низком микромолярном диапазоне. Повторное введение дозы препарата в середине лечения ещё больше усиливало эффект, что предполагает, что поддержание уровней ATC12 со временем может быть важным для длительного нарушения комплекса Aurora-A/TPX2.
Что это означает для терапии рака
Работа подтверждает идею, что разрыв специфических белковых партнерств может стать эффективным способом обезоружить раковые клетки, избегая некоторых недостатков традиционных ингибиторов ферментов. Нацеливаясь на комплекс Aurora-A/TPX2, ATC12 вмешивается как в делящиеся, так и в неделящиеся раковые клетки, вызывая либо гибель клеток, либо устойчивую сенесценцию в зависимости от генетического фона опухоли. Его способность подавлять рост в 3D-маммосферах и в органоидах из трудно лечимых тройных отрицательных раков молочной железы подчёркивает его перспективность в качестве исходной структуры для создания новых препаратов, включая усовершенствованные молекулы или деградаторы на той же основе. Хотя требуется дальнейшая оптимизация для повышения мощности и стабильности, исследование демонстрирует, что селективное разрушение пары Aurora-A/TPX2 — реалистичная и потенциально ценная стратегия для будущих противораковых терапий.
Цитирование: Boi, D., Fianco, G., Polverino, F. et al. The ATC12 small molecule inhibits the Aurora-A/TPX2 interaction and impairs the proliferation of breast cancer cells. Cell Death Dis 17, 356 (2026). https://doi.org/10.1038/s41419-026-08579-3
Ключевые слова: Aurora-A, TPX2, рак молочной железы, ингибитор белок–белкового взаимодействия, органоиды