Clear Sky Science · de
Das kleine Molekül ATC12 hemmt die Aurora-A/TPX2-Interaktion und schränkt die Proliferation von Brustkrebszellen ein
Warum diese Forschung für künftige Krebstherapien wichtig ist
Viele Krebsmedikamente versuchen, Enzyme auszuschalten, die die Zellteilung antreiben, treffen dabei aber häufig zu viele Ziele und verursachen Nebenwirkungen oder wirken in Patienten nur eingeschränkt. Diese Studie verfolgt einen anderen Ansatz: Anstatt ein Enzym komplett zu deaktivieren, zielt sie darauf ab, eine spezifische Partnerschaft zwischen zwei Proteinen zu stören, die gemeinsam das Wachstum und Überleben von Brustkrebszellen fördern. Die Forschenden identifizieren und testen ein neues kleines Molekül, ATC12 genannt, das diese Partnerschaft stört und das Wachstum von Krebszellen verlangsamt — einschließlich Zellen, die direkt aus Patienten-Tumoren entnommen wurden.
Eine zentrale Partnerschaft in teilenden Zellen
In unseren Zellen orchestriert ein Enzym namens Aurora-A die Zellteilung. Ein anderes Protein, TPX2, bindet an Aurora-A, hilft, es korrekt an das zelluläre Gerüst zu positionieren, und stabilisiert es. Gemeinsam bilden sie ein funktionales Paar, das in Tumoren, darunter Brustkrebserkrankungen, oft in erhöhten Mengen vorkommt. Über seine Rolle in der Zellteilung hinaus kann Aurora-A sich im Zellkern nicht teilender Krebszellen anreichern und Gene aktivieren, die Tumorwachstum und -ausbreitung fördern. Hinweise deuten darauf hin, dass TPX2 auch bei der Kernlokalisation von Aurora-A hilft. Konventionelle Wirkstoffe, die die Aktivität von Aurora-A durch Wettbewerb am ATP-Bindungsplatz blockieren, zeigten in klinischen Studien nur begrenzten Erfolg, teilweise weil die ATP-Bindungstasche in vielen Enzymen ähnlich ist und so Off-Target-Effekte entstehen. Das hat Forschende dazu veranlasst, selektivere Wege zu suchen, die krebsfördernden Funktionen von Aurora-A einzuschränken.

Ein Molekül entwerfen, das eine Proteinbindung aufbricht
Das Team nutzte computerbasierte Screening-Verfahren, um Millionen käuflicher Moleküle auf Kandidaten zu durchsuchen, die in die Kontaktregion passen könnten, in der TPX2 an Aurora-A bindet. Sie konzentrierten sich auf chemische Merkmale, die für diese Interaktion entscheidend sind, wie hydrophobe Taschen und wichtige Bindungs‑"Hotspots". Aus einem großen Anfangspool reduzierte sich die Auswahl auf 184 Verbindungen und schließlich auf 15 Spitzenkandidaten, die Form und Chemie der Schnittstelle am besten trafen. Laboruntersuchungen mittels nativer Massenspektrometrie zeigten, dass vier dieser Moleküle die Bindung eines TPX2-Fragments an Aurora-A abschwächen konnten. Weitere Dosis‑Antwort-Experimente identifizierten zwei Verbindungen, ATC7 und insbesondere ATC12, als die wirksamsten Kandidaten, die TPX2 von Aurora-A verdrängen, ohne die Enzymaktivität von Aurora-A zu blockieren — ein Hinweis auf einen spezifischen Effekt auf die Partnerschaft statt auf die katalytische Stelle.
Wie ATC12 Krebszellen und deren Verhalten beeinflusst
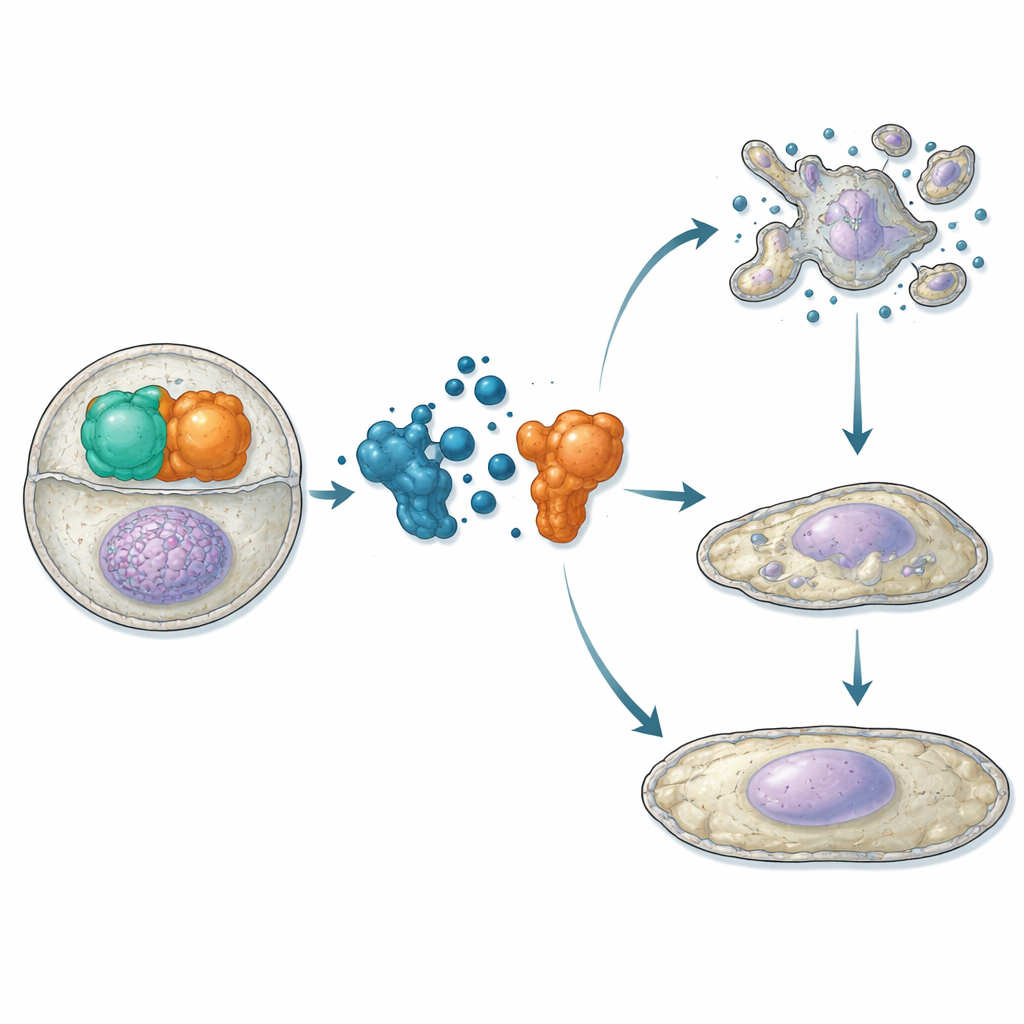
Nachdem gezeigt wurde, dass ATC12 an Aurora-A bindet und TPX2 in vitro konkurriert, gingen die Forschenden zu lebenden Zellen über. In Osteosarkom- und Brustkrebszelllinien verwendeten sie Proximity-Assays und Mikroskopie, um zu zeigen, dass ATC12-Behandlung die Aurora-A/TPX2-Interaktion sowohl im mitotischen Spindelapparat als auch in Interphase-Kernen reduziert, begleitet von einem verringerten Aurora-A-Signal an diesen Orten. In zwei Brustkrebsmodellen — MCF7 (weniger aggressiv, Hormonrezeptor-positiv) und MDA-MB-231 (hochaggressiv, triple-negativ) — senkte ATC12 die Zellviabilität dosisabhängig, während eine Kontrollverbindung, die die Interaktion nicht störte, keinen Effekt zeigte. Zeitrafferaufnahmen zeigten, dass ATC12 in MCF7-Zellen den Anteil der in die Mitose eintretenden Zellen stark verringerte, die Mitosedauer für die teilenden Zellen verlängerte und zu umfangreichem Zelltod mit biochemischen Merkmalen der Apoptose führte. Im Gegensatz dazu zeigten MDA-MB-231-Zellen verlangsamte Proliferation ohne signifikanten Zelltod; stattdessen stieg das Niveau des Zellzyklus-Inhibitors p21, die Zellkerne vergrößerten sich und Seneszenzmarker wurden aktiviert, was auf einen Übergang in einen stabilen, nicht mehr teilenden Zustand hinweist.
Prüfung von ATC12 in 3D-Modellen und patientenabgeleiteten Organoiden
Um das Tumorverhalten im Körper besser zu modellieren, untersuchten die Forschenden ATC12 in dreidimensionalen Kulturen. Wuchsen Brustkrebszellen als Mammosphären — kugelförmige Klümpchen, die für stammzellähnliche, therapieresistente Zellen anreichern — reduzierte ATC12 sowohl ihre Viabilität als auch ihre Größe in MCF7- und MDA-MB-231-Hintergründen, während ein standardmäßiger Aurora-A-Kinaseinhibitor die Sphären nicht verkleinerte. Das Team ging anschließend zu Organoiden über, die aus Biopsien von Patientinnen mit triple-negativem Brustkrebs gezüchtet wurden, deren Tumoren gegen Chemotherapie resistent gewesen waren. In diesen patientenabgeleiteten Organoiden verringerte ATC12 das Überleben der Zellen deutlich dosisabhängig, mit wirksamen Konzentrationen im niedrigen Mikromolarbereich. Eine wiederholte Verabreichung der Dosis während der Behandlung verstärkte den Effekt zusätzlich, was darauf hindeutet, dass die Aufrechterhaltung von ATC12‑Spiegeln über die Zeit wichtig für eine anhaltende Störung des Aurora-A/TPX2-Komplexes sein könnte.
Was das für die Krebstherapie bedeutet
Diese Arbeit stützt die Idee, dass das Aufbrechen spezifischer Proteinpartnerschaften ein wirkungsvoller Weg sein kann, Krebszellen zu entwaffnen und gleichzeitig einige Nachteile herkömmlicher Enzyminhibitoren zu vermeiden. Durch die gezielte Störung des Aurora-A/TPX2-Komplexes greift ATC12 sowohl teilende als auch nicht teilende Krebszellen an und löst, abhängig von der genetischen Ausstattung des Tumors, entweder Zelltod oder stabile Seneszenz aus. Die Fähigkeit, das Wachstum in 3D‑Mammosphären und in Organoiden schwer behandelbarer triple‑negativer Brustkrebse zu beeinträchtigen, unterstreicht sein Potenzial als Ausgangspunkt für neue Wirkstoffe, einschließlich verfeinerter Moleküle oder Degrader, die auf derselben Gerüststruktur basieren. Obwohl weitere Optimierungen notwendig sind, um Potenz und Stabilität zu verbessern, zeigt die Studie, dass die selektive Störung des Aurora‑A/TPX2‑Paares eine realistische und potenziell wertvolle Strategie für künftige krebsbekämpfende Therapien darstellt.
Zitation: Boi, D., Fianco, G., Polverino, F. et al. The ATC12 small molecule inhibits the Aurora-A/TPX2 interaction and impairs the proliferation of breast cancer cells. Cell Death Dis 17, 356 (2026). https://doi.org/10.1038/s41419-026-08579-3
Schlüsselwörter: Aurora-A, TPX2, Brustkrebs, Inhibitor der Protein–Protein-Interaktion, Organoide