Clear Sky Science · fr
La petite molécule ATC12 inhibe l’interaction Aurora‑A/TPX2 et gêne la prolifération des cellules du cancer du sein
Pourquoi cette recherche compte pour les traitements du cancer à venir
Beaucoup de médicaments anticancéreux cherchent à bloquer des enzymes qui pilotent la division cellulaire, mais ils touchent souvent trop de cibles et provoquent des effets secondaires, ou bien ils échouent à être efficaces chez les patients. Cette étude explore une autre tactique : au lieu d’éteindre une enzyme, elle vise à rompre un partenariat précis entre deux protéines qui coopèrent pour aider les cellules du cancer du sein à croître et à survivre. Les chercheurs découvrent et testent une nouvelle petite molécule, appelée ATC12, qui perturbe ce partenariat et ralentit la croissance des cellules cancéreuses, y compris des cellules prélevées directement dans des tumeurs de patients.
Un partenariat crucial dans les cellules en division
À l’intérieur de nos cellules, une enzyme nommée Aurora‑A aide à orchestrer la division cellulaire. Une autre protéine, TPX2, se lie à Aurora‑A, contribue à la positionner correctement sur l’échafaudage interne de la cellule et la stabilise. Ensemble, elles forment un duo fonctionnel souvent surexprimé dans les tumeurs, y compris les cancers du sein. Au‑delà de son rôle dans la division, Aurora‑A peut s’accumuler dans le noyau des cellules cancéreuses non en division, où elle stimule des gènes favorisant la croissance et la diffusion tumorales. Des preuves suggèrent que TPX2 aide aussi Aurora‑A à atteindre le noyau. Les médicaments traditionnels qui bloquent l’activité d’Aurora‑A en compétition avec l’ATP ont montré un succès limité en essais cliniques, en partie parce que le site de liaison à l’ATP ressemble à celui de nombreuses autres enzymes, entraînant des effets hors cible. Cela a poussé les chercheurs à chercher des moyens plus sélectifs de freiner les rôles favorisants le cancer d’Aurora‑A.

Concevoir une molécule pour rompre une liaison protéique
L’équipe a utilisé le criblage assisté par ordinateur pour parcourir des millions de molécules commercialement disponibles à la recherche de candidates susceptibles de se loger dans la zone de contact où TPX2 se lie à Aurora‑A. Ils se sont concentrés sur des caractéristiques chimiques connues comme cruciales pour cette interaction, telles que des poches hydrophobes et des « points chauds » de liaison. À partir d’un large ensemble initial, ils ont réduit la sélection à 184 composés, puis à 15 candidats principaux correspondant le mieux à la forme tridimensionnelle et à la chimie de l’interface. Des tests en laboratoire par spectrométrie de masse native ont montré que quatre de ces molécules pouvaient affaiblir la liaison d’un fragment de TPX2 à Aurora‑A. Des expériences dose‑réponse ont ensuite identifié deux composés, ATC7 et surtout ATC12, comme les plus puissants pour déplacer TPX2 d’Aurora‑A sans bloquer l’activité enzymatique d’Aurora‑A, indiquant un effet spécifique sur le partenariat plutôt que sur le site catalytique.
Comment ATC12 affecte les cellules cancéreuses et leur comportement
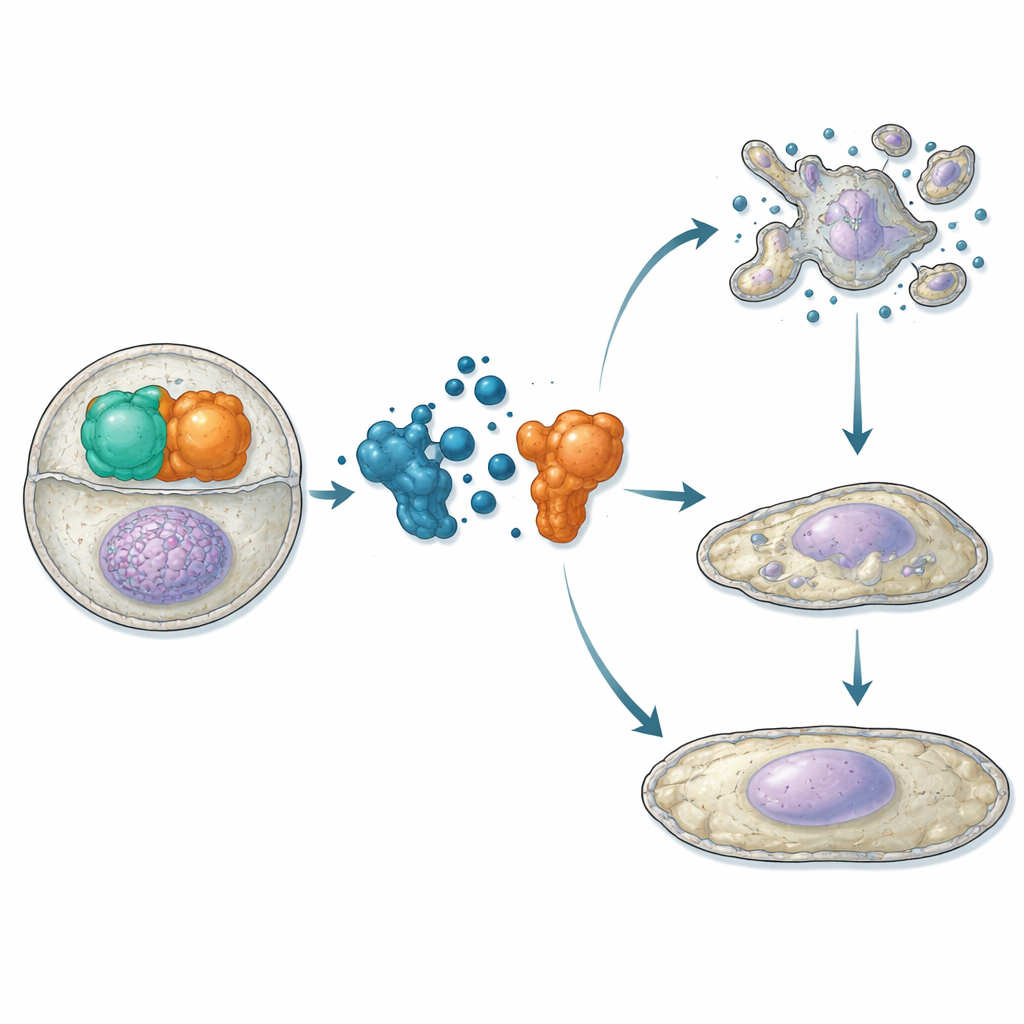
Ayant établi qu’ATC12 se lie à Aurora‑A et rivalise avec TPX2 in vitro, les chercheurs sont passés aux cellules vivantes. Dans des lignées d’ostéosarcome et de cancer du sein, ils ont utilisé des tests de proximité et la microscopie pour montrer que le traitement par ATC12 réduit l’interaction Aurora‑A/TPX2 tant au niveau du fuseau mitotique que dans les noyaux en interfase, accompagné d’une diminution du signal Aurora‑A à ces endroits. Dans deux modèles de cancer du sein — MCF7 (moins agressif, récepteur hormonal positif) et MDA‑MB‑231 (très agressif, triple négatif) — ATC12 a réduit la viabilité cellulaire de façon dépendante de la dose, tandis qu’un composé témoin ne perturbant pas l’interaction n’avait aucun effet. L’imagerie en continu a révélé que dans les cellules MCF7, ATC12 réduisait fortement la fraction de cellules entrant en mitose, prolongeait la durée de la mitose pour celles qui se divisaient et entraînait une mort cellulaire étendue avec des signes biochimiques d’apoptose. En revanche, les cellules MDA‑MB‑231 montraient un ralentissement de la prolifération sans mortalité significative ; elles présentaient plutôt une augmentation du frein du cycle cellulaire p21, des noyaux agrandis et l’activation de marqueurs de sénescence, indiquant une bascule vers un état permanent de non‑division.
Tester ATC12 dans des modèles 3D et des organoïdes dérivés de patients
Pour mieux imiter le comportement des tumeurs in vivo, les scientifiques ont examiné ATC12 dans des cultures tridimensionnelles. Lorsque des cellules de cancer du sein étaient cultivées en mammosphères — amas sphériques enrichis en cellules de type souches, résistantes aux thérapies — ATC12 a réduit à la fois leur viabilité et leur taille, en contextes MCF7 et MDA‑MB‑231, alors qu’un inhibiteur classique de la kinase Aurora‑A n’a pas réduit les sphères. L’équipe est ensuite passée à des organoïdes cultivés à partir de biopsies de patientes atteintes de cancers du sein triple négatifs dont les tumeurs avaient résisté à la chimiothérapie. Dans ces organoïdes dérivés de patients, ATC12 a diminué la survie cellulaire de façon nette et dépendante de la dose, avec des concentrations efficaces dans la plage micromolaire basse. Répéter l’administration du médicament en cours de traitement a encore renforcé l’effet, suggérant que le maintien des niveaux d’ATC12 dans le temps pourrait être important pour une perturbation soutenue du complexe Aurora‑A/TPX2.
Ce que cela signifie pour la thérapie anticancéreuse
Ce travail étaye l’idée que rompre des partenariats protéiques spécifiques peut être une façon puissante de désarmer les cellules cancéreuses tout en évitant certains écueils des inhibiteurs enzymatiques traditionnels. En ciblant le complexe Aurora‑A/TPX2, ATC12 perturbe à la fois les cellules cancéreuses en division et hors division, provoquant soit la mort cellulaire soit une sénescence stable selon le profil génétique de la tumeur. Sa capacité à gêner la croissance dans des mammosphères 3D et dans des organoïdes issus de cancers du sein triple négatifs difficiles à traiter souligne son potentiel comme point de départ pour de nouveaux médicaments, y compris des molécules affinées ou des agents dégradants basés sur le même échafaudage. Bien que des optimisations supplémentaires soient nécessaires pour améliorer la puissance et la stabilité, l’étude démontre que perturber sélectivement la paire Aurora‑A/TPX2 est une stratégie réaliste et potentiellement précieuse pour les traitements anticancéreux futurs.
Citation: Boi, D., Fianco, G., Polverino, F. et al. The ATC12 small molecule inhibits the Aurora-A/TPX2 interaction and impairs the proliferation of breast cancer cells. Cell Death Dis 17, 356 (2026). https://doi.org/10.1038/s41419-026-08579-3
Mots-clés: Aurora‑A, TPX2, cancer du sein, inhibiteur d’interaction protéine–protéine, organoïdes