Clear Sky Science · ja
ATC12という低分子はAurora-A/TPX2相互作用を阻害し、乳がん細胞の増殖を損なう
この研究が将来のがん治療にとって重要な理由
多くの抗がん薬は細胞分裂を促す酵素を停止させようとしますが、標的が多岐にわたって副作用が出たり、患者で十分に効果を示さないことがしばしばあります。本研究は別の戦略を探ります。酵素を直接オフにするのではなく、乳がん細胞の増殖と生存を助ける二つのタンパク質の特定の結びつきを壊すことを目指します。研究者たちはATC12と名付けた新しい低分子を発見・検証し、この結合を妨げることで癌細胞の増殖を遅らせ、患者腫瘍由来の細胞を含むモデルで効果を示しました。
分裂する細胞内の重要なパートナーシップ
細胞内では、Aurora-Aという酵素が細胞分裂の調整を担います。別のタンパク質TPX2はAurora-Aに結合して細胞内部の足場上に正しく位置づけ、安定化させます。二者は協調して機能し、乳がんを含む腫瘍でしばしば過剰発現します。分裂していないがん細胞ではAurora-Aが核内に蓄積し、腫瘍増殖や転移を促す遺伝子を活性化することが知られていますが、TPX2がAurora-Aの核内移行を助ける証拠もあります。従来のATP競合的なAurora-A阻害薬は、多くの酵素でATP結合部位が類似しているためオフターゲットを招き、臨床での成功が限定的でした。このため、Aurora-Aのがん促進作用をより選択的に抑える手段が模索されています。

タンパク質結合を壊す分子の設計
研究チームはコンピュータによるスクリーニングを用いて、TPX2がAurora-Aに結合する接触領域にフィットする市販可能な分子を何百万と検索しました。疎水性ポケットや重要な「ホットスポット」といった相互作用に必須と考えられる化学的特徴に注目しました。初期の大規模候補群から184化合物に絞り込み、さらに立体形状と界面の化学に最も合致する15のトップ候補を選定しました。ネイティブ質量分析による実験で、これらのうち4分子がTPX2断片のAurora-Aへの結合を弱めることが示されました。用量反応実験の結果、ATC7と特にATC12の二つが、Aurora-Aの酵素活性を阻害することなくTPX2を置換する点で最も有効であり、触媒部位ではなくパートナーシップ特異的な作用であることが示唆されました。
ATC12ががん細胞とその挙動に及ぼす影響
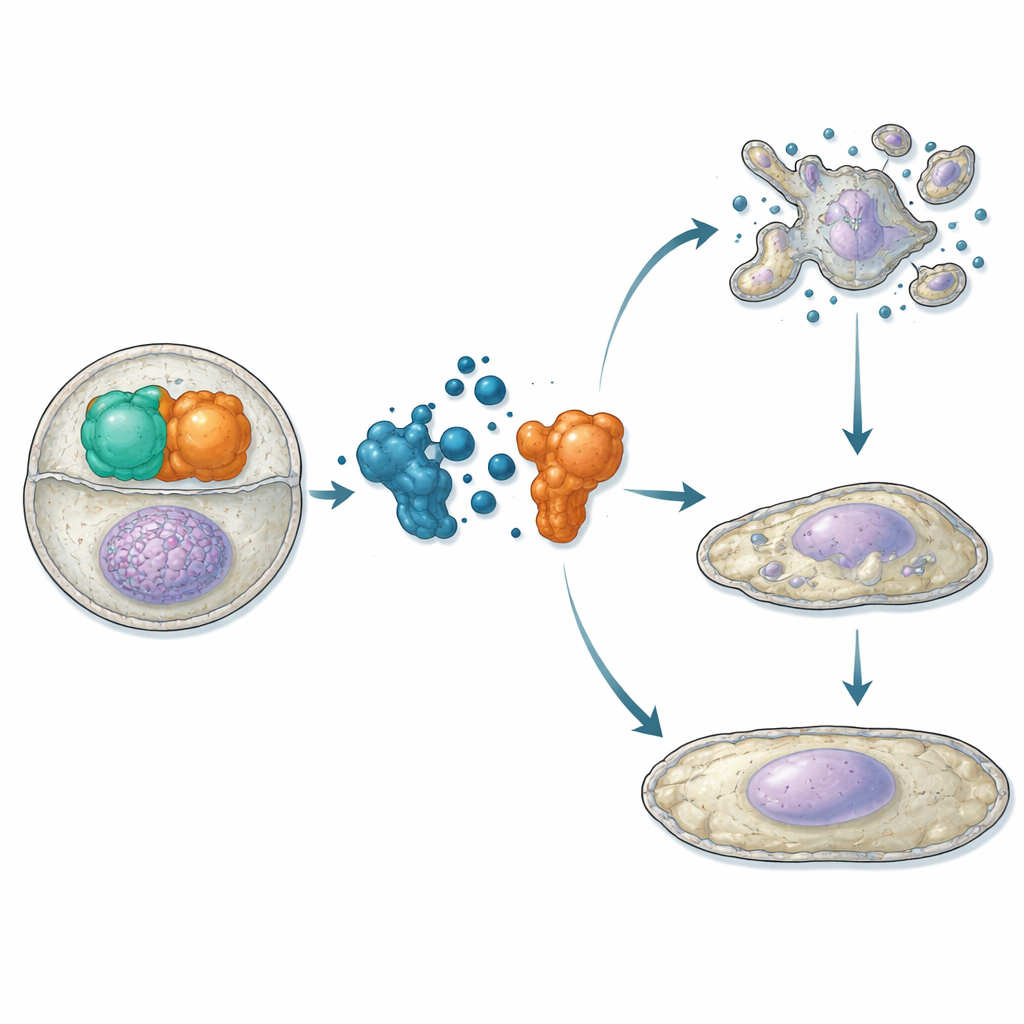
ATC12がAurora-Aに結合しin vitroでTPX2と競合することを示した後、研究者たちは生細胞で検証を進めました。骨肉腫および乳がん細胞株で近接アッセイと顕微鏡観察を用いると、ATC12処理により、有糸分裂紡錘体および間期の核内でのAurora-A/TPX2相互作用が減少し、これらの局在でのAurora-Aシグナルも低下しました。二つの乳がんモデル(MCF7:低侵襲でホルモン受容体陽性、MDA-MB-231:高悪性度でトリプルネガティブ)では、ATC12は用量依存的に細胞生存率を低下させ、相互作用を妨げない対照化合物では影響がありませんでした。タイムラプスイメージングでは、MCF7細胞でATC12は有糸分裂に入る細胞の割合を大幅に減らし、有糸分裂を行った細胞ではその継続時間を延長し、アポトーシスの生化学的兆候を伴う広範な細胞死をもたらしました。一方、MDA-MB-231細胞では著しい死滅は見られず増殖が緩やかになり、細胞周期抑制因子p21の増加、核の肥大、老化マーカーの活性化を示し、恒常的な非分裂状態への移行が示唆されました。
3Dモデルと患者由来オルガノイドでのATC12の評価
腫瘍の体内挙動をより再現するため、研究者らは三次元培養でATC12を評価しました。乳がん細胞をマモスフィア(幹様で治療抵抗性の細胞を濃縮する球状クラスター)として培養した場合、ATC12はMCF7およびMDA-MB-231両背景で生存率とサイズを低下させ、標準的なAurora-Aキナーゼ阻害剤では球の縮小は観察されませんでした。次に、化学療法に抵抗したトリプルネガティブ乳がん患者の生検から作製したオルガノイドでもATC12は用量依存的に細胞生存を低下させ、効果的濃度は低マイクロモル領域でした。治療途中で薬剤量を再投与すると効果が増強され、ATC12濃度を持続させることがAurora-A/TPX2複合体の長期的な破壊に重要である可能性を示唆します。
がん治療への示唆
本研究は、特定のタンパク質間パートナーシップを切断することが、従来の酵素阻害剤の欠点を回避しつつがん細胞を無力化する有力な手段になりうることを支持します。Aurora-A/TPX2複合体を標的とするATC12は、分裂中の細胞と分裂していない細胞の双方に干渉し、腫瘍の遺伝的背景により細胞死または安定した老化を誘導します。3Dマモスフィアや治療困難なトリプルネガティブ乳がん由来オルガノイドで増殖を阻害したことは、同骨格を基にした改良分子や分解誘導体など新薬開発の出発点としての有望性を示します。効力や安定性の向上にはさらなる最適化が必要ですが、Aurora-A/TPX2ペアを選択的に破壊する戦略は現実的で有望な抗がんアプローチであることを本研究は示しています。
引用: Boi, D., Fianco, G., Polverino, F. et al. The ATC12 small molecule inhibits the Aurora-A/TPX2 interaction and impairs the proliferation of breast cancer cells. Cell Death Dis 17, 356 (2026). https://doi.org/10.1038/s41419-026-08579-3
キーワード: Aurora-A, TPX2, 乳がん, タンパク質間相互作用阻害剤, オルガノイド