Clear Sky Science · he
המולקולה הקטנה ATC12 מעכבת את האינטראקציה בין Aurora‑A ל‑TPX2 ומפחיתה את התרבות תאי סרטן השד
מדוע מחקר זה חשוב לטיפולים עתידיים בסרטן
תרופות רבות נגד סרטן מנסות להשבית אנזימים המניעים חלוקת תאים, אך הן לרוב פוגעות ביותר מדי מטרות וגורמות לתופעות לוואי, או שאינן יעילות בצורה מספקת בחולים. מחקר זה בוחן טקטיקה שונה: במקום לכבות אנזים, הוא שואף לפגוע בשותפות מסוימת בין שני חלבונים שעובדים יחד כדי לסייע לתאי סרטן השד לגדול ולהישרדות. החוקרים מגלים ובודקים מולקולה קטנה חדשה, שכותרתה ATC12, שמפריעה לשותפות זו ומאטה את גדילת תאי הסרטן, כולל תאים שנלקחו ישירות מגידולים של מטופלים.
שותפות מכרעת בתוך תאים מתחלקים
במקרים שלנו, אנזים בשם Aurora‑A מסייע לתזמר את חלוקת התאים. חלבון אחר, TPX2, נקשר ל‑Aurora‑A, ממקם אותו נכון על השלד התאי ומייצב אותו. יחד הם יוצרים זוג פונקציונלי שנמצא לעתים ברמות לא תקינות בגידולים, כולל בסרטן השד. מעבר לתפקידו בחלוקה, Aurora‑A יכול להצטבר בגרעין של תאים סרטניים שאינם מתחלקים, שם הוא מעודד גנים התומכים בצמיחת הגידול ובהתפשטותו. יש עדויות ש‑TPX2 מסייע גם בהעברת Aurora‑A לגרעין. תרופות מסורתיות החוסמות את פעילות Aurora‑A על ידי תחרות עם ATP הראו הצלחה מוגבלת בניסויים קליניים, בחלקה מכיוון שאתר הקישור ל‑ATP דומה בהרבה אנזימים, מה שמוביל להשפעות לא ממוקדות. זה דחף את החוקרים לחפש דרכים סלקטיביות יותר להמעיט בתפקידיו המקדמים סרטן של Aurora‑A.

עיצוב מולקולה לשבירת קשר חלבוני
הצוות השתמש בסריקה ממוחשבת כדי לחפש בין מיליוני מולקולות מסחריות מועמדים שיכולים להתאים לאזור המגע שבו TPX2 נקשר ל‑Aurora‑A. הם התרכזו בתכונות כימיות הידועות כחשובות לאינטראקציה זו, כגון כיסים הידרופוביים ו"נקודות חמות" לקישור. מתוך מאגר ראשוני גדול הם צמצמו ל‑184 תרכובות, ולאחר מכן ל‑15 מועמדות מובילות שהשתוו בצורה ותכונות כימיות לתצורת הממשק התלת‑ממדית. בדיקות מעבדה בעזרת ספקטרומטריית מסה של חומרים טבעיים הראו כי ארבעה מן המולקולות יכולות להחליש את קשירת מקטע של TPX2 ל‑Aurora‑A. ניסויי מנה‑תשובה נוספים זיהו שתי תרכובות, ATC7 ובייחוד ATC12, כעוצמתיות ביותר בהדחת TPX2 מ‑Aurora‑A מבלי לחסום את פעילות האנזים של Aurora‑A, מה שמעיד על השפעה ממוקדת על השותפות ולא על אתר הקטליזה.
כיצד ATC12 משפיעה על תאי סרטן והתנהגותם
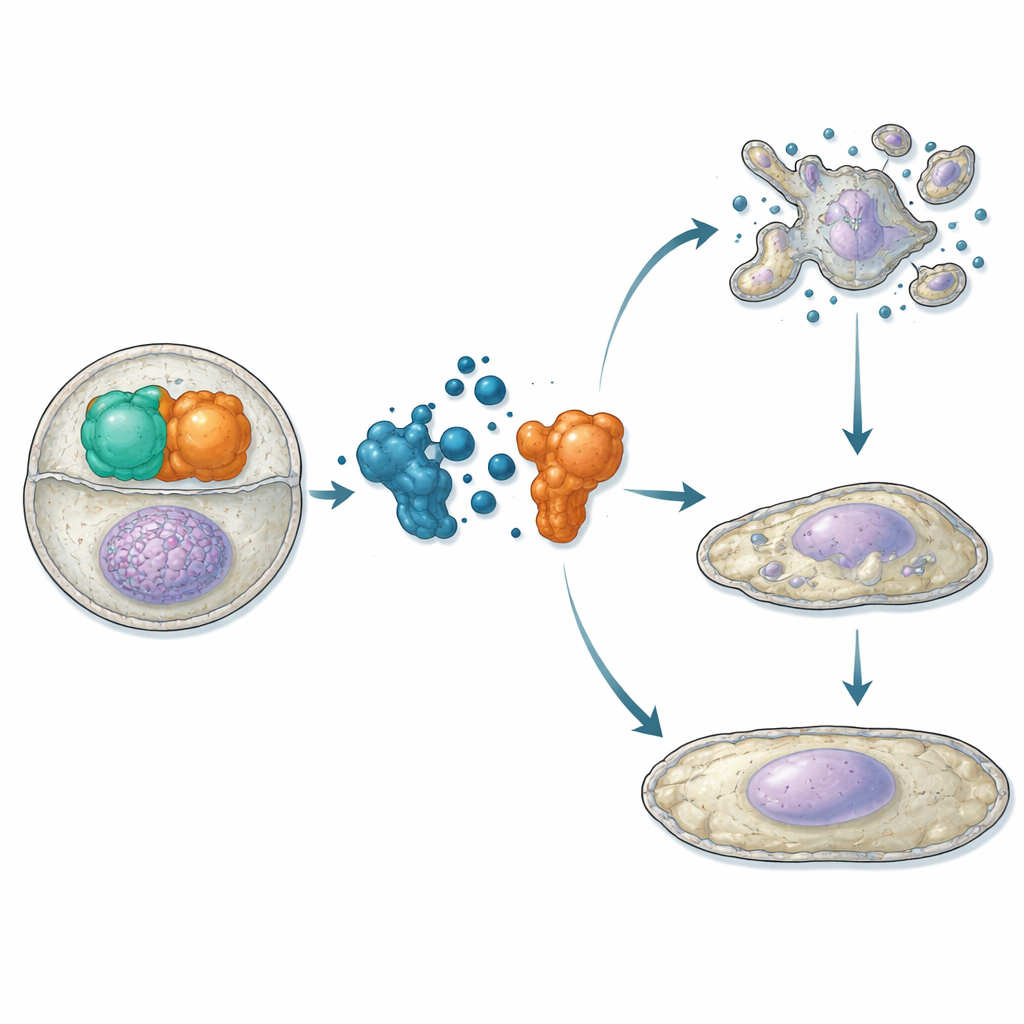
לאחר שקבעו ש‑ATC12 נקשרת ל‑Aurora‑A ומתחרה ב‑TPX2 מבחינה מבחנתית, החוקרים עברו לתאים חיים. בקווי תאים של אוסטאוסרקומה וסרטן השד השתמשו בבדיקות קרבה ומיקרוסקופיה כדי להראות שטיפול ב‑ATC12 מקטין את האינטראקציה בין Aurora‑A ל‑TPX2 הן על שׂן המיטוטי והן בתוך גרעיני אינטרפזה, ולצד זאת אות Aurora‑A באזורים אלה פחת. בשני מודלים של סרטן השד — MCF7 (פחות אגרסיבי, חיובי לקולטנים הורמונליים) ו‑MDA‑MB‑231 (אגרסיבי מאוד, שלילי לשלוש הקבוצות) — ATC12 הוריד את כמות התאים בשיעור תלוי מינון, בעוד שתרכובת בקרה שלא הפרה את האינטראקציה לא הראתה אפקט. הדמיות בזמן אמת הראו שבתאי MCF7 ATC12 הקטין מאוד את השיעור של תאים הנכנסים למיטוזה, האריך את משך המיטוזה אצל אלה שחילקו, והוביל לתמותה תאית נרחבת עם סימנים ביוכימיים לאפופטוזיס. בניגוד לכך, תאי MDA‑MB‑231 הציגו האטה בהתרבות מבלי תמותה משמעותית; במקום זאת נצפו רמות מוגברות של מעצור מחזור התא p21, גרעינים מוגדלים והפעלה של סמני זקנה, מה שמעיד על מעבר למצב של אי‑תחלוקה קבועה.
בדיקת ATC12 במודלים תלת‑ממדיים ואורגנוידים שמקורם בחולים
כדי לדמות טוב יותר את התנהגות הגידול בגוף, הבדקו החוקרים את ATC12 בתרביות תלת־ממדיות. כאשר תאי סרטן השד גודלו כממוספרות — צברים סגלגלים שמעשירים לתאים דמויי‑גזע ולעמידים לטיפול — ATC12 הקטין הן את הכמות והן את גודל הכדורים בשתי הרקעים של MCF7 ו‑MDA‑MB‑231, בעוד שמעכב קינאז סטנדרטי של Aurora‑A לא הקטין את הכדורים. הצוות עבר לאחר מכן לאורגנוידים שגודלו ממקורות ביופסיה של חולות עם סרטן שד טרבל‑נגטיב שעמד בכישלון לכימותרפיה. באורגנוידים שמקורם בחולים אלה, ATC12 הוריד את הישרדות התאים באופן תלוי מינון, בריכוזים אפקטיביים בטווח המיקרומולרי הנמוך. חזרה על מתן המנה באמצע הטיפול שיפרה עוד את האפקט, מה שמרמז ששימור רמות ATC12 לאורך זמן עשוי להיות חשוב להפרעה מתמשכת במורכבות Aurora‑A/TPX2.
מה המשמעות לטיפול בסרטן
עבודה זו תומכת ברעיון ששבירת שותפויות חלבוניות ספציפיות יכולה להיות דרך חזקה לנטרל תאים סרטניים תוך הימנעות מחלק מהמגבלות של מעכבי אנזים מסורתיים. על ידי מיקוד במורכבות Aurora‑A/TPX2, ATC12 מתערבת הן בתאים מתחלקים והן בתאים שאינם מתחלקים, ומעוררת או מוות תאי או זקנה יציבה בהתאם להרכב הגנטי של הגידול. יכולתה לפגוע בצמיחה בכדורי‑ממוספרות תלת‑ממדיים ובאורגנוידים ממקרי טרבל‑נגטיב קשים לטיפול מדגישה את הפוטנציאל שלה כנקודת פתיחה לתרופות חדשות, כולל מולקולות משופרות או מפורקות (degraders) המבוססות על אותו שלד. אף שדרושות אופטימיזציות נוספות לשיפור העוצמה והיציבות, המחקר מדגים כי הפרעה סלקטיבית בזוג Aurora‑A/TPX2 היא אסטרטגיה מציאותית ובעלת ערך פוטנציאלי לטיפולים עתידיים נגד סרטן.
ציטוט: Boi, D., Fianco, G., Polverino, F. et al. The ATC12 small molecule inhibits the Aurora-A/TPX2 interaction and impairs the proliferation of breast cancer cells. Cell Death Dis 17, 356 (2026). https://doi.org/10.1038/s41419-026-08579-3
מילות מפתח: Aurora‑A, TPX2, סרטן השד, מעכב אינטראקציות חלבון–חלבון, אורגנוידים