Clear Sky Science · it
La piccola molecola ATC12 inibisce l’interazione Aurora-A/TPX2 e compromette la proliferazione delle cellule del cancro al seno
Perché questa ricerca conta per i futuri trattamenti contro il cancro
Molti farmaci antitumorali cercano di bloccare enzimi che guidano la divisione cellulare, ma spesso colpiscono troppi bersagli causando effetti collaterali, o non funzionano bene nei pazienti. Questo studio esplora una strategia diversa: invece di spegnere un enzima, mira a rompere una partnership specifica tra due proteine che cooperano per favorire la crescita e la sopravvivenza delle cellule del cancro al seno. I ricercatori scoprono e testano una nuova piccola molecola, chiamata ATC12, che interferisce con questa collaborazione e rallenta la crescita delle cellule tumorali, incluse cellule prelevate direttamente dai tumori dei pazienti.
Una partnership cruciale all’interno delle cellule in divisione
All’interno delle nostre cellule, un enzima chiamato Aurora-A aiuta a orchestrare la divisione cellulare. Un’altra proteina, TPX2, si lega ad Aurora-A, ne facilita il corretto posizionamento sullo scheletro interno della cellula e ne stabilizza la forma. Insieme formano una coppia funzionale che spesso è presente a livelli anormalmente elevati nei tumori, incluso il cancro al seno. Oltre al ruolo nella divisione cellulare, Aurora-A può accumularsi nel nucleo di cellule tumorali non in divisione, dove aumenta l’espressione di geni che favoriscono la crescita e la diffusione tumorale. Evidenze suggeriscono che anche TPX2 aiuti Aurora-A a raggiungere il nucleo. I farmaci tradizionali che bloccano l’attività di Aurora-A competendo con l’ATP hanno mostrato successo limitato negli studi clinici, in parte perché il sito di legame per l’ATP è simile in molti enzimi, causando effetti off-target. Questo ha spinto i ricercatori a cercare modi più selettivi per frenare i ruoli pro-tumorali di Aurora-A.

Progettare una molecola per rompere un legame proteico
Il gruppo ha utilizzato screening basati su computer per cercare milioni di molecole acquistabili che potessero adattarsi alla regione di contatto dove TPX2 si lega ad Aurora-A. Si sono concentrati su caratteristiche chimiche note per essere cruciali in questa interazione, come tasche idrofobiche e “hot spot” chiave di legame. Da una grande popolazione iniziale hanno ristretto il campo a 184 composti, e poi a 15 candidati principali che meglio si adattavano alla forma tridimensionale e alla chimica dell’interfaccia. Test di laboratorio mediante spettrometria di massa nativa hanno mostrato che quattro di queste molecole potevano indebolire il legame di un frammento di TPX2 con Aurora-A. Ulteriori esperimenti dose–risposta hanno identificato due composti, ATC7 e in particolare ATC12, come i più potenti nello spiazzare TPX2 da Aurora-A senza bloccare l’attività enzimatica di Aurora-A, indicando un effetto specifico sulla partnership piuttosto che sul sito catalitico.
Come ATC12 influenza le cellule tumorali e il loro comportamento
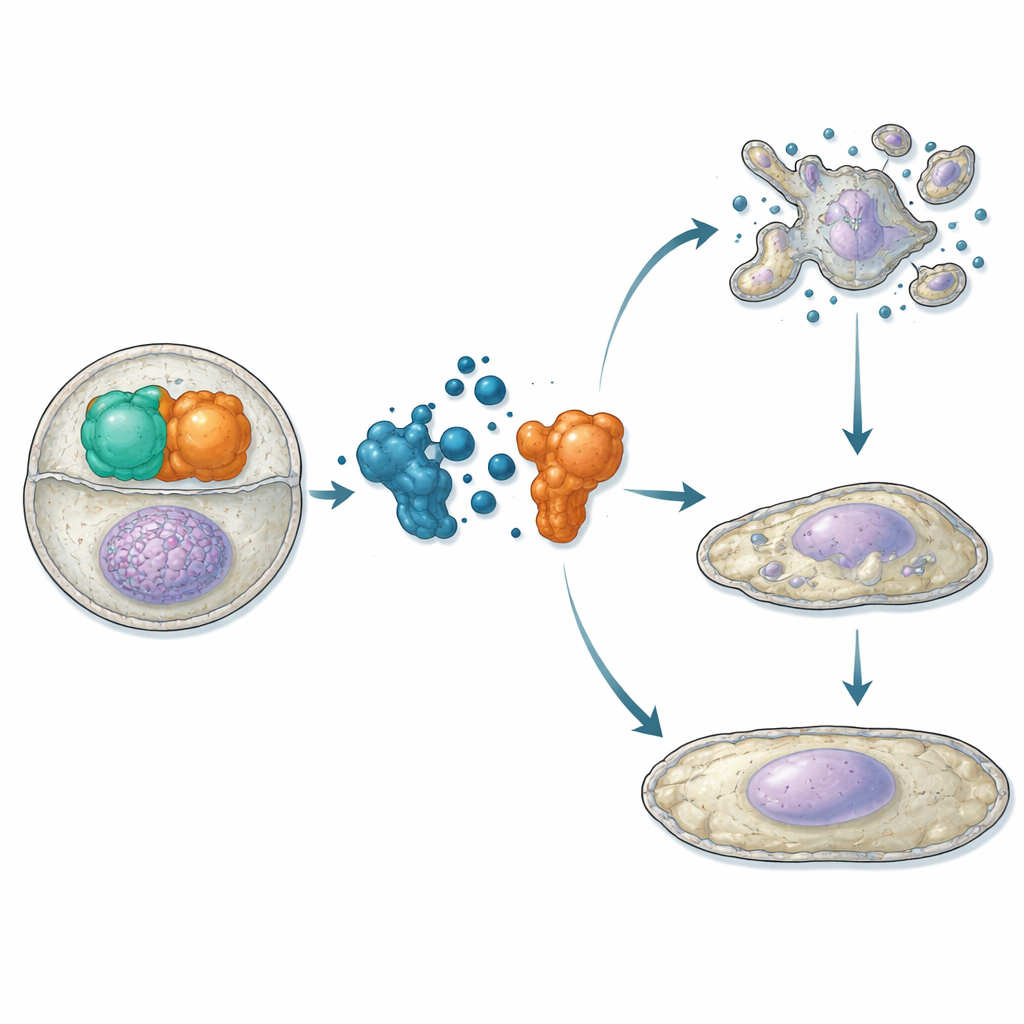
Dopo aver stabilito che ATC12 si lega ad Aurora-A e compete con TPX2 in vitro, i ricercatori sono passati alle cellule vive. In linee cellulari di osteosarcoma e carcinoma mammario, hanno usato saggi di prossimità e microscopia per mostrare che il trattamento con ATC12 riduce l’interazione Aurora-A/TPX2 sia sul fuso mitotico sia nei nuclei in interfase, accompagnato da un segnale di Aurora-A diminuito in queste sedi. In due modelli di cancro al seno—MCF7 (meno aggressivo, positivo per recettori ormonali) e MDA-MB-231 (altamente aggressivo, triplo-negativo)—ATC12 ha ridotto la vitalità cellulare in modo dose-dipendente, mentre un composto di controllo che non interrompeva l’interazione non ha avuto effetto. Immagini time-lapse hanno rivelato che nelle cellule MCF7 ATC12 ha ridotto fortemente la frazione di cellule che entrano in mitosi, ha prolungato la durata della mitosi per quelle che si dividevano e ha portato a un’estesa morte cellulare con segnali biochimici di apoptosi. Al contrario, le cellule MDA-MB-231 hanno mostrato una proliferazione rallentata senza morte significativa; hanno infatti mostrato un aumento dei livelli del freno del ciclo cellulare p21, nuclei ingranditi e attivazione di marcatori di senescenza, indicando un passaggio a uno stato non divisorio permanente.
Testare ATC12 in modelli 3D e organoidi derivati da pazienti
Per mimare meglio il comportamento dei tumori in vivo, gli scienziati hanno esaminato ATC12 in colture tridimensionali. Quando le cellule del cancro al seno sono state coltivate come mammosfere—aggregate sferiche che arricchiscono cellule con caratteristiche staminali e resistenti alle terapie—ATC12 ha ridotto sia la loro vitalità sia le dimensioni in entrambi i contesti MCF7 e MDA-MB-231, mentre un inibitore standard della chinasi Aurora-A non ha ridotto le sfere. Il gruppo ha poi testato organoidi coltivati da biopsie di pazienti con carcinoma mammario triplo-negativo i cui tumori avevano resistito alla chemioterapia. In questi organoidi derivati da pazienti, ATC12 ha diminuito la sopravvivenza cellulare in modo chiaramente dose-dipendente, con concentrazioni efficaci nell’ordine dei micromolari bassi. Ripetere la somministrazione del farmaco a metà trattamento ha ulteriormente potenziato l’effetto, suggerendo che mantenere livelli di ATC12 nel tempo può essere importante per una distruzione sostenuta del complesso Aurora-A/TPX2.
Cosa significa per la terapia del cancro
Questo lavoro supporta l’idea che rompere partnership proteiche specifiche possa essere un modo potente per disarmare le cellule tumorali evitando alcuni limiti degli inibitori enzimatici tradizionali. Mirando al complesso Aurora-A/TPX2, ATC12 interferisce sia con le cellule tumorali in divisione sia con quelle non in divisione, provocando o morte cellulare o senescenza stabile a seconda del profilo genetico del tumore. La sua capacità di compromettere la crescita in mammosfere 3D e in organoidi provenienti da tumori triplo-negativi difficili da trattare ne sottolinea il potenziale come punto di partenza per nuovi farmaci, compresi molecole ottimizzate o degradatori basati sullo stesso scaffold. Sebbene sia necessario ulteriore lavoro di ottimizzazione per migliorare potenza e stabilità, lo studio dimostra che interrompere selettivamente la coppia Aurora-A/TPX2 è una strategia realistica e potenzialmente preziosa per futuri trattamenti anticancro.
Citazione: Boi, D., Fianco, G., Polverino, F. et al. The ATC12 small molecule inhibits the Aurora-A/TPX2 interaction and impairs the proliferation of breast cancer cells. Cell Death Dis 17, 356 (2026). https://doi.org/10.1038/s41419-026-08579-3
Parole chiave: Aurora-A, TPX2, cancro al seno, inibitore dell’interazione proteina–proteina, organoidi