Clear Sky Science · tr
Apoptoz ve senesansla ilişkili tümörleşmenin indüksiyonunda Drosophila p53 izoformlarının transkripsiyona bağımlı ve bağımsız işlevleri
Bu çalışma neden önemli
Hücrelerimiz sürekli olarak güneş ışığı, kimyasallar ve normal aşınma-yıpranma nedeniyle hasara maruz kalır. p53 adlı bir protein, hasarlı bir hücrenin kendini onarıp onaramayacağına, bölünmeyi durdurup durdurmayacağına veya ölmeye karar verip vermeyeceğine hükmetmesiyle ünlüdür. p53 bozulduğunda kanserler sıklıkla ortaya çıkar. Bu çalışma, meyve sineği Drosophila’yı kullanarak p53’ün farklı versiyonlarının hücreleri güvenli kendi kendini yok etmeye mi yoksa tehlikeli, tümörü teşvik edici bir duruma mı ittiğini ayırıyor. Sinek ve insan p53’ü şaşırtıcı derecede benzer olduğu için bu bulgular, hasara verilen bazı hücresel yanıtların kanseri nasıl önlediğini, bazı yanıtların ise neden sessizce onu besleyebileceğini aydınlatmaya yardımcı olur.
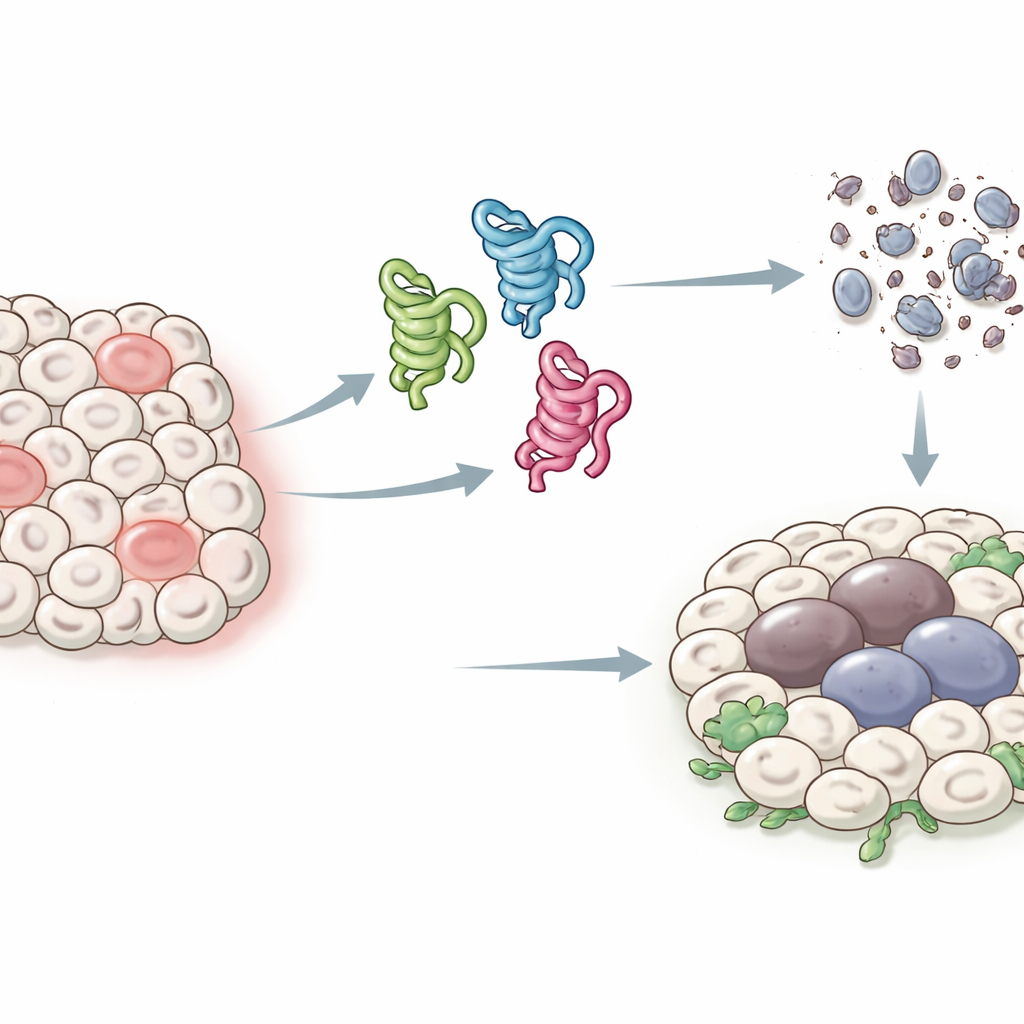
Bir koruyucu proteinin farklı yüzleri
İnsanlarda p53 geni en az bir düzine hafifçe farklı protein formu, yani izoform üretebilir; bu da her birinin ne yaptığını tayin etmeyi zorlaştırır. Meyve sineklerinde daha basit bir düzen vardır: yalnızca üç ana izoform üreten tek bir p53 geni bulunur; bunlara p53-A, p53-B ve p53-E denir. Üçü de DNA’ya bağlanabilen ortak bir çekirdek bölgeyi paylaşır, ancak uçlarında farklılıklar vardır ve bu farklılıklar diğer proteinlerle etkileşim biçimlerini değiştirir. Yazarlar bu sade sistemi, her izoformu belirli sinek dokularında ifade ederek stres veya DNA hasarı sonrası iki ana sonucu — programlı hücre ölümü (apoptoz) ve tümör büyümesini teşvik edebilen uzun süreli bir duraklama hâli olan hücresel yaşlanmaya benzeyen senesans — nasıl etkilediklerini sormak için kullandılar.
Hücre bölünme hızı sonucu nasıl değiştiriyor
Ekip ilk olarak hücre döngüsünün, yani hücre bölünmesinin ritminin, her p53 izoformunun apoptozu tetiklemesini değiştirip değiştirmediğini test etti. Sinek hücrelerini aktif olarak bölünen, belirli fazlarda durdurulmuş veya mitozu atlayan özel bir büyüme desenine geçirilmiş hâllere zorladılar. p53-A ve p53-E izoformları temkinli karar vericiler gibi davrandı: yalnızca hücreler aktif olarak döngüdeyken güçlü şekilde apoptoz indükleyebiliyorlardı. Hücreler durdurulmuşsa veya özel bir büyüme döngüsündeyse, hücre ölümü tetikleme yetenekleri büyük ölçüde ortadan kalktı. Buna karşın p53-B çok daha katıydı. Hem imaginal disklerde (gelişen dokular) hem de büyük, bölünmeyen salivary gland hücrelerinde hücrelerin bölünüp bölünmediğine bakılmaksızın güçlü apoptozu sürdü. Bu, p53 ile hücre döngüsü arasındaki ilişkinin evrensel olmayıp izoforma özgü olduğunu gösterdi.
Genleri atlayan hücre ölümüne kısa yol
Klasik ders kitabı p53 bir transkripsiyon faktörü olarak davranır: hücrenin ölüm makinasını başlatan reaper ve hid gibi genleri açar. Yazarlar p53-A ve p53-E’nin bu senaryoyu izlediğini doğruladı. Bu pro-ölüm genleri engellendiğinde, p53-A ve p53-E’nin neden olduğu apoptoz çöktü. Ancak p53-B kuralları bozdu. Ana pro-apoptotik genler genetik olarak ortadan kaldırıldığında bile p53-B hücreleri hâlâ güçlü şekilde öldürdü. Ayrıntılı deneyler nedenini gösterdi: p53-B, ölüm kaskadının en üstüne yakın yer alan “başlatıcı” kaspazın sinek karşılığı Dronc ile fiziksel olarak bağlanabiliyordu. Biyokimyasal pull-down deneyleri ve bölünmüş floresan protein testi kullanarak, hücre çekirdekleri içinde p53-B ile Dronc arasında özgül bir etkileşimi görselleştirdiler. DNA bağlama çekirdeği çıkarılmış bir p53-B versiyonu bile, Dronc kendisi mevcut olduğu sürece özel olarak tasarlanmış bir Dronc sensörünü etkinleştirebiliyor ve apoptozu tetikleyebiliyordu. Bu, p53-B’den kaspaz mekanizmasına doğrudan, transkripsiyona bağımlı olmayan bir yol olduğunu ortaya koyuyor.
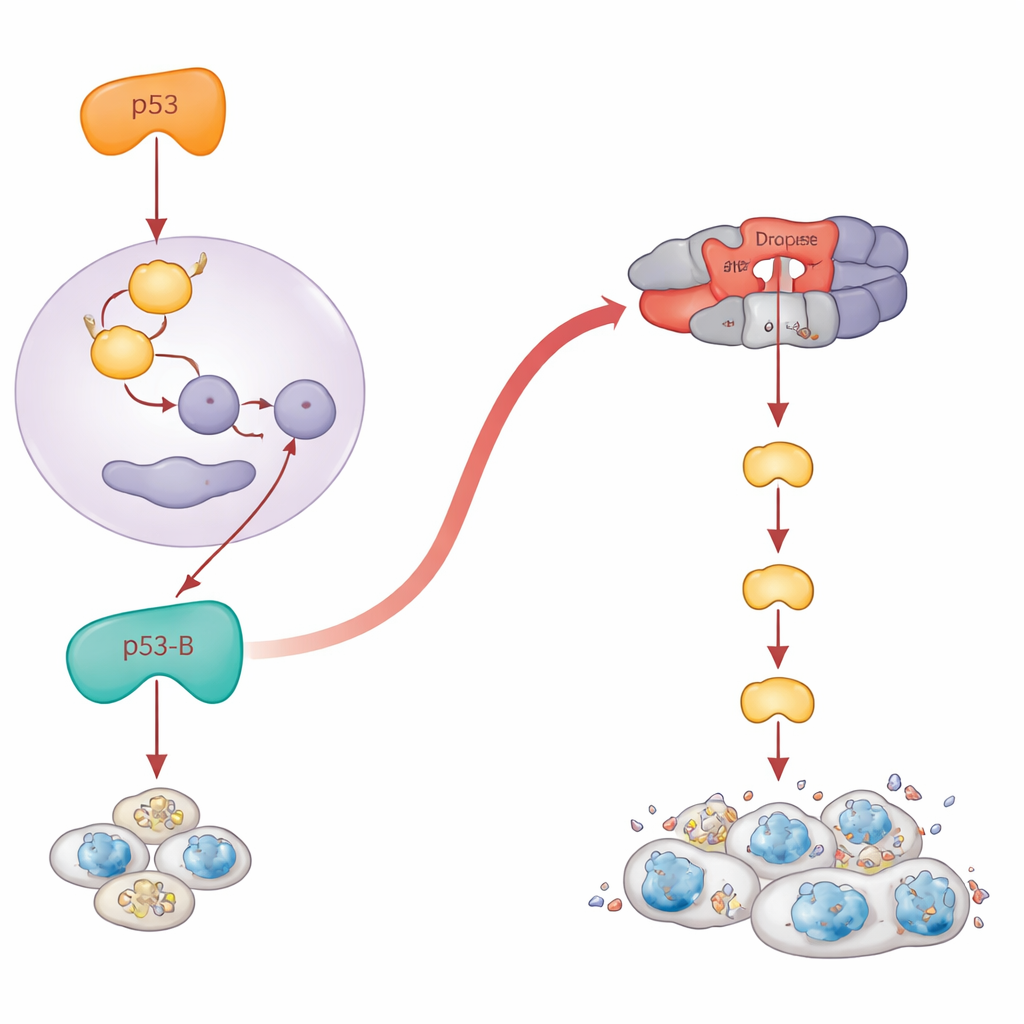
Başarısız ölümün tehlikeli büyümeye dönüşmesi
Paradoksal olarak, ölemeyen hücreler uzun ömürlü, iltihaplı ve tümörü teşvik edici hâle gelebilir. Yazarlar apoptozun engellendiği dokularda her p53 izoformunun ne yaptığını sordular. İzoformları gelişen kanatta, ya normal koşullarda ya da ana ölüm genlerinden yoksun sineklerde ifade ettiler. Apoptoz devre dışı bırakıldığında, p53-A ve p53-E artık doku küçültmedi. Bunun yerine JNK adı verilen bir stres yolunu açan ve büyüme sinyalleri salgılayan senesans-benzeri hücre cepleri ürettiler. Bu bölgeler dramatik şekilde genişleyerek hasarlı hücrelerin etrafında aşırı büyümüş, tümör benzeri yapılar oluşturdular. Dikkat çekici biçimde, p53-B de bu tür bir aşırı büyümeyi başlattı, ancak yalnızca apoptozun Dronc düzeyinde engellendiği durumlarda; eğer daha erken pro-ölüm genleri devre dışı bırakıldıysa, p53-B hâlâ hücreleri öldürmeyi başardı ve aşırı büyüme görülmedi. p53-A ve p53-E için JNK’nin açılması ve tümör büyümesi onların DNA bağlama yeteneğini gerektiriyordu; oysa p53-B DNA’ya bağlanmasa bile JNK’yi etkinleştirebiliyor ve senesansla ilişkili aşırı büyümeyi teşvik edebiliyordu; bu durum yine transkripsiyonel olmayan eylemlere işaret ediyor.
Sineğin bize insan p53’ü hakkında öğrettikleri
Araştırmacılar daha sonra bir insan p53 izoformunu (tam uzunlukta TAp53α) sinek dokularına tanıttılar. İnsan p53 kısmen sinek p53-A gibi davrandı: esas olarak pro-apoptotik genleri açarak hücreleri öldürdü ve başlatıcı kaspaz Dronc’a ihtiyaç duydu. Hücre döngüsü durdurulduğunda öldürme gücü azaldı ama tamamen ortadan kalkmadı ve DNA bağlama çekirdeği eksik bir versiyon bile Dronc’u zayıf şekilde doğrudan etkinleştirebildi; bu da korunmuş bir transkripsiyon-dışı yol olabileceğine işaret etti. Ancak önemli bir fark vardı: apoptoza yetersiz dokularda insan p53 tümör benzeri aşırı büyümeyi tetiklemedi. Bunun yerine güçlü bir şekilde hücre döngüsünü durdurdu, DNA replikasyonunu azalttı ve doku boyutunu kontrol altında tuttu; bu, insan hücre bölünmesini frenleyen iyi bilinen rolüne benziyordu.
Büyük resmi çıkarımlar
Bu çalışma tüm p53 izoformlarının aynı şekilde davranmadığını gösteriyor. Meyve sineği p53-A ve p53-E gibi bazıları ağırlıklı olarak genleri açıp kapamaya dayanır ve hücrelerin bölünüp bölünmediğine duyarlı yanıt verir. Diğerleri, p53-B gibi, DNA kontrolünü tamamen atlayabilir ve doğrudan protein–protein etkileşimleri aracılığıyla çekirdek ölüm mekanizmasına veya stres yollarına bağlanabilir. Sağlıklı dokularda bu katmanlı mekanizmalar hasarlı hücrelerin ya temizce ölmesini ya da kontrol altında bir senesans durumuna girmesini sağlamaya yardımcı olur. Ancak apoptoz engellendiğinde, aynı p53 etkinlikleri kronik stres sinyallemesi ve doku aşırı büyümesini besleyebilir. Basit bir hayvanda bu davranışları ayrıştırarak çalışma, farklı p53 versiyonlarının bazı bağlamlarda tümörleri nasıl bastırabildiğini, bazen de nasıl teşvik edebildiğini açıklamaya yardımcı olur ve p53 ile kaspazlar arasındaki doğrudan bağlantı gibi belirli etkileşimlerin gelecekteki kanser terapileri için önemli hedefler olabileceğini vurgular.
Atıf: Pérez-Aguilera, M., Ruiz-Losada, M., Gil Cortes, P. et al. Transcription-dependent and -independent functions of Drosophila p53 isoforms in the induction of apoptosis and senescence-associated tumorigenesis. Cell Death Dis 17, 367 (2026). https://doi.org/10.1038/s41419-026-08571-x
Anahtar kelimeler: p53 izoformları, apoptoz, hücre senesansı, Drosophila modelleri, tümörogenez