Clear Sky Science · ru
Транскрипционно-зависимые и -независимые функции изоформ p53 Drosophila в индукции апоптоза и сенесценции, ассоциированной с опухлеобразованием
Почему это исследование важно
Наши клетки постоянно подвергаются повреждениям от солнечного света, химикатов и обычного износа. Белок p53 известен тем, что решает, должна ли повреждённая клетка восстановиться, прекратить деление или погибнуть. Когда p53 работает неправильно, часто развиваются раковые заболевания. Это исследование использует плодовую мушку Drosophila, чтобы разобраться, как разные варианты p53 направляют клетки либо к безопасной саморазрушению, либо в опасное состояние, способствующее опухлеобразованию. Поскольку p53 у мух и людей удивительно сходен, эти результаты помогают понять, почему одни клеточные ответы на повреждение предотвращают рак, тогда как другие могут незаметно его питать.
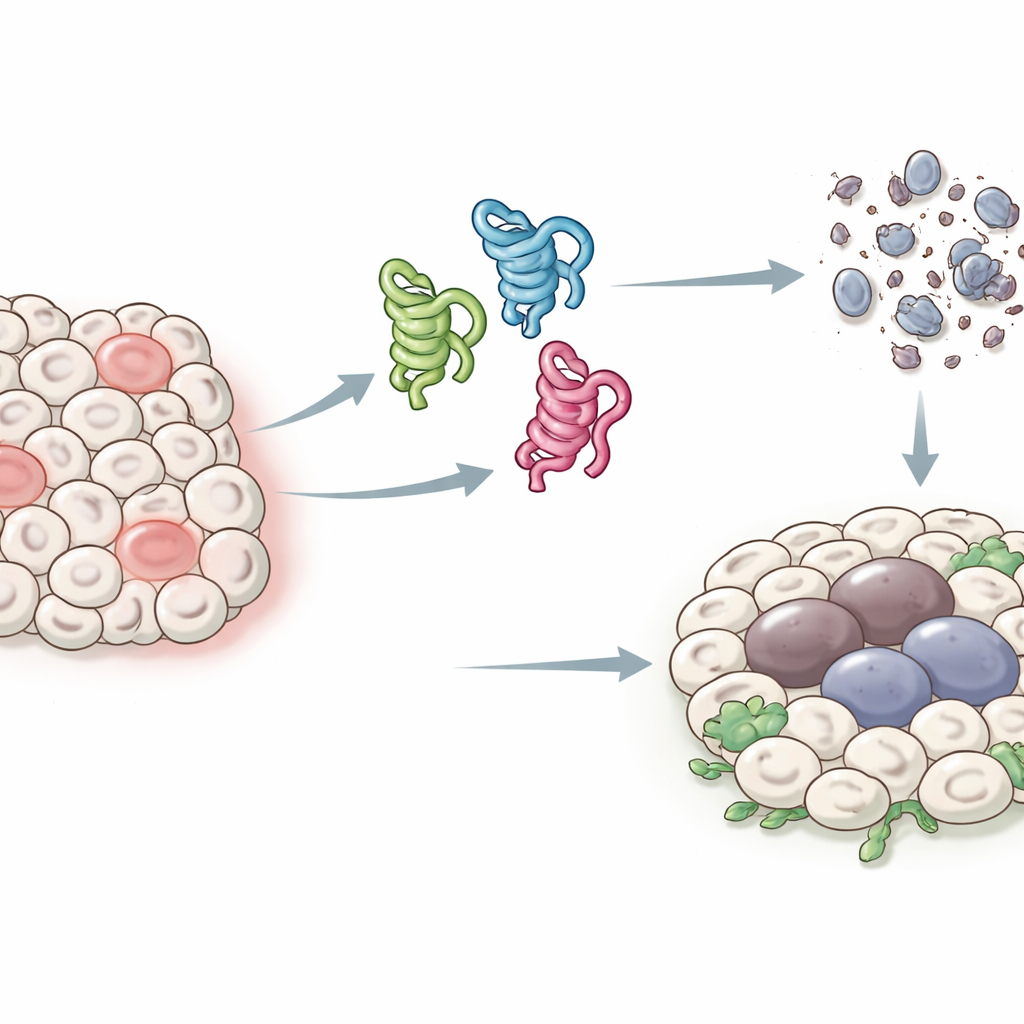
Разные лица белка-хранителя
У людей ген p53 может давать по крайней мере дюжину слегка отличающихся белковых форм, или изоформ, что затрудняло установление функций каждой из них. У плодовой мушки более простая система: единый ген p53 кодирует всего три основные изоформы, названные p53-A, p53-B и p53-E. Все три имеют общую центральную область, способную связываться с ДНК, но отличаются по концам, что меняет их взаимодействия с другими белками. Авторы воспользовались этой упрощённой системой, чтобы экспрессировать каждую изоформу в определённых тканях мухи и выяснить, как они влияют на два ключевых исхода после стресса или повреждения ДНК: программируемую гибель клеток (апоптоз) и длительное состояние ареста, напоминающее старение клеток (сенесценция), которое может способствовать росту опухолей.
Когда скорость деления клеток меняет результат
Команда сначала проверила, меняет ли клеточный цикл, ритм деления клеток, то, как каждая изоформа p53 инициирует апоптоз. Они принудительно переводили клетки мух в разные состояния: активно делящиеся, задержанные в определённых фазах или переключённые в режим роста с пропуском митоза. Изоформы p53-A и p53-E вели себя как осторожные судьямы: они могли сильно вызывать апоптоз только тогда, когда клетки активно делились. Если клетки были остановлены или находились в особом режиме роста, их способность инициировать гибель в значительной степени исчезала. Напротив, p53-B оказался гораздо менее снисходительным. Он вызывал мощный апоптоз независимо от того, делились ли клетки или нет, как в имагинальных дисках (развивающиеся ткани), так и в крупных неделящихся клетках слюнных желёз. Это продемонстрировало, что связь между p53 и клеточным циклом не универсальна, а зависит от изоформы.
Короткий путь к смерти клетки, минующий гены
Классический учебный p53 действует как фактор транскрипции: он включает гены, такие как reaper и hid, которые запускают машину клеточной гибели. Авторы подтвердили, что p53-A и p53-E следуют этому сценарию. Когда эти про-апоптотические гены блокировали, апоптоз, вызванный p53-A и p53-E, разрушался. Но p53-B нарушал правила. Даже при генетическом удалении основных про-апоптотических генов p53-B по-прежнему эффективно убивал клетки. Подробные эксперименты показали причину: p53-B способен физически связываться с Dronc, муховым эквивалентом «инициирующей» каспазы, которая стоит близко к вершине каспазного каскада. С помощью биохимических pull-down'ов и теста с раздельным флуоресцентным белком они визуализировали специфическое взаимодействие между p53-B и Dronc внутри ядер клеток. Даже версия p53-B без центрального домена связывания ДНК могла активировать специально сконструированный сенсор Dronc и вызывать апоптоз, при условии присутствия самого Dronc. Это выявляет прямой, транскрипционно-независимый путь от p53-B к каспазному механизму.
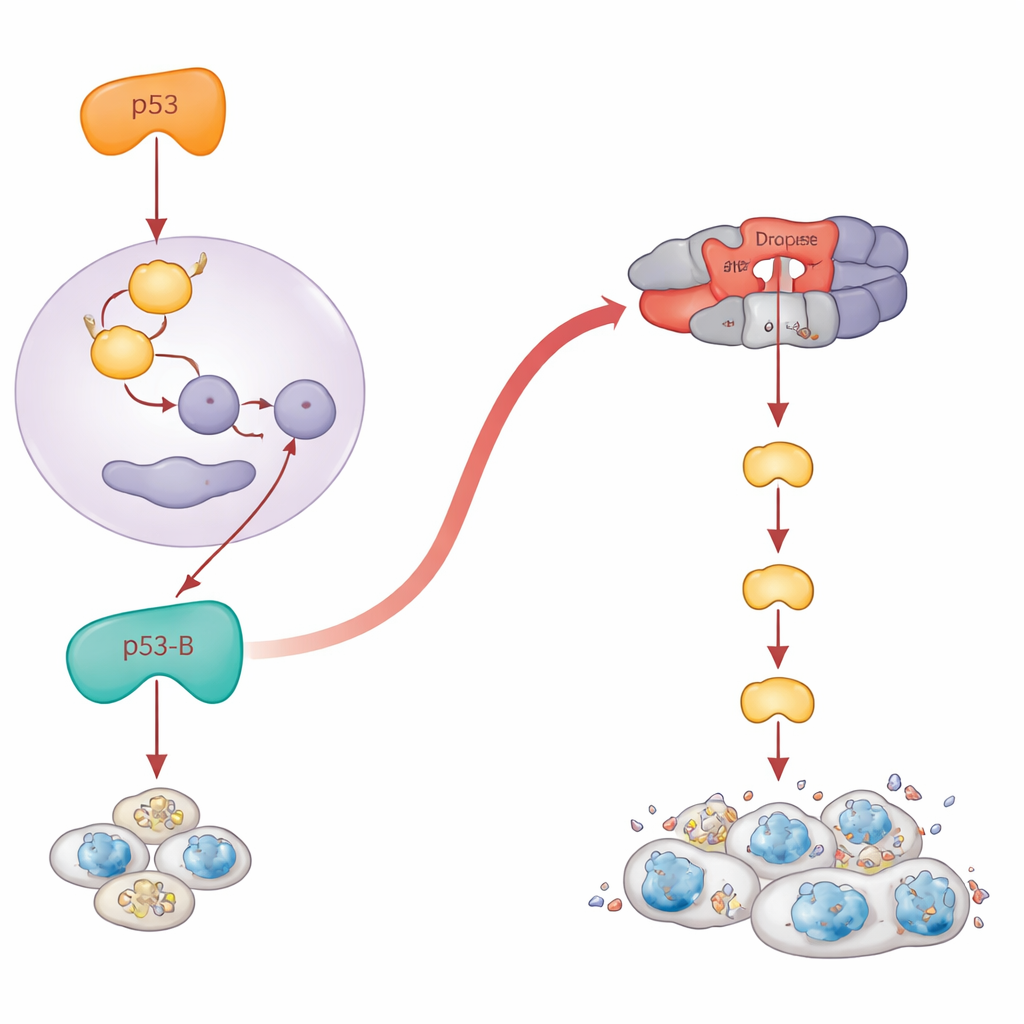
Когда неудавшаяся гибель превращается в опасный рост
Парадоксально, но клетки, которые не смогли погибнуть, могут стать долгоживущими, воспалёнными и способствовать опухолевому росту. Авторы изучили, что делает каждая изоформа p53 в тканях, где апоптоз заблокирован. Они экспрессировали изоформы в развивающемся крыле — в нормальных условиях или в мухах, лишённых ключевых генов смерти. Когда апоптоз был отключён, p53-A и p53-E переставали уменьшать ткань. Вместо этого они давали очаги клеток, похожих на сенесцентные, которые включали стрессовый путь JNK и секретировали сигналы роста. Эти регионы резко разрастались, формируя гипертрофированные, напоминающие опухоль структуры вокруг повреждённых клеток. Поразительно, что p53-B также вызывал такой рост, но только когда апоптоз был блокирован ниже по цепочке на уровне Dronc; если ранние про-апоптотические гены были отключены, p53-B всё ещё умудрялся убивать клетки и гипертрофии не возникало. Для p53-A и p53-E включение JNK и опухолевого роста требовало их способности связываться с ДНК, тогда как p53-B мог активировать JNK и способствовать росту, связанному с сенесценцией, даже без связывания ДНК, что снова указывает на нетранскрипционные механизмы.
Чему муха учит нас о человеческом p53
Исследователи затем ввели человеческую изоформу p53 (полноразмерный TAp53α) в ткани мухи. Человеческий p53 вёл себя частично как муховый p53-A: он в основном убивал клетки, включая про-апоптотические гены, и требовал инициирующей каспазы Dronc. Его убивающая способность снижалась, но не исчезала при остановке клеточного цикла, и версия без домена связывания ДНК всё ещё могла слабо активировать Dronc напрямую, намекая на сохранённый транскрипционно-независимый путь. Однако было и важное отличие: в тканях с дефектным апоптозом человеческий p53 не вызывал опухолеподобного разрастания. Вместо этого он сильно останавливал клеточный цикл, снижая репликацию ДНК и сдерживая размер ткани, подобно его известной роли тормоза деления клеток у людей.
Выводы в целом
Эта работа показывает, что не все изоформы p53 действуют одинаково. Некоторые, например муховые p53-A и p53-E, в основном опираются на включение или выключение генов и чувствительно реагируют на то, делятся ли клетки. Другие, такие как p53-B, могут обходить контроль ДНК и напрямую подключаться к ядру механизма смерти или к стрессовым путям посредством прямых белок–белковых контактов. В здоровых тканях эти многоуровневые механизмы помогают гарантировать, что повреждённые клетки либо чисто погибают, либо входят в контролируемое сенесцентное состояние. Но когда апоптоз блокирован, те же самые действия p53 могут способствовать хроническому стрессовому сигналингу и разрастанию ткани. Исследуя эти поведения в простом животном, изучение помогает объяснить, почему разные версии p53 могут подавлять опухоли в одних контекстах и способствовать им в других, а также выделяет конкретные взаимодействия — такие как прямая связь между p53 и каспазами — которые могут быть важными целями для будущих противораковых терапий.
Цитирование: Pérez-Aguilera, M., Ruiz-Losada, M., Gil Cortes, P. et al. Transcription-dependent and -independent functions of Drosophila p53 isoforms in the induction of apoptosis and senescence-associated tumorigenesis. Cell Death Dis 17, 367 (2026). https://doi.org/10.1038/s41419-026-08571-x
Ключевые слова: изоформы p53, апоптоз, клеточная сенесценция, модели Drosophila, опухлеобразование