Clear Sky Science · he
תפקודים התלויים ובלתי תלויים בטרנסקריפציה של איזו־צורת p53 בלבוקס Drosophila באינדוקציה של אפופטוזה וגידול הסרטני הקשור לסניסנס
מדוע המחקר הזה חשוב
התאים שלנו נחשפים באופן מתמיד לנזק מאור השמש, לכימיקלים ולבלאי רגיל. חלבון בשם p53 מפורסם בכך שהוא מחליט האם תא שנפגע צריך לתקן את עצמו, להפסיק להתחלק או למות. כאשר p53 לוקה בחסר, סרטן לעיתים קרובות מתפתח. מחקר זה משתמש בזבוב הפירות, Drosophila, כדי לפענח כיצד גרסאות שונות של p53 דוחפות תאים לכיוון של השמדה עצמית מבוקרת ובטוחה או לכיוון מצב מסוכן שמעודד גידול סרטני. מאחר שה־p53 של הזבוב והאדם דומים באופן מפתיע, הממצאים מסייעים להבהיר מדוע תגובות תאים שונות לנזק מונעות סרטן בעוד שאחרות עלולות דווקא לתרום לו בשקט.
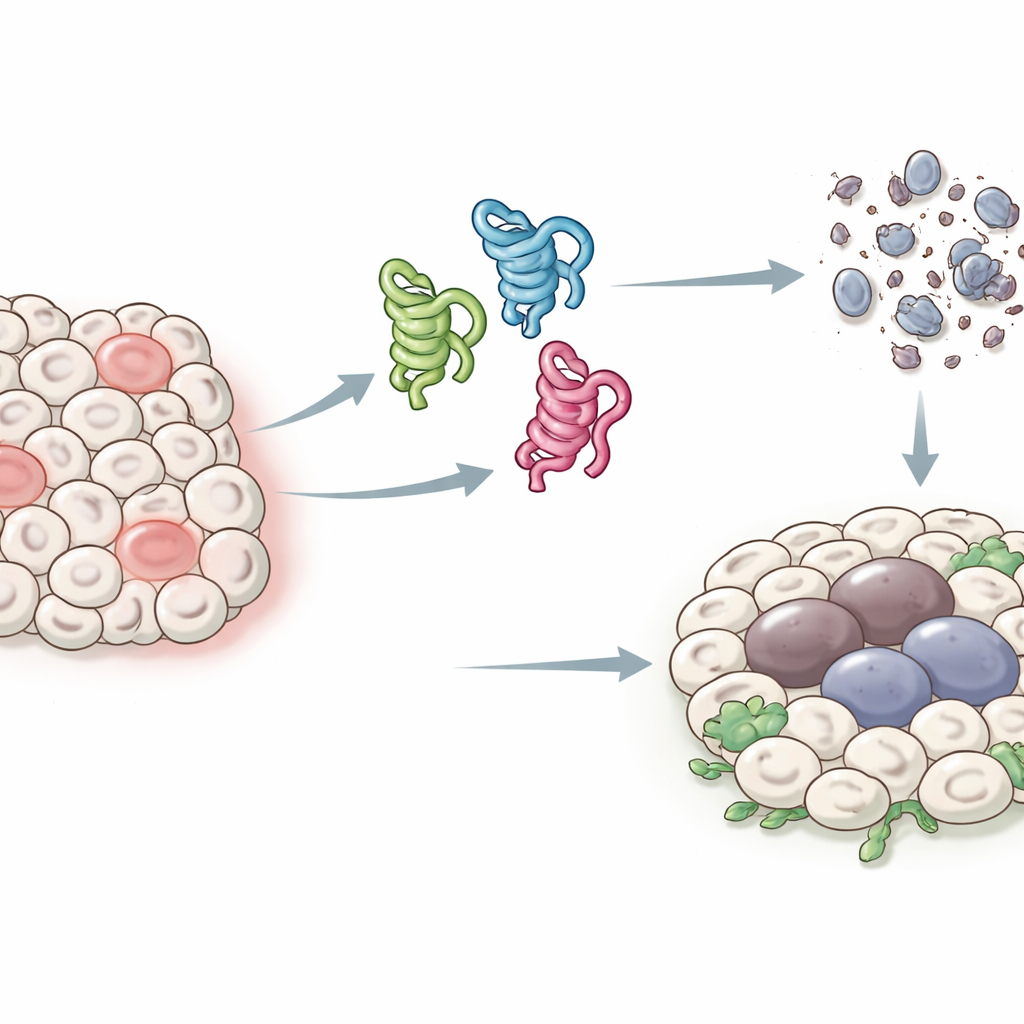
פנים שונות של חלבון שומר
בבני אדם, גן p53 יכול לייצר לפחות תריסר צורות חלבון מעט שונות, או איזואיזו־צורות, מה שהקשה על זיהוי תפקיד ספציפי לכל אחת. בזבובים יש מערכת פשוטה יותר: גן p53 יחיד שמייצר רק שלוש איזואיזו־צורות עיקריות, הנקראות p53‑A, p53‑B ו‑p53‑E. שלושתן חולקות אזור ליבת DNA, אך שונות בקצוות שלהן, מה שמשנה את האינטראקציות שלהן עם חלבונים אחרים. המחברים ניצלו את המערכת המצומצמת הזו כדי לבטא כל איזואיזו־צורה ברקמות זבוב ספציפיות ולבחון כיצד הן משפיעות על שתי תוצאות מרכזיות לאחר לחץ או נזק ל‑DNA: מוות תאי מתוכנת (אפופטוזה) ומצב עצירה ממושך הדומה להזדקנות תאית (סניסנס) שיכול לעודד גידול סרטני.
מתי קצב חלוקת התא משנה את התוצאה
הצוות בדק תחילה האם מחזור התא, המקצב של חלוקת התאים, משנה כיצד כל איזואיזו‑צורה של p53 מעוררת אפופטוזה. הם אילצו תאים של זבוב למצבים שונים: מתחלקים באופן פעיל, עצורים בשלב מסוים או הועברו לתבנית גדילה שמדלגת על מיטוזה. איזואיזו‑ה‑p53‑A ו‑p53‑E התנהגו כמו מקבלי החלטות זהירים: הן יכלו לגרום לאפופטוזה חזקה רק כאשר התאים היו במחזור פעיל. אם התאים נעצרו או היו במחזור גדילה מיוחד, היכולת שלהן לעורר מוות תאי כמעט נעלמה. לעומת זאת, p53‑B הייתה חסרת פשרות הרבה יותר. היא הובילה לאפופטוזה חזקה ללא תלות בכך שהתאים מתחלקים או לא, הן בדיסקי הדמיון (רקמות מתפתחות) והן בתאי בלוטות הרוק הגדולים שאינם מתחלקים. ממצא זה הראה שהקשר בין p53 ומחזור התא אינו אוניברסלי, אלא ספציפי לאיזואיזו‑צורה.
קיצור דרך למוות תאי שמדלג על גנים
ה־p53 הקלאסי בתיאוריה פועל כגורם שעתוק: הוא מדליק גנים כמו reaper ו‑hid המפעילים את מכונת המוות של התא. המחברים אישרו ש‑p53‑A ו‑p53‑E פועלות לפי התסריט הזה. כאשר חסמו את הגנים הפרו‑מתי המוות, האפופטוזה שגרמו p53‑A ו‑p53‑E קרסה. אבל p53‑B שבר את החוקים. גם כאשר הגנים הפרו‑אפופטוטיים המרכזיים הוסרו גנטית, p53‑B עדיין הרג תאים בעוצמה. ניסויים מפורטים הראו מדוע: p53‑B יכול לקשור פיזית את Dronc, מקבילו של זבוב לקסקאזת 'מפעיל' שנמצאת בראש מסלול המוות. באמצעות משיכות ביוכימיות וניסוי חלבון פלואורסצנטי מפוצל, הם חזו באינטראקציה ספציפית בין p53‑B ל‑Dronc בתוך גרעיני התאים. אפילו גרסה של p53‑B שמוצא ממנה ליבת קיבוע ה‑DNA הצליחה להפעיל חיישן מיוחד של Dronc ולעורר אפופטוזה, בתנאי ש‑Dronc עצמו נמצא. זה חושף מסלול ישיר, בלתי תלוי בשעתוק, מ‑p53‑B אל מכונת הקסקאזות.
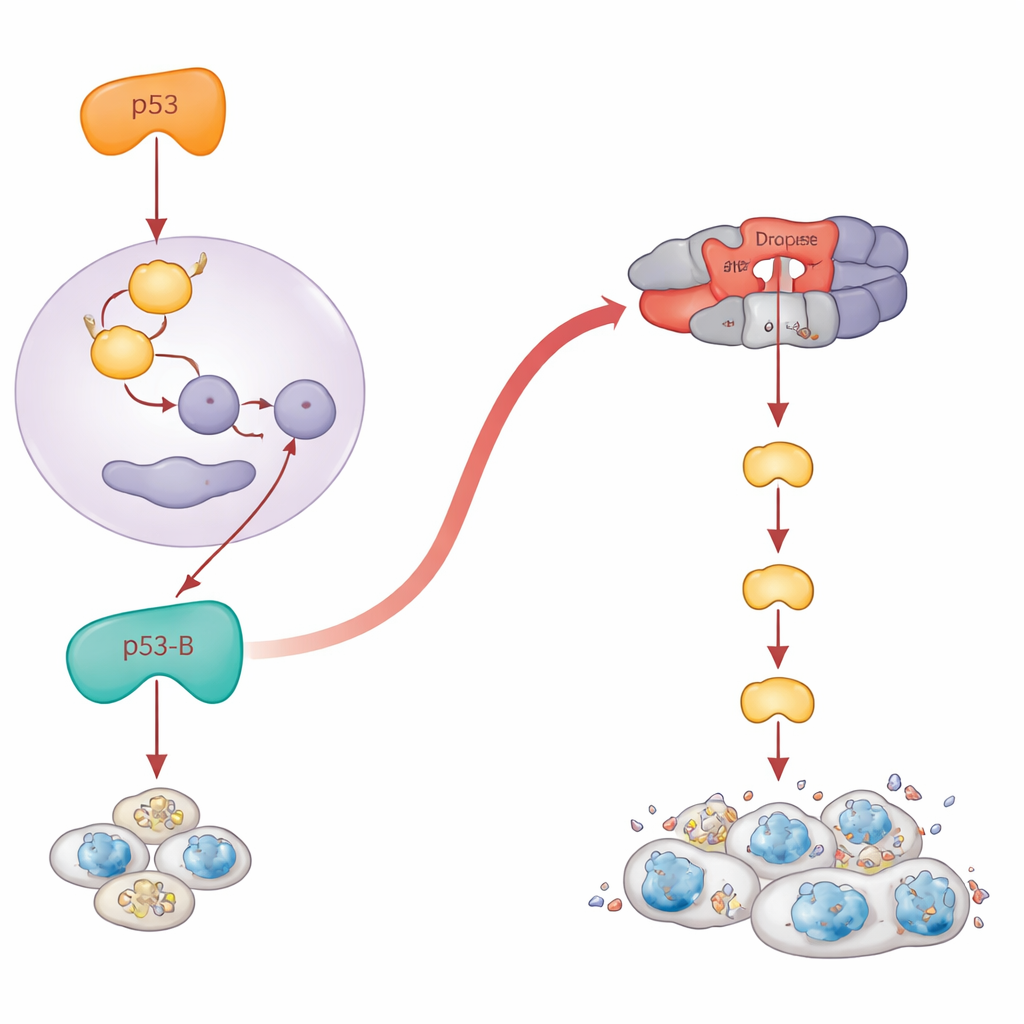
מתי כשל במוות הופך לצמיחה מסוכנת
באופן פרדוקסלי, תאים שנכשלים למות עלולים להפוך לחיי־מושך, מדוללים בדלקת ומקדמים גידול סרטני. המחברים בחנו מה כל איזואיזו‑צורה עושה ברקמות שבהן האפופטוזה נחסמת. הם הביעו את האיזואיזו‑צורות בכנף המתפתחת, בתנאים נורמליים או בזבובים חסרי גנים מרכזיים למוות. כאשר האפופטוזה הושבתה, p53‑A ו‑p53‑E כבר לא הקטינו את הנפח של הרקמה. במקום זאת הן יצרו כיסים של תאים הדומים לסניסנס שהפעילו מסלול לחץ הנקרא JNK וסיפקו אותות גדילה מופרשים. אזורים אלה התרחבו בצורה דרמטית, ויצרו מבנים מוגדלים הדומים לגידול סביב התאים שנפגעו. באופן בולט, גם p53‑B הוביל לסוג זה של גדילה-יתר, אבל רק כאשר האפופטוזה נחסמה במורד הזרם ברמת Dronc; אם הגנים הפרו‑מתי המוות המוקדמים הושבתו, p53‑B עדיין הצליח להרוג תאים ולא נצפה גדילה-יתר. אצל p53‑A ו‑p53‑E, הדלקת של JNK והגידול הסרטני דרשו את יכולתן לקשור DNA, בעוד p53‑B יכול היה להפעיל JNK ולקדם גדילה־יתר הקשורה לסניסנס גם ללא קיבוע DNA, מה שמצביע שוב על פעולות שאינן תלויות בשעתוק.
מה הזבוב מלמד אותנו על p53 האנושי
החוקרים לאחר מכן הציגו איזואיזוורת p53 אנושית (TAp53α המלאה) ברקמות הזבוב. ה‑p53 האנושי התנהג בחלקו כמו p53‑A של הזבוב: בעיקר הרג תאים על ידי הדלקת גנים פרו‑אפופטוטיים והיה תלוי בקסקאזת המפעיל Dronc. כושר ההרג שלו פחת, אך לא נעלם, כאשר מחזור התא נעצר, וגרסה שחרבה את ליבת קיבוע ה‑DNA יכלה עדיין להפעיל באופן חלש את Dronc ישירות, מרמזת על מסלול שמור בלתי תלוי בשעתוק. עם זאת, היה הבדל חשוב: ברקמות חסרות אפופטוזה, ה‑p53 האנושי לא הוביל לגדילה הדומה לגידול. במקום זאת, הוא עצר בעוצמה את מחזור התא, הפחית שכפול DNA ושמר על גודל הרקמה תחת שליטה, בדומה לתפקידו המוכר כבלם על חלוקת תאים אנושית.
מסקנות ברמת התמונה הגדולה
עבודה זו מראה שלא כל איזואיזו‑צורות p53 פועלות באותו אופן. חלקן, כמו p53‑A ו‑p53‑E של הזבוב, תלויות בעיקר בהפעלה או דיכוי של גנים ורגישות למצב חלוקת התאים. אחרות, כמו p53‑B, יכולות לדלג לחלוטין על בקרה גנטית ולהתחבר ישירות למכונת המוות או למסלולי לחץ דרך אינטראקציות חלבון–חלבון. ברקמות בריאות, מנגנונים מרובים אלה עוזרים להבטיח שתאים שניזוקו או ימותו בצורה נקייה או ייכנסו למצב סניסנס מבוקר. אך כאשר האפופטוזה נחסמת, אותן פעילויות של p53 עלולות לעודד איתות לחץ כרוני וגדילה‑יתר של הרקמה. על ידי פירוק ההתנהגויות האלה בחיה פשוטה, המחקר מסביר כיצד גרסאות שונות של p53 יכולות לדכא גידולים בהקשרים מסוימים אך לקדם אותם באחרים, ומדגיש אינטראקציות ספציפיות — כגון הקשר הישיר בין p53 וקסקאזות — שעשויות להיות מטרות חשובות לטיפולים עתידיים בסרטן.
ציטוט: Pérez-Aguilera, M., Ruiz-Losada, M., Gil Cortes, P. et al. Transcription-dependent and -independent functions of Drosophila p53 isoforms in the induction of apoptosis and senescence-associated tumorigenesis. Cell Death Dis 17, 367 (2026). https://doi.org/10.1038/s41419-026-08571-x
מילות מפתח: איזו־צורות p53, אפופטוזה, הזדקנות תאים, מודלים של Drosophila, גידול סרטני