Clear Sky Science · it
Funzioni dipendenti e indipendenti dalla trascrizione degli isoformi di p53 di Drosophila nell'induzione di apoptosi e tumorigenesi associata alla senescenza
Perché questo studio è importante
Le nostre cellule sono continuamente sottoposte a danni provocati dalla luce solare, da sostanze chimiche e dall'usura ordinaria. Una proteina chiamata p53 è famosa per decidere se una cellula danneggiata debba ripararsi, interrompere la divisione o morire. Quando p53 funziona male, spesso insorgono tumori. Questo studio utilizza il moscerino della frutta, Drosophila, per districare come diverse versioni di p53 spingano le cellule verso l'autodistruzione protettiva o verso uno stato pericoloso che favorisce i tumori. Poiché p53 di mosca e uomo sono sorprendentemente simili, questi risultati aiutano a chiarire perché alcune risposte cellulari al danno prevengono il cancro mentre altre possono, silenziosamente, alimentarlo.
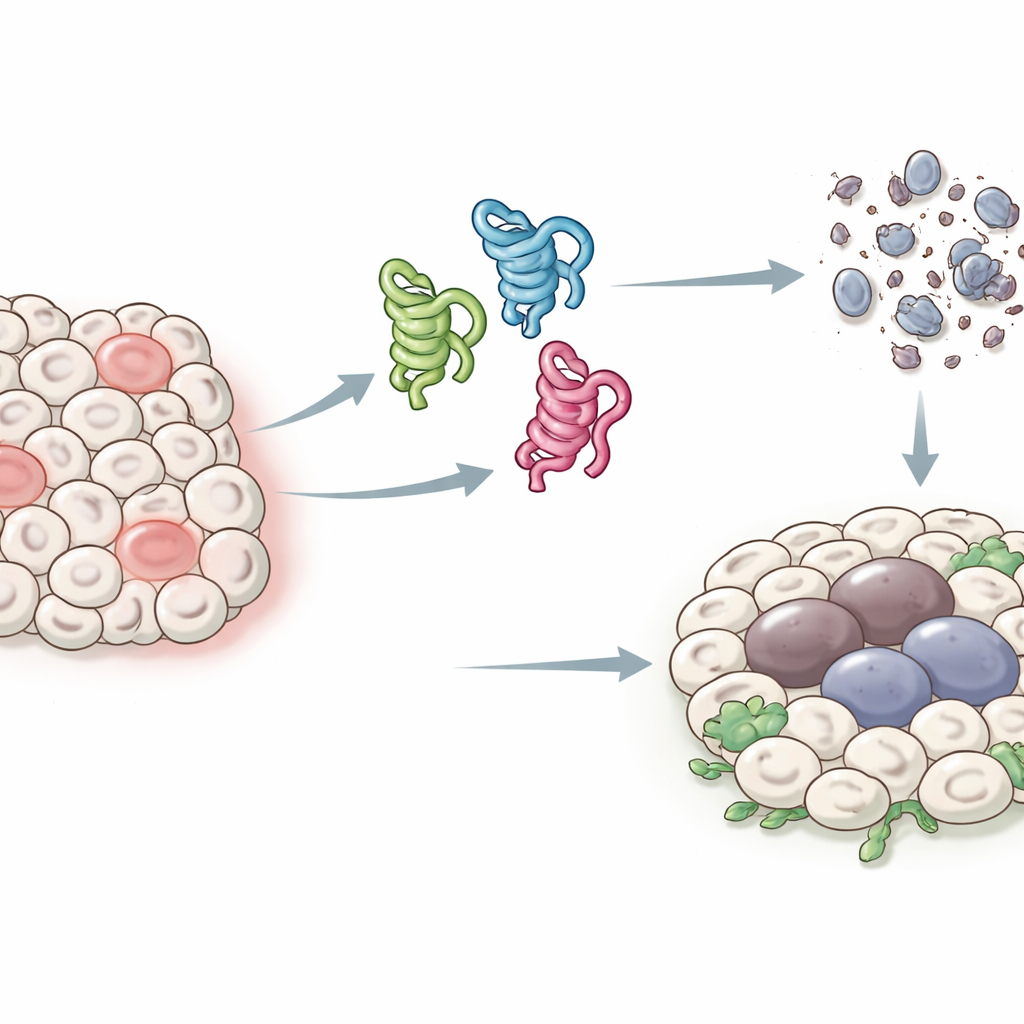
Volti diversi di una proteina guardiana
Nell'uomo, il gene p53 può produrre almeno una dozzina di forme proteiche leggermente diverse, o isoformi, il che ha reso difficile individuare la funzione di ciascuna. I moscerini hanno un assetto più semplice: un singolo gene p53 che produce solo tre isoformi principali, chiamati p53-A, p53-B e p53-E. Tutti e tre condividono una regione centrale che può legare il DNA, ma differiscono alle estremità, il che cambia il modo in cui interagiscono con altre proteine. Gli autori hanno sfruttato questo sistema semplificato per esprimere ciascun isoforma in tessuti specifici della mosca e chiedersi come influenzino due risultati chiave dopo stress o danno al DNA: la morte cellulare programmata (apoptosi) e uno stato di arresto persistente che ricorda l'invecchiamento cellulare (senescenza) e che può promuovere la crescita tumorale.
Quando la velocità di divisione cellulare cambia l'esito
Il gruppo ha prima verificato se il ciclo cellulare, il ritmo della divisione cellulare, modifichi il modo in cui ogni isoforma di p53 induce l'apoptosi. Hanno forzato le cellule di mosca in diversi stati: attivamente in divisione, bloccate in fasi particolari o deviate verso un modello di crescita che salta la mitosi. Gli isoformi p53-A e p53-E si sono comportati come decisori prudenti: potevano indurre fortemente l'apoptosi solo quando le cellule erano in ciclo attivo. Se le cellule erano arrestate o in un ciclo di crescita speciale, la loro capacità di innescare la morte cellulare svaniva in gran parte. Al contrario, p53-B è risultato molto più inflessibile. Ha guidato un'apoptosi robusta indipendentemente dal fatto che le cellule stessero dividendo o meno, sia nei discchi immaginali (tessuti in sviluppo) sia nelle grandi cellule ghiandolari non in divisione. Ciò dimostra che la relazione tra p53 e ciclo cellulare non è universale, ma specifica per isoforma.
Una scorciatoia verso la morte che bypassa i geni
Il classico p53 descritto nei testi agisce come fattore di trascrizione: attiva geni come reaper e hid che avviano la macchina della morte cellulare. Gli autori hanno confermato che p53-A e p53-E seguono questo copione. Quando questi geni pro‑morte sono stati bloccati, l'apoptosi causata da p53-A e p53-E è venuta meno. Ma p53-B ha infranto le regole. Anche quando i principali geni pro-apoptotici sono stati rimossi geneticamente, p53-B ha comunque ucciso le cellule con grande efficacia. Esperimenti dettagliati hanno mostrato il perché: p53-B può legarsi fisicamente a Dronc, l'equivalente nella mosca della caspasi “iniziatrice” che sta in cima alla cascata della morte. Usando pull-down biochimici e un saggio con proteine fluorescenti split, hanno visualizzato un'interazione specifica tra p53-B e Dronc all'interno dei nuclei cellulari. Anche una versione di p53-B privata del suo core di legame al DNA poteva ancora attivare un sensore progettato per Dronc e innescare l'apoptosi, purché Dronc fosse presente. Questo rivela una via diretta, indipendente dalla trascrizione, che collega p53-B alla macchina delle caspasi.
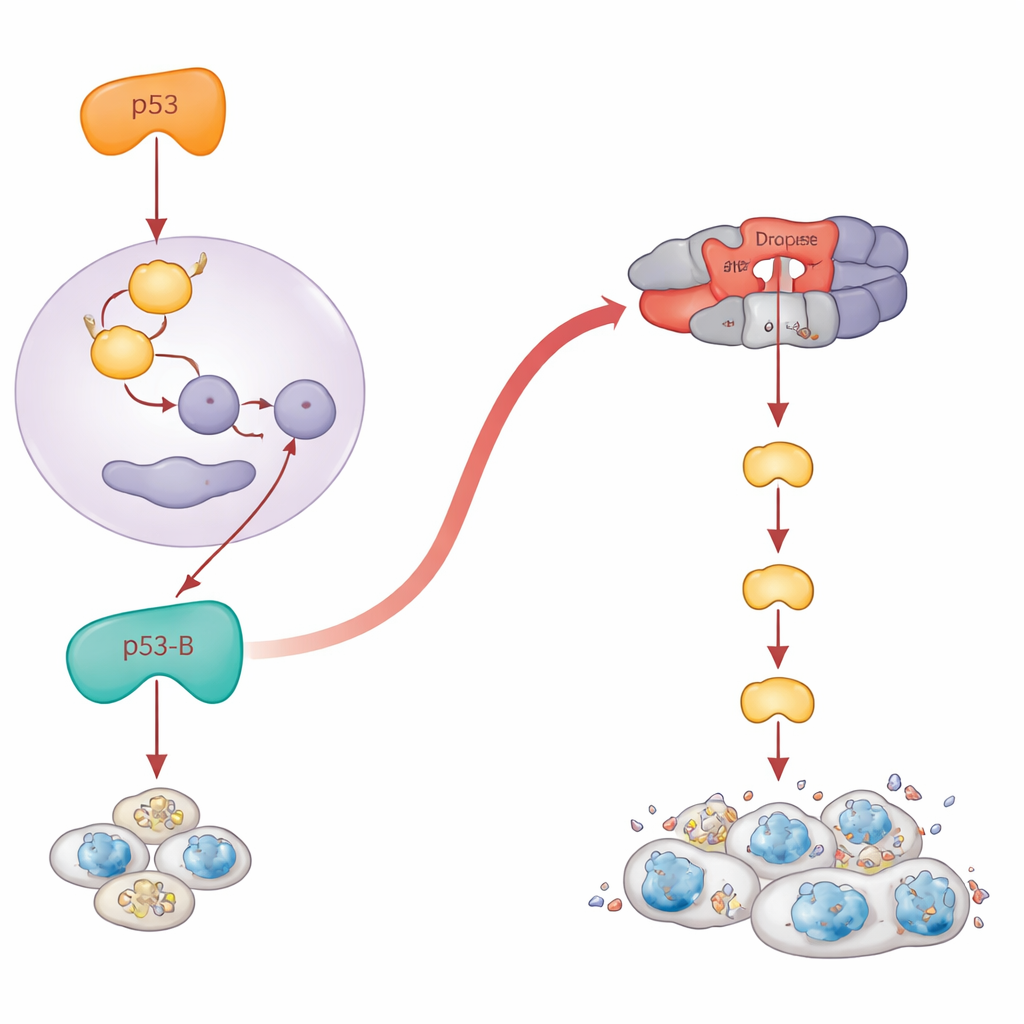
Quando la morte mancata si trasforma in crescita pericolosa
Paradossalmente, le cellule che non riescono a morire possono diventare longeve, infiammate e promotrici di tumori. Gli autori hanno chiesto cosa fa ciascun isoforma di p53 nei tessuti in cui l'apoptosi è bloccata. Hanno espresso gli isoformi nell'ala in sviluppo, sia in condizioni normali sia in mosche prive di geni chiave della morte. Quando l'apoptosi era disabilitata, p53-A e p53-E non riducevano più il tessuto. Al contrario, hanno prodotto sacche di cellule simili alla senescenza che attivavano una via di stress chiamata JNK e secern evano segnali di crescita. Queste regioni si sono espanse drasticamente, formando strutture ipertrofiche simili a tumori intorno alle cellule danneggiate. Colpisce che anche p53-B abbia promosso questo tipo di iper-crescita, ma solo quando l'apoptosi era bloccata a valle, al livello di Dronc; se i geni pro‑morte più precoci erano disattivati, p53-B riusciva comunque a uccidere le cellule e non compariva alcuna iper-crescita. Per p53-A e p53-E, l'attivazione di JNK e la crescita tumorale richiedevano la loro capacità di legare il DNA, mentre p53-B poteva attivare JNK e promuovere l'iper-crescita associata alla senescenza anche senza legare il DNA, indicando ancora una volta azioni non trascrizionali.
Cosa ci insegna la mosca sul p53 umano
I ricercatori hanno quindi introdotto un isoforma umano di p53 (la forma completa TAp53α) nei tessuti della mosca. Il p53 umano si è comportato in parte come il p53-A della mosca: uccideva principalmente le cellule attivando geni pro-apoptotici e necessitava della caspasi iniziatrice Dronc. Il suo potere di uccidere era ridotto, ma non annullato, quando il ciclo cellulare veniva arrestato, e una versione priva del core di legame al DNA poteva ancora attivare debolmente Dronc in modo diretto, suggerendo una via conservata indipendente dalla trascrizione. Tuttavia, c'era una differenza importante: nei tessuti privi di apoptosi, il p53 umano non promuoveva l'iper-crescita simile a tumori. Invece, induceva fortemente l'arresto del ciclo cellulare, riducendo la replicazione del DNA e mantenendo sotto controllo la dimensione del tessuto, molto simile al suo noto ruolo come freno sulla divisione cellulare umana.
Conclusioni generali
Questo lavoro mostra che non tutti gli isoformi di p53 agiscono allo stesso modo. Alcuni, come i p53-A e p53-E della mosca, si basano principalmente sull'attivazione o repressione genica e rispondono sensibilmente allo stato di divisione delle cellule. Altri, come p53-B, possono aggirare completamente il controllo del DNA e innestarsi direttamente nella macchina della morte o in vie di stress tramite contatti proteina‑proteina diretti. Nei tessuti sani, questi meccanismi stratificati aiutano a garantire che le cellule danneggiate muoiano in modo pulito o entrino in uno stato di senescenza confinato. Ma quando l'apoptosi è bloccata, le stesse attività di p53 possono favorire una segnalazione di stress cronica e l'iper-crescita tissutale. Dissectando questi comportamenti in un animale semplice, lo studio aiuta a spiegare come diverse versioni di p53 possano sopprimere i tumori in alcuni contesti e promuoverli in altri, e mette in evidenza interazioni specifiche — come il collegamento diretto tra p53 e le caspasi — che potrebbero essere bersagli importanti per future terapie anti‑cancro.
Citazione: Pérez-Aguilera, M., Ruiz-Losada, M., Gil Cortes, P. et al. Transcription-dependent and -independent functions of Drosophila p53 isoforms in the induction of apoptosis and senescence-associated tumorigenesis. Cell Death Dis 17, 367 (2026). https://doi.org/10.1038/s41419-026-08571-x
Parole chiave: isoformi di p53, apoptosi, senescenza cellulare, modelli di Drosophila, tumorigenesi