Clear Sky Science · ja
アポトーシス誘導と老化関連腫瘍形成におけるショウジョウバエp53アイソフォームの転写依存的および非依存的機能
この研究が重要な理由
私たちの細胞は常に日光、化学物質、日常的な摩耗などの損傷にさらされています。p53と呼ばれるタンパク質は、損傷した細胞が修復すべきか、増殖を止めるべきか、あるいは死ぬべきかを決めることで知られています。p53が機能不全に陥ると、がんが発生しやすくなります。本研究ではショウジョウバエ(Drosophila)を用いて、p53の異なるバージョン(アイソフォーム)が細胞を安全な自己破壊へと導くのか、あるいは危険で腫瘍を促進する状態へ誘導するのかを解きほぐしています。ハエとヒトのp53は驚くほど類似しているため、これらの知見は損傷に対する細胞応答のうち、なぜ一部はがんを防ぎ、他は静かにその成長を助長してしまうのかを明確にする手がかりになります。
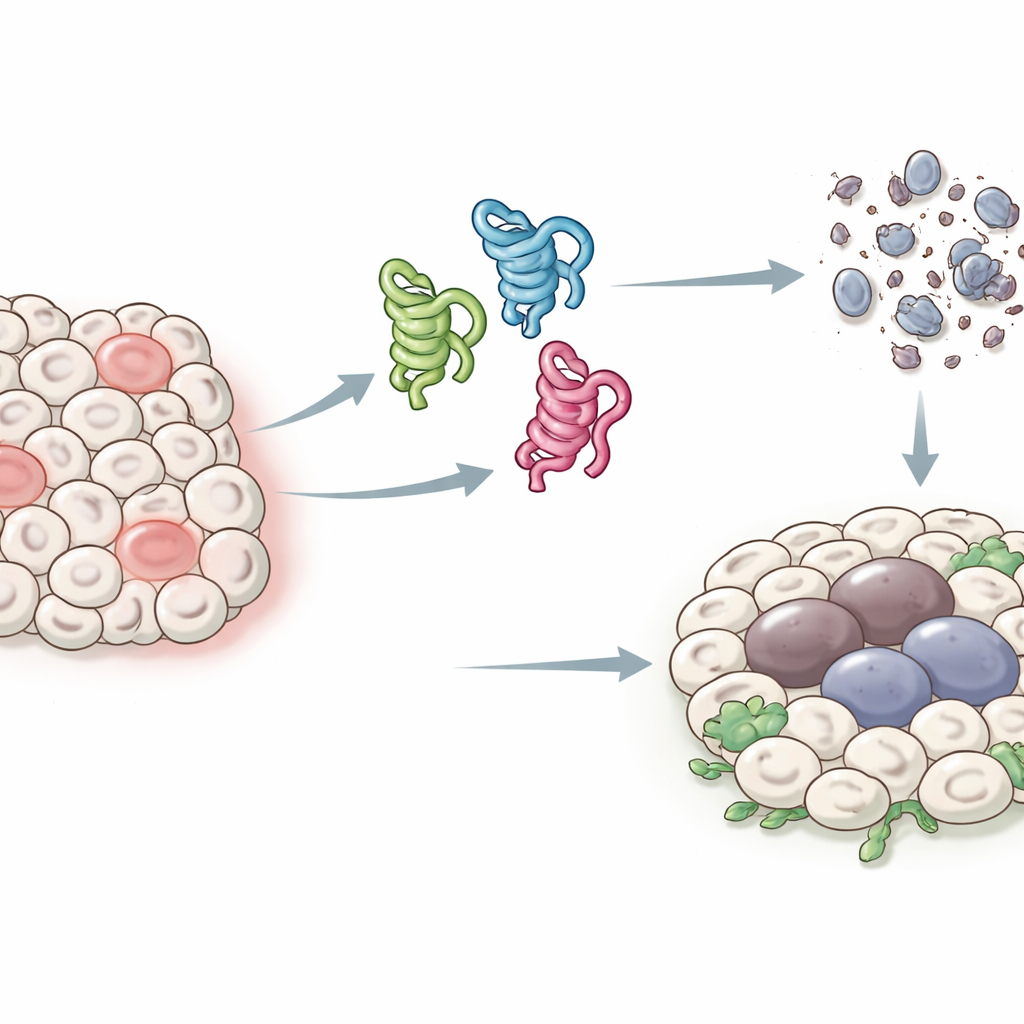
守護者タンパク質の多様な姿
ヒトでは、p53遺伝子は少なくとも十数種類のわずかに異なるタンパク質形態(アイソフォーム)を生み出すため、それぞれの機能を特定するのが難しくなっています。ショウジョウバエはより単純で、単一のp53遺伝子から主に3つのアイソフォーム(p53-A、p53-B、p53-E)だけが作られます。これらはすべてDNA結合可能な中核領域を共有しますが、端部が異なり他のタンパク質との相互作用が変わります。著者らはこの簡素化された系を利用し、各アイソフォームを特定の組織で発現させ、ストレスやDNA損傷後に起こる二つの主要な結果――プログラムされた細胞死(アポトーシス)と、腫瘍増殖を促す長期的な停止状態に似た細胞老化(セネescence)――に対する影響を調べました。
細胞分裂の速さが結果を変えるとき
研究班はまず、細胞周期(分裂のリズム)が各p53アイソフォームによるアポトーシス誘導に影響するかを検証しました。彼らはハエ細胞を活発に分裂している状態、特定の期で停止している状態、あるいは有糸分裂を飛ばす成長パターンに切り替えた状態へと強制しました。p53-Aとp53-Eは慎重な判断者のように振る舞い、細胞が活発にサイクリングしているときにのみ強くアポトーシスを誘導できました。細胞が停止しているか特殊な成長サイクルにある場合、これらのアイソフォームの細胞死誘導能はほとんど消えました。対照的に、p53-Bははるかに妥協しない性質を持っていました。分裂中か否かに関わらず、imaginal disc(発生組織)や大きく分裂しない唾液腺細胞のいずれでも強いアポトーシスを駆動しました。これはp53と細胞周期の関係が普遍的ではなく、アイソフォームごとに異なることを示しています。
遺伝子を介さない細胞死への近道
教科書的なp53は転写因子として働き、reaperやhidのような遺伝子をオンにして細胞の死の機構を始動させます。著者らはp53-Aとp53-Eがこの脚本に従うことを確認しました。これらの脱落誘導遺伝子を阻害すると、p53-Aおよびp53-Eによるアポトーシスは崩れました。しかしp53-Bは規則を破りました。主要な促死遺伝子が遺伝学的に除去されても、p53-Bは依然として強力に細胞を死に導きました。詳細な実験によりその理由が示されました:p53-BはDronc(ハエでの“イニシエーター”カスパーゼに相当)に物理的に結合できるのです。生化学的プルダウンや分割蛍光タンパク質アッセイを用いて、細胞核内でp53-BとDroncの特異的相互作用を可視化しました。DNA結合コアを取り除いたp53-Bのバージョンであっても、Droncが存在する限り特別に設計したDroncセンサーを活性化してアポトーシスを誘発できました。これはp53-Bからカスパーゼ機構への直接的で転写に依存しない経路を明らかにします。
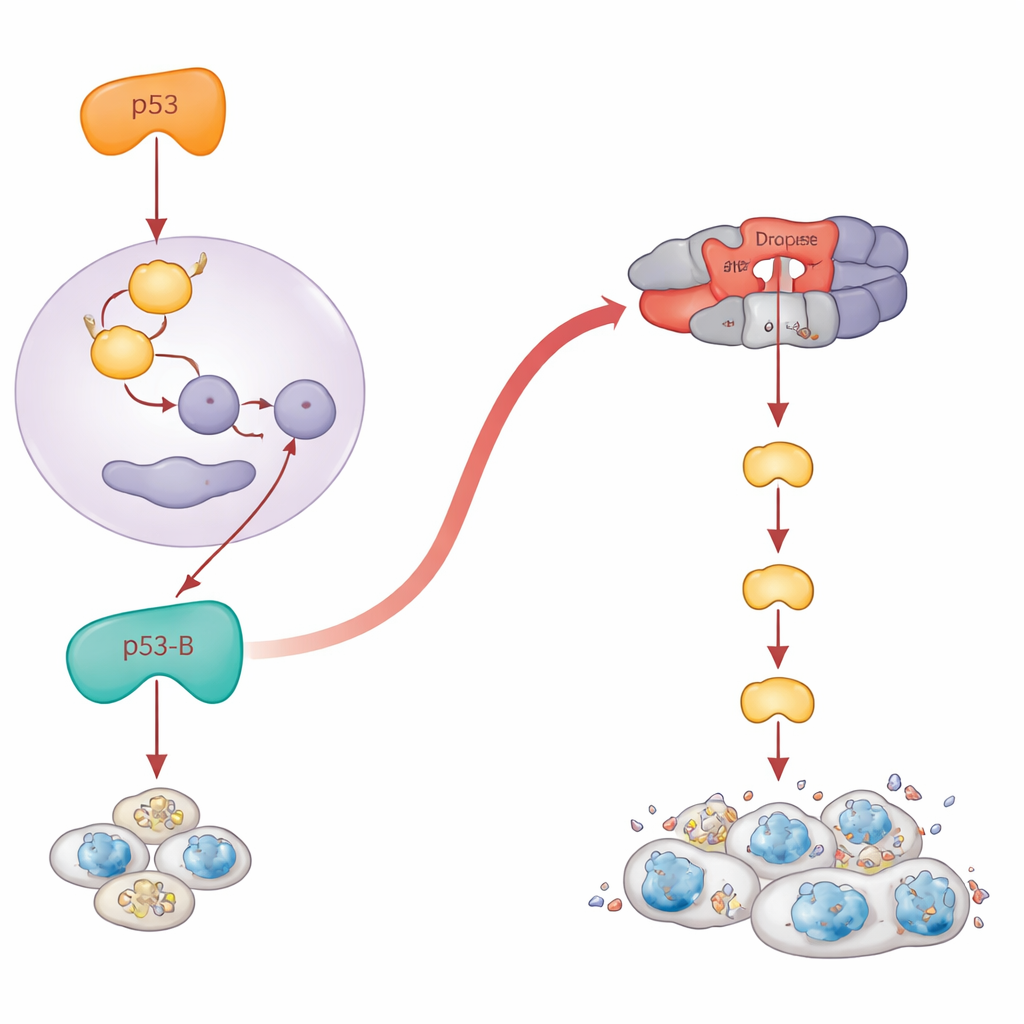
死に失敗したときに危険な増殖へ転じる場合
逆説的に、死ぬはずだった細胞が死なないと長寿化し、炎症を起こし、腫瘍を促進することがあります。著者らはアポトーシスが阻害された組織で各p53アイソフォームが何をするかを問いただしました。彼らは発生中の翅(はね)でアイソフォームを発現させ、通常条件下と主要な死因遺伝子が欠損したハエで比較しました。アポトーシスが無効化されると、p53-Aとp53-Eはもはや組織を縮小させず、代わりにJNKというストレス経路をオンにして増殖シグナルを分泌するセネセンス様の細胞の集団を生み出しました。これらの領域は劇的に拡大し、損傷細胞の周りに過成長した腫瘍様構造を形成しました。注目すべきことに、p53-Bもこの種の過成長を駆動しましたが、それはDroncのレベルで下流側のアポトーシスがブロックされたときに限られました;より上流の促死遺伝子が無効化されている場合、p53-Bは依然として細胞を死に至らしめ、過成長は現れませんでした。p53-Aとp53-Eに関しては、JNKの活性化と腫瘍増殖にはDNA結合能が必要でしたが、p53-BはDNA結合がなくてもJNKを活性化し、老化関連の過成長を促進でき、再び非転写作用を示唆しました。
ハエが人間のp53について教えてくれること
研究者らは次にヒトのp53アイソフォーム(全長のTAp53α)をハエ組織に導入しました。ヒトp53は部分的にハエのp53-Aのように振る舞い、主に促アポトーシス遺伝子をオンにして細胞を殺し、イニシエーターカスパーゼであるDroncを必要としました。細胞周期が停止するとその殺傷力は低下しましたが完全には消えず、DNA結合コアを欠くバージョンでもわずかにDroncを直接活性化できることが示され、転写非依存的な経路が保存されていることを示唆しました。しかし重要な違いもありました:アポトーシス欠損組織では、ヒトp53は腫瘍様過成長を駆動せず、代わりに強力に細胞周期を停止させてDNA複製を抑え、組織サイズを抑制しました。これはヒト細胞分裂に対するブレーキというよく知られた役割に一致します。
大局的な要点
本研究は、すべてのp53アイソフォームが同じように作用するわけではないことを示しています。ハエのp53-Aやp53-Eのように主に遺伝子のオン/オフに依存し、細胞分裂の有無に敏感に反応するものがあります。一方、p53-BのようにDNA制御を完全に迂回し、直接タンパク質–タンパク質相互作用を介して死の機構やストレス経路に接続できるものもあります。健全な組織では、これらの多層的なメカニズムが損傷細胞をきれいに死なせるか、または封じ込められたセネセント状態へ導くのを助けます。しかしアポトーシスが遮断されると、同じp53の働きが慢性的なストレスシグナル伝達や組織の過成長を助長する可能性があります。単純な動物でこれらの振る舞いを分解することで、本研究は異なるp53バージョンがある文脈では腫瘍を抑制し、別の文脈では促進してしまう理由を説明し、p53とカスパーゼ間の直接的な結びつきのような具体的な相互作用が将来のがん治療の重要な標的になり得ることを浮き彫りにしています。
引用: Pérez-Aguilera, M., Ruiz-Losada, M., Gil Cortes, P. et al. Transcription-dependent and -independent functions of Drosophila p53 isoforms in the induction of apoptosis and senescence-associated tumorigenesis. Cell Death Dis 17, 367 (2026). https://doi.org/10.1038/s41419-026-08571-x
キーワード: p53アイソフォーム, アポトーシス, 細胞老化, ショウジョウバエモデル, 腫瘍形成