Clear Sky Science · ar
وظائف معتمدة على النسخ وغير معتمدة على النسخ لأشكال p53 في ذبابة الفاكهة في تحفيز الموت المبرمج والسرطنة المرتبطة بالشيخوخة الخلوية
لماذا تهم هذه الدراسة
تتعرض خلايانا باستمرار لأضرار ناجمة عن ضوء الشمس والمواد الكيميائية والتآكل الطبيعي. بروتين يُدعى p53 مشهور بقدرته على تقرير ما إذا كان يجب على الخلية التالفة أن تصلح نفسها أو تتوقف عن الانقسام أو تموت. عندما يختل عمل p53، تنشأ في كثير من الأحيان أورام. تستخدم هذه الدراسة ذبابة الفاكهة، Drosophila، لتفكيك كيفية دفع النسخ المختلفة من p53 للخلايا إما نحو الانتحار الخاضع للرقابة أو نحو حالة خطرة تشجع الأورام. وبما أن p53 في الذبابة والإنسان متشابهان بشكل مفاجئ، تساعد هذه النتائج في توضيح سبب منع بعض استجابات الخلايا للضرر للسرطان بينما قد يغذي بعضها الآخر الورم بهدوء.
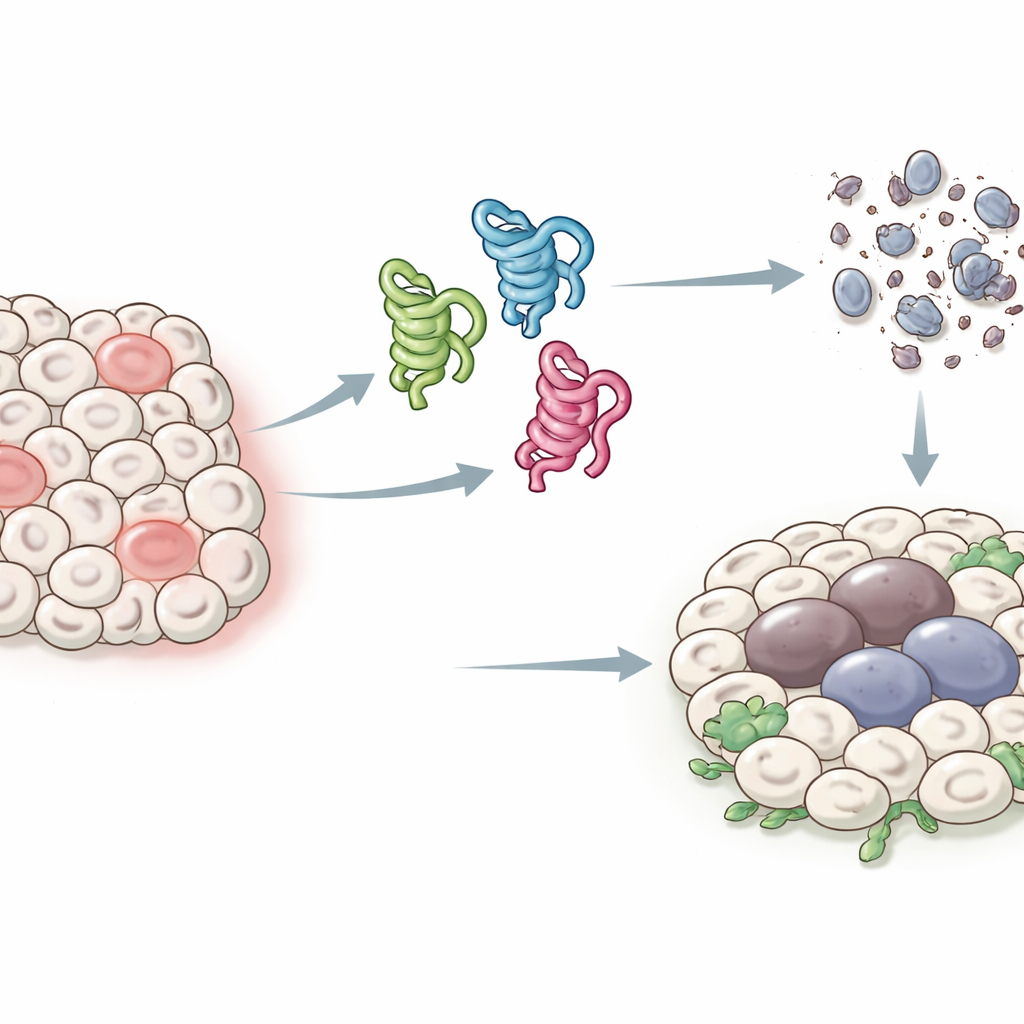
وجوه مختلفة لبروتين الحارس
في البشر، يمكن لجين p53 أن ينتج ما لا يقل عن اثني عشر نسخًا بروتينية متباينة قليلاً، مما صعّب تحديد وظيفة كلٍ منها. لدى ذباب الفاكهة إعداد أبسط: جين p53 واحد ينتج ثلاثة أشكال رئيسية فقط، تسمى p53-A وp53-B وp53-E. تشترك الثلاثة في منطقة أساسية يمكنها ربط الحمض النووي، لكنها تختلف في نهاياتها، مما يغير كيف تتفاعل مع بروتينات أخرى. استغل المؤلفون هذا النظام المبسّط للتعبير عن كل شكل في أنسجة ذبابة محددة وللسؤال عن كيفية تأثيرها على نتيجةين رئيسيتين بعد الإجهاد أو تلف الحمض النووي: موت الخلايا المبرمج (الاستماتة) وحالة توقف طويلة الأمد تشبه شيخوخة الخلايا (الشيخوخة الخلوية) التي يمكن أن تعزز نمو الأورام.
عندما يغير سرعة انقسام الخلايا النتيجة
اختبر الفريق أولاً ما إذا كان دورة الخلية، إيقاع انقسام الخلايا، يغيّر كيف يحفز كل شكل p53 الاستماتة. أرغموا خلايا الذباب على دخول حالات مختلفة: تقسم بنشاط، متوقفة في مراحل معينة، أو تحولت إلى نمط نمو يتخطى الانقسام النووي. تصرف الشكلان p53-A وp53-E كصانعي قرارات حذرين: كانا قادرين على تحفيز الاستماتة بقوة فقط عندما كانت الخلايا في حالة دورة نشطة. إذا كانت الخلايا متوقفة أو في دورة نمو خاصة، اختفت قدرتها على تحريض موت الخلايا إلى حد كبير. بالمقابل، كان p53-B أكثر صرامة. حفز استماتة قوية بغض النظر عمّا إذا كانت الخلايا منقسمة أم لا، سواء في الأقراص التخيّلية (الأنسجة النامية) أو في خلايا الغدة اللعابية الكبيرة غير المنقسمة. أظهر ذلك أن العلاقة بين p53 ودورة الخلية ليست عامة، بل خاصة بالشكل البروتيني.
طريق مختصر للموت يتجاوز الجينات
يعمل p53 الكلاسيكي في الكتب كعامل نسخ: يفعّل جينات مثل reaper وhid التي تطلق آلية موت الخلية. أكد المؤلفون أن p53-A وp53-E يتبعان هذا السيناريو. عندما عطّلوا هذه الجينات المحفزة للموت، انهارت الاستماتة التي سببها p53-A وp53-E. لكن p53-B خالف القواعد. حتى عندما أُزيلت الجينات الرئيسية المحفزة للموت وراثيًا، ظل p53-B يقتل الخلايا بقوة. أوضحت تجارب مفصلة السبب: يمكن لـ p53-B أن يرتبط ماديًا بـ Dronc، المعادل في الذبابة لكاسباز "المبادِر" الذي يجلس بالقرب من قمة شلال الموت. باستخدام سحب حيوي كيميائي ومقياس بروتين مفصول فلوريسنتي، صوروا تفاعلًا محددًا بين p53-B وDronc داخل أنوية الخلايا. حتى نسخة من p53-B نُقِصت من نواتها القابلة لربط الحمض النووي كان بإمكانها تفعيل مجس Dronc مصمّمًا خصيصًا وتحفيز الاستماتة، طالما أن Dronc نفسه كان حاضرًا. يكشف ذلك عن طريق مباشر مستقل عن النسخ من p53-B إلى آلية الكاسباز.
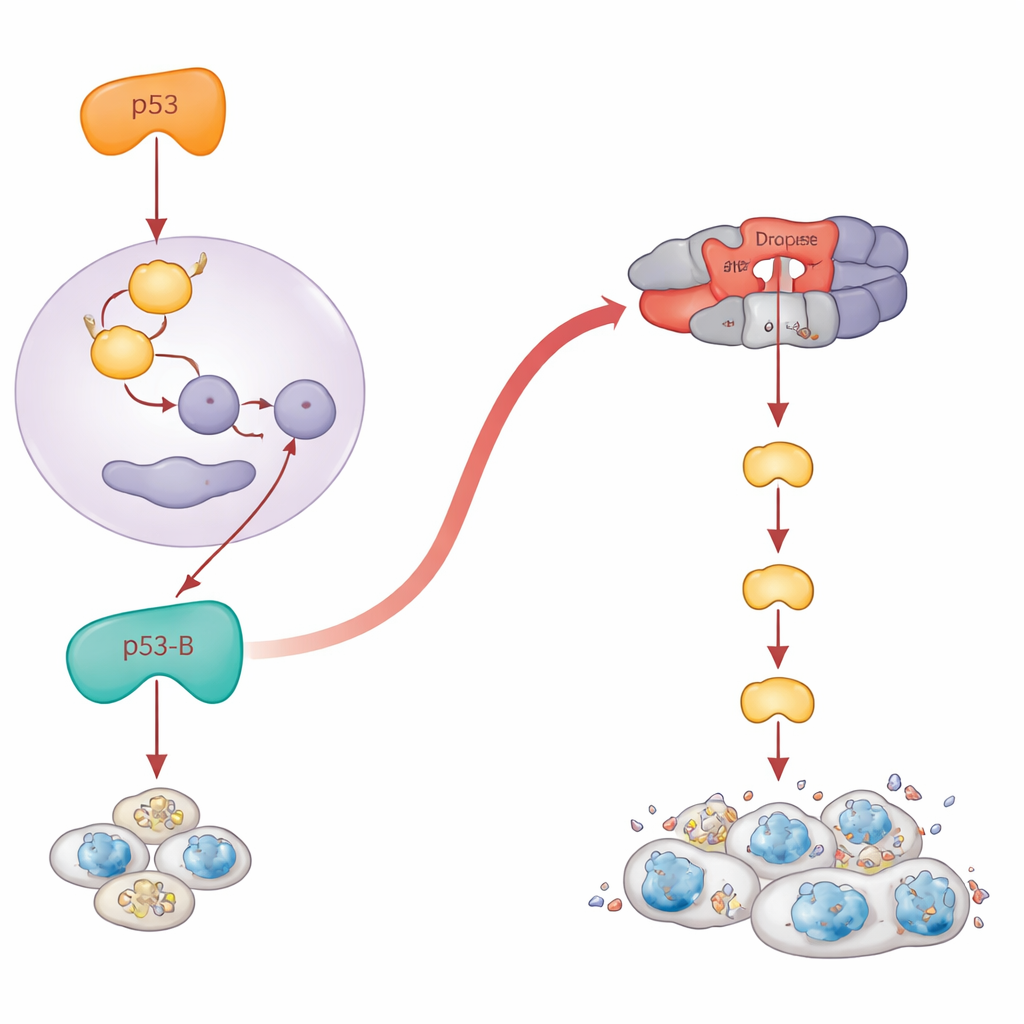
عندما يتحول الفشل في الموت إلى نمو خطير
من المفارقات أن الخلايا التي تفشل في الموت قد تصبح طويلة العمر، ملتهبة، ومروّجة للأورام. سأل المؤلفون ماذا يفعل كل شكل من أشكال p53 في أنسجة تم فيها تعطيل الاستماتة. عبّروا عن الأشكال في الجناح النامي، إما في ظروف طبيعية أو في ذباب يفتقر إلى جينات الموت الأساسية. عندما تعطلت الاستماتة، لم يعد p53-A وp53-E يقلمان النسيج. بدلًا من ذلك، أنتجا جيوبًا من خلايا شبيهة بالشيخوخة شغّلت مسارًا إجهاديًا يُدعى JNK وأفرزت إشارات نمو. توسعت هذه المناطق بشكل كبير، مكوّنة هياكل متضخمة أشبه بالأورام حول الخلايا المتضررة. اللافت أن p53-B أيضًا دفع هذا النوع من التضخم، لكن فقط عندما كانت الاستماتة معطّلة على مستوى Dronc؛ إذا عُطلت الجينات المحفزة للموت المبكرة، ظل p53-B قادرًا على قتل الخلايا ولم يظهر تضخم. بالنسبة إلى p53-A وp53-E، تطلب تشغيل JNK ونمو الورم قدرتها على ربط الحمض النووي، بينما كان بإمكان p53-B تنشيط JNK وتعزيز التضخم المرتبط بالشيخوخة حتى دون ربط الحمض النووي، مما يشير مرة أخرى إلى أفعال غير معتمدة على النسخ.
ماذا تعلمنا من الذبابة عن p53 البشري
أدخل الباحثون بعد ذلك شكلًا بشريًا من p53 (الشكل الكامل TAp53α) إلى أنسجة الذبابة. تصرف p53 البشري جزئيًا مثل p53-A في الذبابة: كان يقتل الخلايا أساسًا عن طريق تشغيل جينات محفزة للموت وكان بحاجة إلى كاسباز المبادرة Dronc. تقلّصت قوته القاتلة، لكنها لم تُلغَ، عندما توقف دورة الخلية، وكانت نسخة تفتقر إلى النواة المربوطة بالحمض النووي قادرة على تنشيط Dronc بشكل ضعيف مباشرة، مما يلمّح إلى مسار محفوظ مستقل عن النسخ. ومع ذلك، كان هناك فرق مهم: في الأنسجة الناقصة للاستماتة، لم يدفع p53 البشري إلى تضخم شبيه بالورم. بدلًا من ذلك، أوقف دورة الخلية بقوة، قلّل من تكرار الحمض النووي وحافظ على حجم النسيج تحت السيطرة، تمامًا مثل دوره المعروف ككبح لانقسام الخلايا البشرية.
استنتاجات على نطاق واسع
تُظهر هذه الدراسة أن ليس كل أشكال p53 تعمل بالمثل. بعض الأشكال، مثل p53-A وp53-E في الذبابة، تعتمد أساسًا على تشغيل أو إطفاء الجينات وتستجيب بحساسية لحالة انقسام الخلايا. أخرى، مثل p53-B، يمكنها تجاوز التحكم بالحمض النووي تمامًا والالتقاء مباشرة بآلية الموت الأساسية أو بمسارات الإجهاد عبر تواصلات بروتين–بروتين مباشرة. في الأنسجة السليمة، تساعد هذه الآليات متعددة الطبقات في ضمان أن الخلايا التالفة إما تموت بنظافة أو تدخل حالة شيخوخة محتواة. لكن عندما تُعيق الاستماتة، يمكن لنفس أنشطة p53 أن تعزز إشارات إجهاد مزمنة ونموًا نسيجيًا مفرطًا. من خلال تفكيك هذه السلوكيات في حيوان بسيط، تساعد الدراسة على تفسير كيف يمكن لإصدارات p53 المختلفة أن تكبح الأورام في بعض السياقات بينما تروّج لها في أخرى، وتبرز تداخلات محددة — مثل الرابط المباشر بين p53 والكاسبازات — التي قد تكون أهدافًا مهمة لعلاجات السرطان المستقبلية.
الاستشهاد: Pérez-Aguilera, M., Ruiz-Losada, M., Gil Cortes, P. et al. Transcription-dependent and -independent functions of Drosophila p53 isoforms in the induction of apoptosis and senescence-associated tumorigenesis. Cell Death Dis 17, 367 (2026). https://doi.org/10.1038/s41419-026-08571-x
الكلمات المفتاحية: أشكال p53, الموت المبرمج (الاستماتة), شيخوخة الخلايا, نماذج ذبابة الفاكهة, تكوّن الأورام