Clear Sky Science · pt
Funções dependentes e independentes de transcrição dos isoformas de p53 de Drosophila na indução de apoptose e tumorigenese associada à senescência
Por que este estudo importa
Nossas células enfrentam constantemente danos vindos da luz solar, de produtos químicos e do desgaste normal. Uma proteína chamada p53 é famosa por decidir se uma célula lesada deve se reparar, parar de se dividir ou morrer. Quando o p53 falha, frequentemente surgem cânceres. Este estudo usa a mosca-das-frutas, Drosophila, para desvendar como diferentes versões de p53 empurram as células tanto para a autodestruição segura quanto para um estado perigoso que promove tumores. Como o p53 de mosca e humano são surpreendentemente similares, essas descobertas ajudam a esclarecer por que algumas respostas celulares ao dano previnem o câncer enquanto outras podem silenciosamente alimentá-lo.
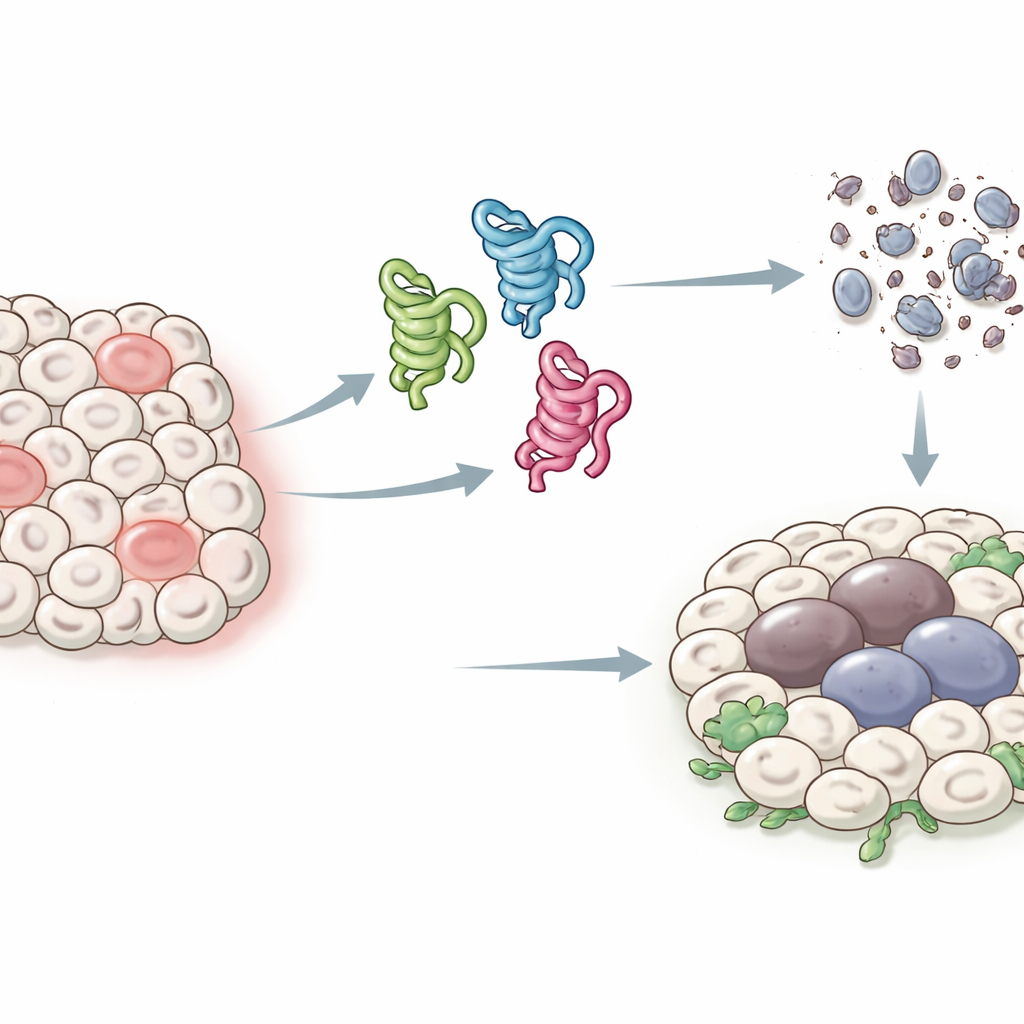
Diferentes faces de uma proteína guardiã
Em humanos, o gene p53 pode produzir pelo menos uma dúzia de formas proteicas ligeiramente diferentes, ou isoformas, o que dificulta identificar a função de cada uma. As moscas têm um sistema mais simples: um único gene p53 que gera apenas três isoformas principais, chamadas p53-A, p53-B e p53-E. Todas as três compartilham uma região central que pode se ligar ao DNA, mas diferem nas extremidades, o que altera como interagem com outras proteínas. Os autores aproveitaram esse sistema simplificado para expressar cada isoforma em tecidos específicos da mosca e perguntar como elas influenciam dois desfechos-chave após estresse ou dano ao DNA: morte celular programada (apoptose) e um estado de parada duradouro semelhante ao envelhecimento celular (senescência) que pode promover o crescimento tumoral.
Quando a velocidade da divisão celular muda o resultado
A equipe primeiro testou se o ciclo celular, o ritmo da divisão celular, altera como cada isoforma de p53 desencadeia a apoptose. Eles forçaram células de mosca a entrar em estados diferentes: dividindo-se ativamente, pausadas em fases particulares, ou convertidas para um padrão de crescimento que pula a mitose. As isoformas p53-A e p53-E comportaram-se como tomadores de decisão cautelosos: podiam induzir fortemente a apoptose apenas quando as células estavam ciclando ativamente. Se as células estavam paralisadas ou em um ciclo de crescimento especial, a capacidade de desencadear a morte celular praticamente desaparecia. Em contraste, p53-B foi muito mais inflexível. Ele promoveu apoptose robusta independentemente de as células estarem se dividindo ou não, tanto em discos imaginais (tecidos em desenvolvimento) quanto em grandes células das glândulas salivares sem divisão. Isso mostrou que a relação entre p53 e o ciclo celular não é universal, mas específica de isoforma.
Um atalho para a morte celular que contorna genes
O p53 clássico dos livros age como um fator de transcrição: ativa genes como reaper e hid que acionam a máquina de morte da célula. Os autores confirmaram que p53-A e p53-E seguem esse roteiro. Quando bloquearam esses genes pró-morte, a apoptose causada por p53-A e p53-E desmoronou. Mas p53-B quebrou as regras. Mesmo quando os principais genes pró-apoptóticos foram removidos geneticamente, p53-B ainda matou células vigorosamente. Experimentos detalhados mostraram o porquê: p53-B pode se ligar fisicamente à Dronc, o equivalente da mosca a uma caspase “iniciadora” que fica perto do topo da cascata da morte. Usando pull-downs bioquímicos e um ensaio de proteína fluorescente dividida, eles visualizaram uma interação específica entre p53-B e Dronc dentro dos núcleos celulares. Mesmo uma versão de p53-B desprovida de seu núcleo de ligação ao DNA ainda pôde ativar um sensor especialmente projetado de Dronc e desencadear apoptose, desde que Dronc estivesse presente. Isso revela uma via direta, independente de transcrição, de p53-B até a maquinaria de caspases.
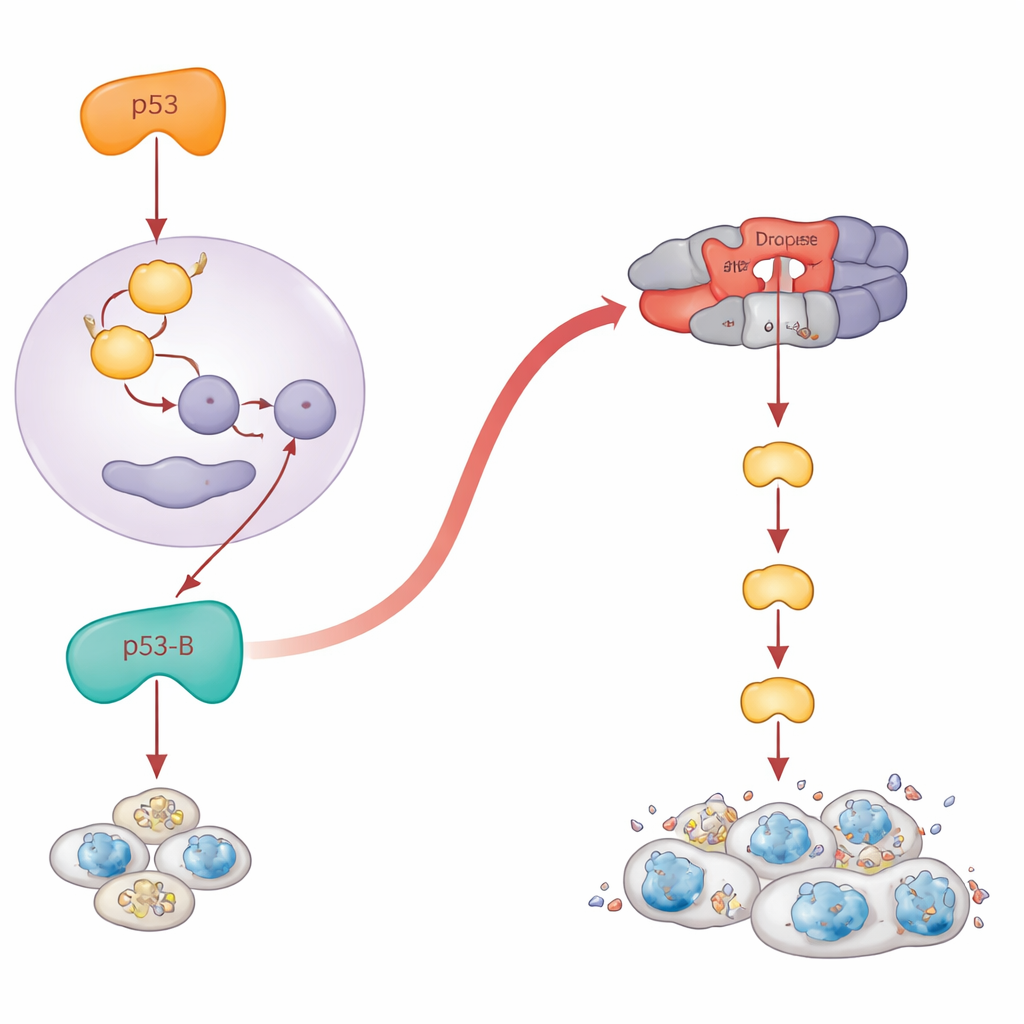
Quando a falha na morte se transforma em crescimento perigoso
Paradoxalmente, células que não conseguem morrer podem tornar-se longevivas, inflamadas e promotoras de tumores. Os autores investigaram o que cada isoforma de p53 faz em tecidos onde a apoptose está bloqueada. Eles expressaram as isoformas na asa em desenvolvimento, tanto em condições normais quanto em moscas sem genes chave da morte. Quando a apoptose foi desativada, p53-A e p53-E deixaram de reduzir o tecido. Em vez disso, produziram bolsões de células semelhantes à senescência que ligaram uma via de estresse chamada JNK e secretaram sinais de crescimento. Essas regiões expandiram-se dramaticamente, formando estruturas supercrescidas semelhantes a tumores ao redor das células danificadas. Notavelmente, p53-B também promoveu esse tipo de hiperplasia, mas somente quando a apoptose estava bloqueada a montante no nível de Dronc; se os genes pró-morte iniciais fossem desativados, p53-B ainda conseguia matar células e nenhum crescimento excessivo aparecia. Para p53-A e p53-E, a ativação de JNK e o crescimento tumoral exigiam sua habilidade de ligar-se ao DNA, enquanto p53-B podia ativar JNK e promover o crescimento associado à senescência mesmo sem ligar-se ao DNA, apontando novamente para ações não transcricionais.
O que a mosca nos ensina sobre o p53 humano
Os pesquisadores então introduziram uma isoforma humana de p53 (o TAp53α de comprimento total) em tecidos de mosca. O p53 humano comportou-se em parte como o p53-A da mosca: matou células principalmente ativando genes pró-apoptóticos e necessitava da caspase iniciadora Dronc. Seu poder de matar foi reduzido, mas não abolido, quando o ciclo celular foi interrompido, e uma versão sem o núcleo de ligação ao DNA ainda pôde ativar fracamente Dronc diretamente, sugerindo uma rota conservada independente de transcrição. No entanto, houve uma diferença importante: em tecidos deficientes em apoptose, o p53 humano não induziu crescimento tumoral. Em vez disso, ele arrestou fortemente o ciclo celular, reduzindo a replicação do DNA e mantendo o tamanho do tecido sob controle, muito parecido com seu papel bem conhecido como freio da divisão celular humana.
Principais conclusões
Este trabalho mostra que nem todas as isoformas de p53 agem da mesma forma. Algumas, como p53-A e p53-E da mosca, dependem principalmente de ligar ou desligar genes e respondem sensivelmente a se as células estão se dividindo. Outras, como p53-B, podem contornar completamente o controle do DNA e conectar-se diretamente à maquinaria central da morte, ou a vias de estresse, por meio de contatos proteína–proteína diretos. Em tecidos saudáveis, esses mecanismos em camadas ajudam a garantir que células danificadas ou morram de forma limpa ou entrem em um estado senescente contido. Mas quando a apoptose é bloqueada, as mesmas atividades de p53 podem fomentar sinalização de estresse crônico e crescimento tecidual. Ao dissecar esses comportamentos em um animal simples, o estudo ajuda a explicar como diferentes versões de p53 podem suprimir tumores em alguns contextos e ainda promovê-los em outros, e destaca interações específicas — como a ligação direta entre p53 e caspases — que podem ser alvos importantes para futuras terapias contra o câncer.
Citação: Pérez-Aguilera, M., Ruiz-Losada, M., Gil Cortes, P. et al. Transcription-dependent and -independent functions of Drosophila p53 isoforms in the induction of apoptosis and senescence-associated tumorigenesis. Cell Death Dis 17, 367 (2026). https://doi.org/10.1038/s41419-026-08571-x
Palavras-chave: isoformas de p53, apoptose, senescência celular, modelos de Drosophila, tumorogênese