Clear Sky Science · es
Funciones dependientes y no dependientes de la transcripción de los isoformas de p53 de Drosophila en la inducción de apoptosis y la tumorogénesis asociada a senescencia
Por qué importa este estudio
Nuestras células enfrentan continuamente daños por la luz solar, productos químicos y el desgaste normal. Una proteína llamada p53 es conocida por decidir si una célula dañada debe repararse, dejar de dividirse o morir. Cuando p53 falla, con frecuencia surgen cánceres. Este estudio utiliza la mosca de la fruta, Drosophila, para desentrañar cómo distintas versiones de p53 empujan a las células bien hacia una autodestrucción segura o bien hacia un estado peligroso que favorece tumores. Dado que el p53 de mosca y humano son sorprendentemente similares, estos hallazgos ayudan a aclarar por qué algunas respuestas celulares al daño previenen el cáncer mientras que otras pueden, de forma silenciosa, alimentarlo.
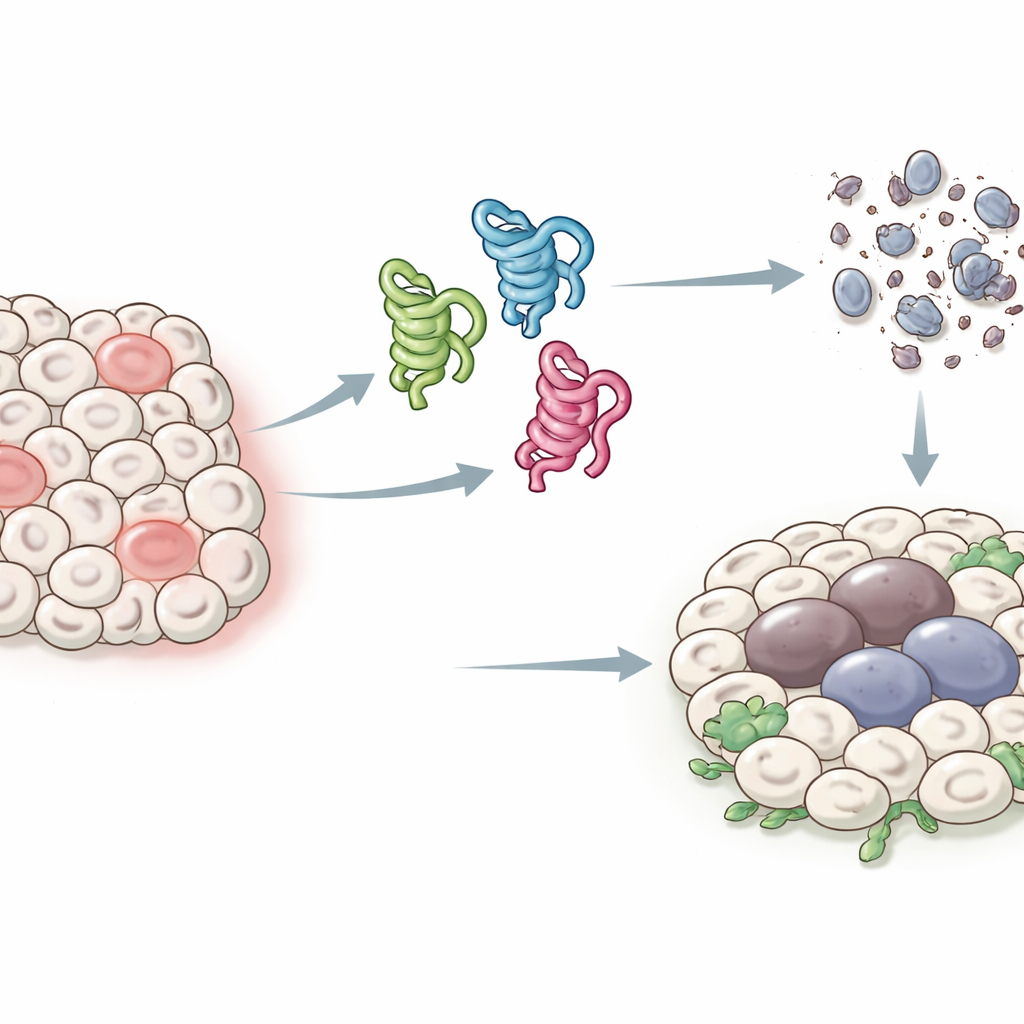
Diferentes caras de una proteína guardiana
En humanos, el gen p53 puede producir al menos una docena de formas proteicas ligeramente distintas, o isoformas, lo que ha dificultado identificar la función de cada una. Las moscas de la fruta tienen una configuración más simple: un único gen p53 que genera solo tres isoformas principales, llamadas p53-A, p53-B y p53-E. Las tres comparten una región central capaz de unirse al ADN, pero difieren en los extremos, lo que altera cómo interactúan con otras proteínas. Los autores aprovecharon este sistema simplificado para expresar cada isoforma en tejidos concretos de la mosca y estudiar cómo influyen en dos resultados clave tras el estrés o el daño del ADN: la muerte celular programada (apoptosis) y un estado prolongado de paro parecido al envejecimiento celular (senescencia) que puede promover el crecimiento tumoral.
Cuando la velocidad de división celular cambia el resultado
El equipo primero probó si el ciclo celular, el ritmo de división celular, modifica cómo cada isoforma de p53 desencadena la apoptosis. Fueron forzadas células de mosca a distintos estados: dividiéndose activamente, detenidas en fases particulares, o convertidas a un patrón de crecimiento que evita la mitosis. Las isoformas p53-A y p53-E se comportaron como tomadores de decisiones cautelosos: podían inducir apoptosis de forma fuerte solo cuando las células estaban en ciclo activo. Si las células estaban arrestadas o en un ciclo de crecimiento especial, su capacidad para provocar la muerte celular prácticamente desaparecía. En contraste, p53-B fue mucho más inflexible. Provocó una apoptosis robusta independientemente de si las células se dividían o no, tanto en los discos imaginales (tejidos en desarrollo) como en grandes células de la glándula salival no divisorias. Esto demostró que la relación entre p53 y el ciclo celular no es universal, sino específica de la isoforma.
Un atajo hacia la muerte celular que evita los genes
El p53 clásico de libro actúa como factor de transcripción: activa genes como reaper e hid que ponen en marcha la maquinaria de muerte celular. Los autores confirmaron que p53-A y p53-E siguen este guion. Cuando bloquearon estos genes pró-muerte, la apoptosis causada por p53-A y p53-E colapsó. Pero p53-B rompió las reglas. Incluso cuando los principales genes proapoptóticos se eliminaron genéticamente, p53-B seguía matando células con gran eficacia. Experimentos detallados explicaron por qué: p53-B puede unirse físicamente a Dronc, el equivalente en mosca de una caspasa “iniciadora” que se sitúa cerca de la cima de la cascada de muerte. Mediante pull-downs bioquímicos y un ensayo de proteína fluorescente dividida, visualizaron una interacción específica entre p53-B y Dronc dentro de los núcleos celulares. Incluso una versión de p53-B desprovista de su núcleo de unión al ADN pudo activar un sensor diseñado para Dronc y desencadenar apoptosis, siempre que Dronc estuviera presente. Esto revela una vía directa, independiente de la transcripción, desde p53-B hasta la maquinaria de caspasas.
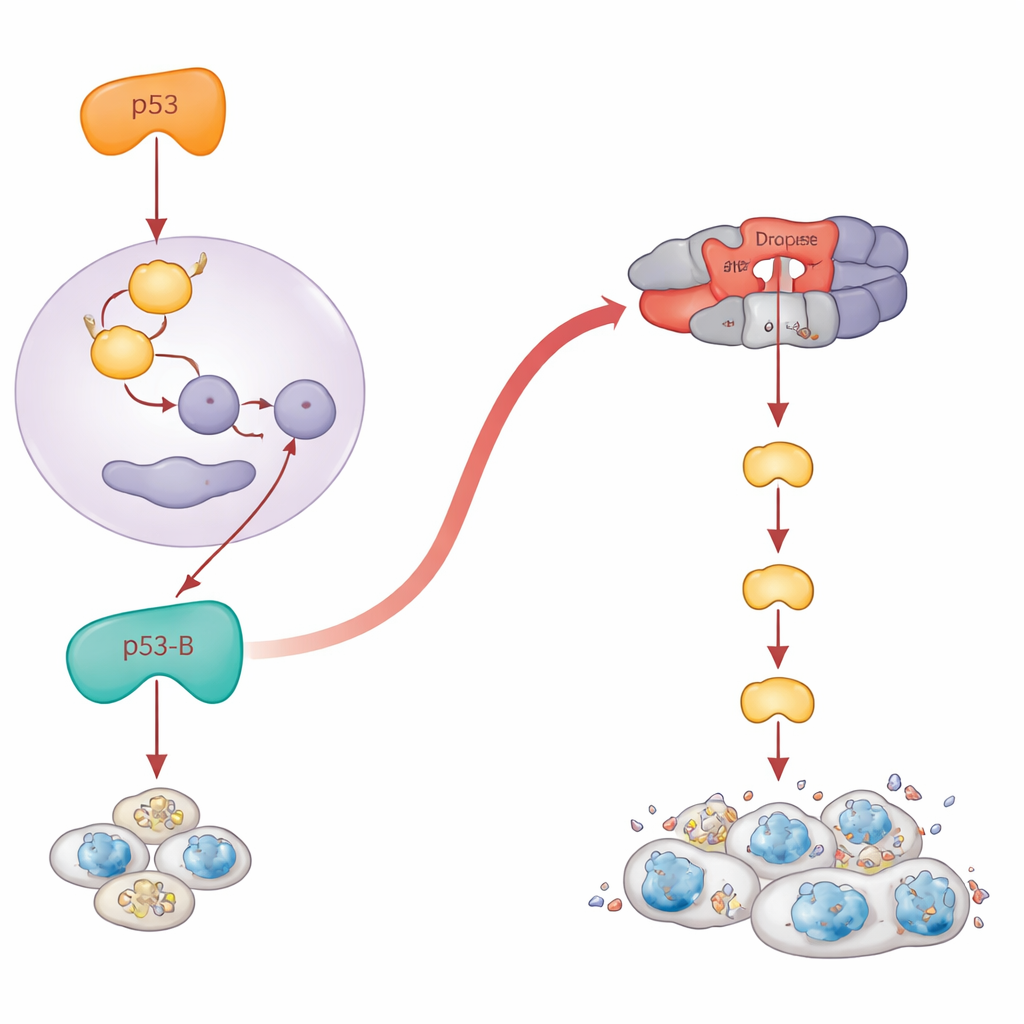
Cuando la muerte fallida se convierte en crecimiento peligroso
Paradójicamente, las células que no logran morir pueden volverse longevas, inflamadas y promotoras de tumores. Los autores interrogaban qué hace cada isoforma de p53 en tejidos donde la apoptosis está bloqueada. Expresaron las isoformas en el ala en desarrollo, tanto en condiciones normales como en moscas carentes de genes clave de muerte. Cuando la apoptosis quedó desactivada, p53-A y p53-E dejaron de achicar el tejido. En su lugar, generaron bolsillos de células con rasgos de senescencia que activaron una vía de estrés llamada JNK y secretaron señales de crecimiento. Estas regiones se expandieron dramáticamente, formando estructuras sobredesarrolladas similares a tumores alrededor de las células dañadas. De manera llamativa, p53-B también impulsó este tipo de sobrecrecimiento, pero solo cuando la apoptosis fue bloqueada aguas abajo a nivel de Dronc; si los genes pró-muerte tempranos estaban desactivados, p53-B todavía consiguió matar células y no aparecía sobrecrecimiento. Para p53-A y p53-E, la activación de JNK y el crecimiento tumoral requirieron su capacidad de unión al ADN, mientras que p53-B pudo activar JNK y promover el sobrecrecimiento ligado a senescencia incluso sin unirse al ADN, apuntando de nuevo a acciones no transcripcionales.
Lo que la mosca nos enseña sobre el p53 humano
Los investigadores introdujeron luego una isoforma humana de p53 (la forma completa TAp53α) en tejidos de mosca. El p53 humano se comportó en parte como el p53-A de la mosca: mataba principalmente activando genes proapoptóticos y necesitaba la caspasa iniciadora Dronc. Su potencia letal se redujo, pero no se abolió, cuando se detuvo el ciclo celular, y una versión carente del núcleo de unión al ADN pudo aún activar débilmente a Dronc de forma directa, sugiriendo una vía conservada independiente de la transcripción. Sin embargo, hubo una diferencia importante: en tejidos deficientes en apoptosis, el p53 humano no provocó sobrecrecimiento tipo tumoral. En su lugar, detuvo fuertemente el ciclo celular, reduciendo la replicación del ADN y manteniendo el tamaño del tejido bajo control, muy parecido a su conocido papel como freno de la división celular en humanos.
Conclusiones generales
Este trabajo muestra que no todas las isoformas de p53 actúan igual. Algunas, como las p53-A y p53-E de la mosca, dependen principalmente de activar o desactivar genes y responden con sensibilidad a si las células se están dividiendo. Otras, como p53-B, pueden eludir por completo el control del ADN y conectarse directamente con la maquinaria central de muerte, o con vías de estrés, mediante contactos proteína–proteína directos. En tejidos sanos, estos mecanismos superpuestos ayudan a asegurar que las células dañadas o bien mueran limpiamente o entren en un estado senescente contenido. Pero cuando la apoptosis está bloqueada, esas mismas actividades de p53 pueden fomentar señalización de estrés crónico y sobrecrecimiento tisular. Al diseccionar estos comportamientos en un animal sencillo, el estudio ayuda a explicar cómo distintas versiones de p53 pueden suprimir tumores en algunos contextos y promoverlos en otros, y destaca interacciones específicas —como el vínculo directo entre p53 y las caspasas— que podrían ser objetivos importantes para futuras terapias contra el cáncer.
Cita: Pérez-Aguilera, M., Ruiz-Losada, M., Gil Cortes, P. et al. Transcription-dependent and -independent functions of Drosophila p53 isoforms in the induction of apoptosis and senescence-associated tumorigenesis. Cell Death Dis 17, 367 (2026). https://doi.org/10.1038/s41419-026-08571-x
Palabras clave: isoformas de p53, apoptosis, senescencia celular, modelos de Drosophila, tumorogénesis