Clear Sky Science · fr
Fonctions dépendantes et indépendantes de la transcription des isoformes de p53 de Drosophila dans l’induction de l’apoptose et la tumorigénèse associée à la sénescence
Pourquoi cette étude est importante
Nos cellules sont continuellement exposées aux dommages causés par le soleil, les produits chimiques et l’usure normale. Une protéine appelée p53 est célèbre pour décider si une cellule endommagée doit se réparer, cesser de se diviser ou mourir. Lorsque p53 dysfonctionne, des cancers apparaissent souvent. Cette étude utilise la mouche du vinaigre, Drosophila, pour démêler comment différentes versions de p53 poussent les cellules soit vers une autodestruction protectrice, soit vers un état dangereux favorisant les tumeurs. Comme p53 des mouches et des humains sont étonnamment similaires, ces résultats aident à clarifier pourquoi certaines réponses cellulaires aux dommages préviennent le cancer tandis que d’autres peuvent, discrètement, l’alimenter.
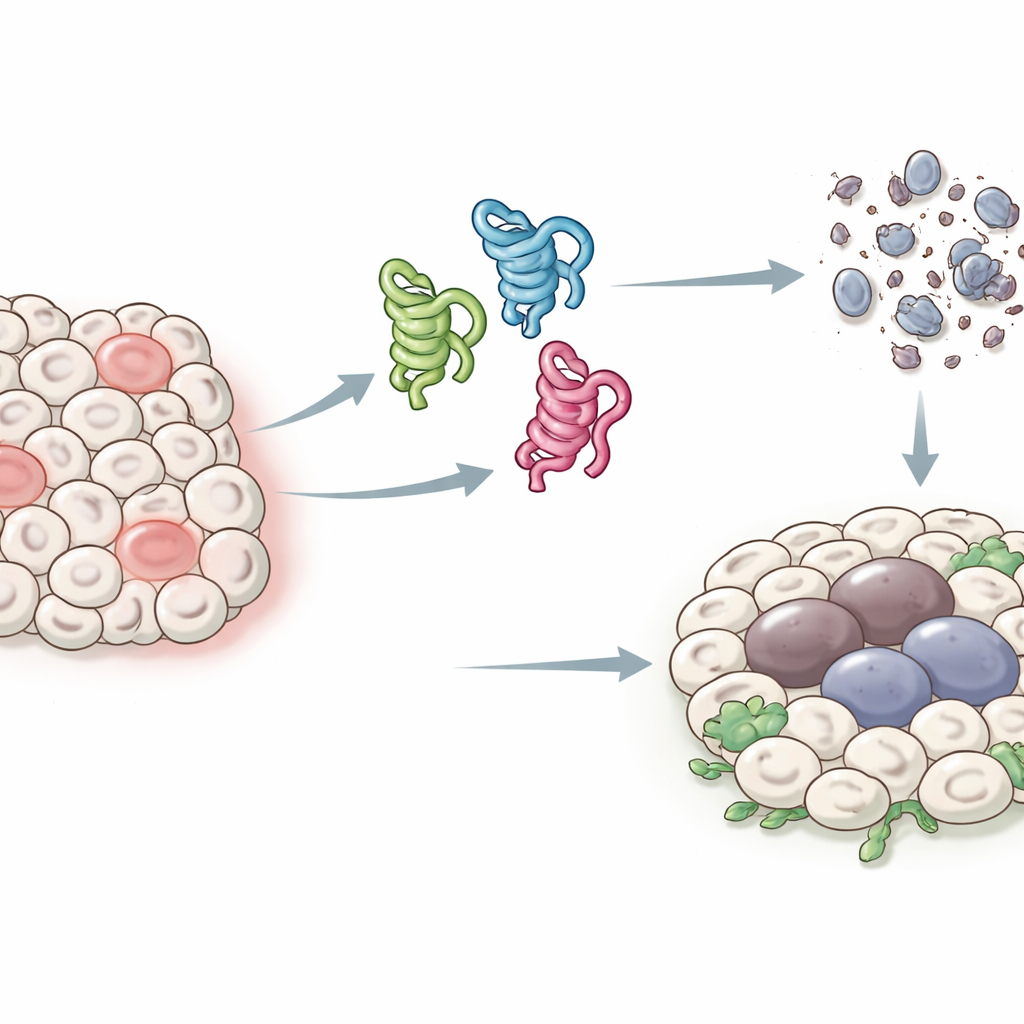
Les visages différents d’une protéine sentinelle
Chez l’humain, le gène p53 peut produire au moins une douzaine de formes protéiques légèrement différentes, ou isoformes, ce qui complique l’identification du rôle de chacune. Les mouches ont une organisation plus simple : un seul gène p53 qui produit seulement trois isoformes principales, appelées p53-A, p53-B et p53-E. Les trois partagent une région centrale capable de se lier à l’ADN, mais diffèrent à leurs extrémités, ce qui modifie leurs interactions avec d’autres protéines. Les auteurs ont tiré parti de ce système simplifié pour exprimer chaque isoforme dans des tissus de la mouche et étudier comment elles influencent deux issues clés après stress ou dommages à l’ADN : la mort cellulaire programmée (apoptose) et un arrêt durable ressemblant au vieillissement cellulaire (sénescence) qui peut promouvoir la croissance tumorale.
Quand la vitesse de division cellulaire change l’issue
L’équipe a d’abord testé si le cycle cellulaire, le rythme de division des cellules, modifie la manière dont chaque isoforme de p53 déclenche l’apoptose. Ils ont forcé les cellules de mouche dans différents états : en division active, bloquées à des phases particulières, ou converties en un mode de croissance qui saute la mitose. Les isoformes p53-A et p53-E se sont comportées comme des décideurs prudents : elles n’induisent fortement l’apoptose que lorsque les cellules sont en cycle actif. Si les cellules étaient arrêtées ou dans un cycle de croissance spécial, leur capacité à déclencher la mort cellulaire disparaissait en grande partie. En revanche, p53-B était beaucoup moins conciliante. Elle induisait une apoptose robuste quel que soit l’état de division des cellules, aussi bien dans les disques imaginales (tissus en développement) que dans les grandes cellules non divisantes des glandes salivaires. Cela montre que la relation entre p53 et le cycle cellulaire n’est pas universelle, mais dépend de l’isoforme.
Un raccourci vers la mort cellulaire qui contourne les gènes
Dans les manuels, p53 classique agit comme un facteur de transcription : il active des gènes tels que reaper et hid qui déclenchent la machinerie de mort cellulaire. Les auteurs ont confirmé que p53-A et p53-E suivent ce scénario. Lorsqu’ils ont bloqué ces gènes pro-mort, l’apoptose provoquée par p53-A et p53-E s’est effondrée. Mais p53-B a enfreint les règles. Même lorsque les principaux gènes pro-apoptotiques étaient supprimés génétiquement, p53-B tuait encore puissamment les cellules. Des expériences détaillées ont expliqué pourquoi : p53-B peut se lier physiquement à Dronc, l’équivalent drosophile d’une caspase « initiatrice » située près du sommet de la cascade de mort. Grâce à des pull-downs biochimiques et à un test avec une protéine fluorescente divisée, ils ont visualisé une interaction spécifique entre p53-B et Dronc à l’intérieur des noyaux cellulaires. Même une version de p53-B dépourvue de son noyau de liaison à l’ADN pouvait activer un capteur spécialement conçu pour Dronc et déclencher l’apoptose, tant que Dronc était présent. Cela révèle une voie directe, indépendante de la transcription, reliant p53-B à la machinerie des caspases.
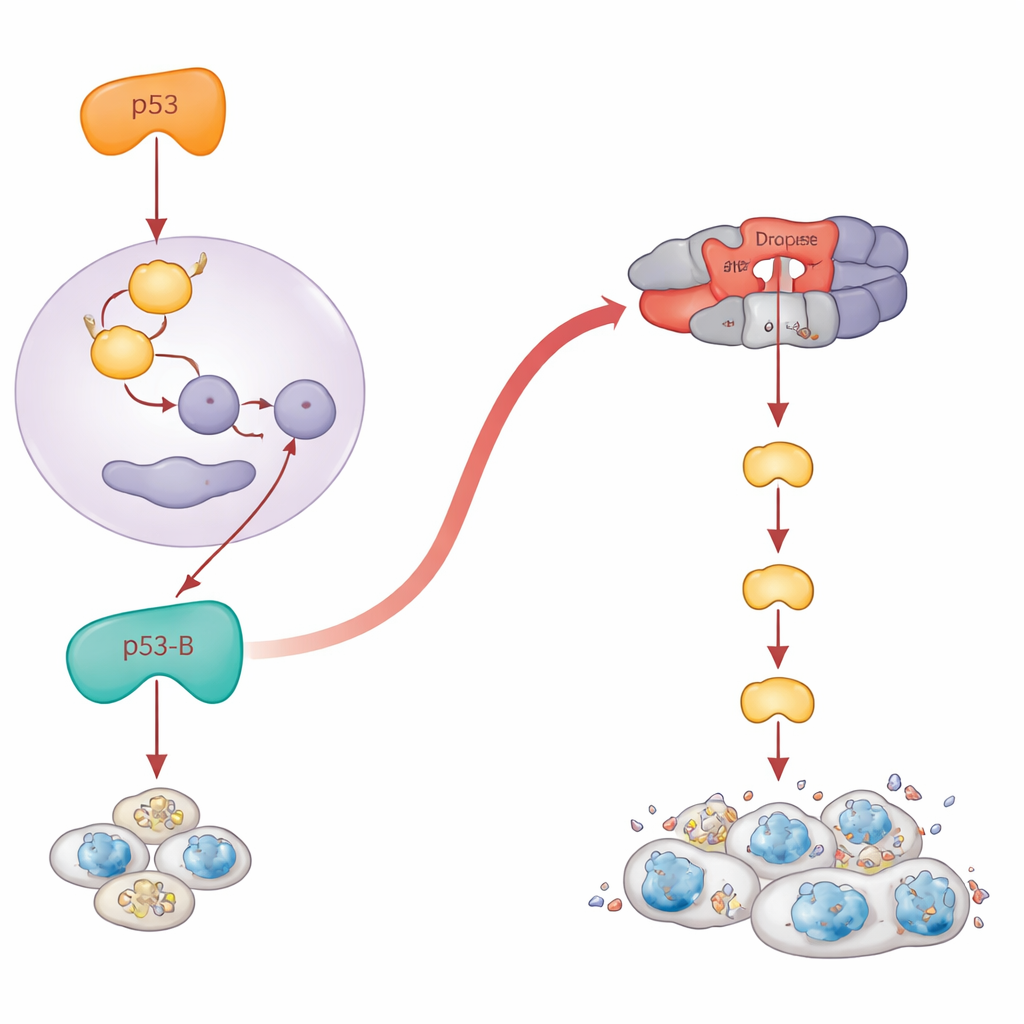
Quand l’échec de la mort devient croissance dangereuse
Paradoxalement, les cellules qui échouent à mourir peuvent devenir longtemps vivantes, enflammées et favoriser les tumeurs. Les auteurs ont examiné ce que fait chaque isoforme de p53 dans des tissus où l’apoptose est bloquée. Ils ont exprimé les isoformes dans l’aile en développement, soit en conditions normales, soit chez des mouches dépourvues des gènes clés de la mort. Lorsque l’apoptose était désactivée, p53-A et p53-E ne réduisaient plus la taille du tissu. Au lieu de cela, elles produisaient des poches de cellules de type sénescentes qui activaient une voie de stress appelée JNK et sécrétaient des signaux de croissance. Ces régions se développaient de manière spectaculaire, formant des structures hypertrophiées semblables à des tumeurs autour des cellules endommagées. Fait frappant, p53-B provoquait aussi ce type de surcroissance, mais seulement lorsque l’apoptose était bloquée en aval au niveau de Dronc ; si les gènes pro-mort en amont étaient désactivés, p53-B parvenait toujours à tuer les cellules et aucune surcroissance n’apparaissait. Pour p53-A et p53-E, l’activation de JNK et la croissance tumorale nécessitaient leur capacité de liaison à l’ADN, alors que p53-B pouvait activer JNK et promouvoir une surcroissance liée à la sénescence même sans liaison à l’ADN, ce qui souligne encore des actions non transcriptionnelles.
Ce que la mouche nous enseigne sur p53 humain
Les chercheurs ont ensuite introduit un isoforme humain de p53 (le TAp53α complet) dans les tissus de la mouche. La p53 humaine s’est comportée en partie comme la p53-A de la mouche : elle tuait principalement les cellules en activant des gènes pro-apoptotiques et dépendait de la caspase initiatrice Dronc. Sa capacité à tuer était réduite, mais pas annulée, lorsque le cycle cellulaire était arrêté, et une version dépourvue du noyau de liaison à l’ADN pouvait encore activer faiblement Dronc directement, suggérant une voie conservationnelle indépendante de la transcription. Cependant, une différence importante est apparue : dans les tissus déficients en apoptose, la p53 humaine ne provoquait pas de surcroissance tumorale. Elle arrêtait plutôt fortement le cycle cellulaire, réduisant la réplication de l’ADN et maintenant la taille tissulaire sous contrôle, à l’image de son rôle bien connu comme frein sur la division cellulaire humaine.
Principaux enseignements
Ce travail montre que les isoformes de p53 n’agissent pas toutes de la même manière. Certaines, comme p53-A et p53-E de la mouche, s’appuient principalement sur l’activation ou la répression de gènes et répondent de façon sensible à l’état de division des cellules. D’autres, comme p53-B, peuvent contourner le contrôle de l’ADN et se raccorder directement à la machinerie de mort, ou à des voies de stress, par des contacts protéine–protéine directs. Dans les tissus sains, ces mécanismes superposés veillent à ce que les cellules endommagées meurent proprement ou entrent dans un état sénescent contenu. Mais lorsque l’apoptose est bloquée, ces mêmes activités de p53 peuvent favoriser des signaux de stress chroniques et la surcroissance tissulaire. En disséquant ces comportements dans un animal simple, l’étude aide à expliquer comment différentes versions de p53 peuvent supprimer les tumeurs dans certains contextes tout en les favorisant dans d’autres, et met en évidence des interactions spécifiques — comme le lien direct entre p53 et les caspases — qui pourraient être des cibles importantes pour de futures thérapies anticancéreuses.
Citation: Pérez-Aguilera, M., Ruiz-Losada, M., Gil Cortes, P. et al. Transcription-dependent and -independent functions of Drosophila p53 isoforms in the induction of apoptosis and senescence-associated tumorigenesis. Cell Death Dis 17, 367 (2026). https://doi.org/10.1038/s41419-026-08571-x
Mots-clés: isoformes de p53, apoptose, sénescence cellulaire, modèles Drosophila, tumorigénèse