Clear Sky Science · sv
Transkriptionsberoende och -oberoende funktioner hos Drosophila p53-isoformer vid induktion av apoptos och senescensassocierad tumörbildning
Varför den här studien är viktig
Våra celler utsätts ständigt för skador från solljus, kemikalier och normalt slitage. Ett protein kallat p53 är välkänt för att avgöra om en skadad cell ska reparera sig, sluta dela sig eller dö. När p53 fungerar felaktigt uppstår ofta cancer. Denna studie använder fruktflugan Drosophila för att reda ut hur olika versioner av p53 driver celler antingen mot säker självdöd eller mot ett farligt, tumörfrämjande tillstånd. Eftersom flugans och människans p53 är förvånansvärt lika, hjälper dessa fynd att klargöra varför vissa cellreaktioner på skada förhindrar cancer medan andra kan underhålla den i det tysta.
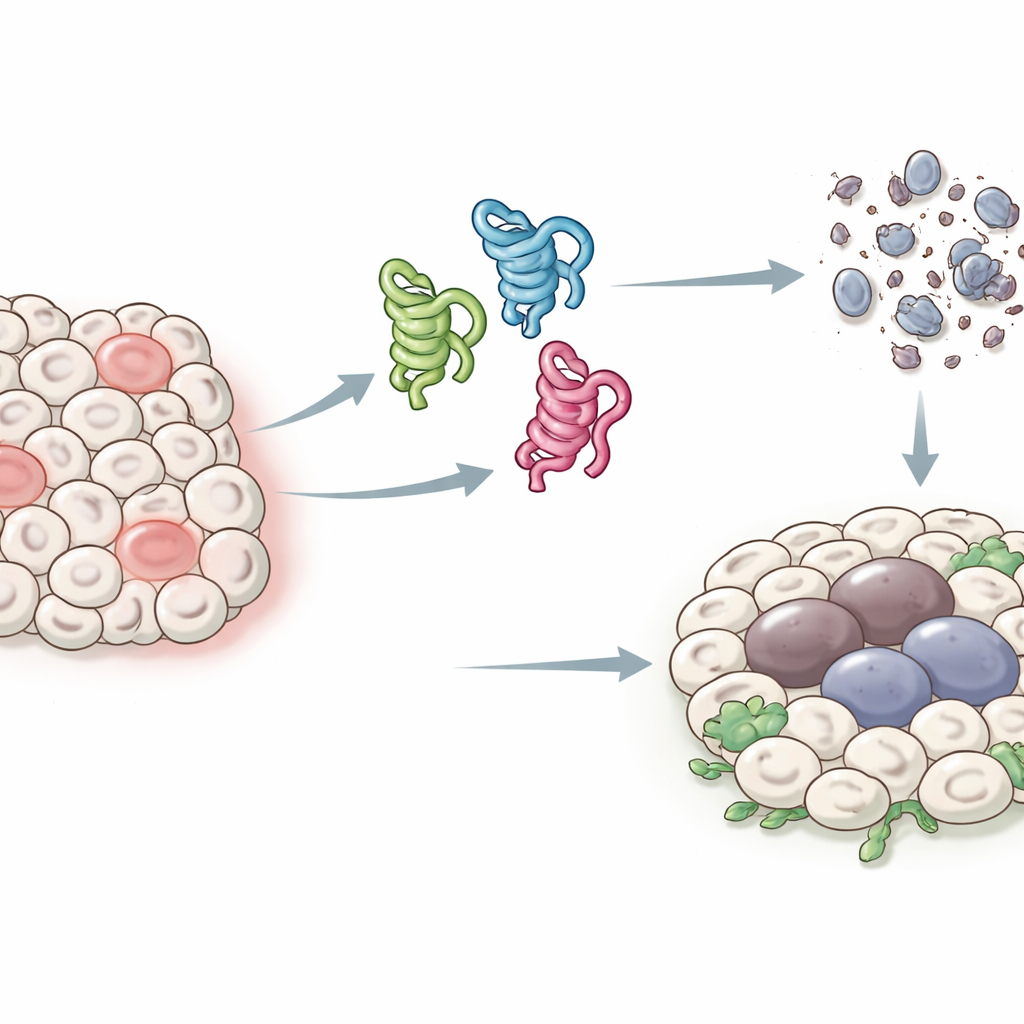
En väktarproteins olika ansikten
I människan kan p53-genen ge upphov till minst ett dussin något olika proteinformer, eller isoformer, vilket har gjort det svårt att precisera vad var och en gör. Fruktflugor har en enklare uppsättning: en enda p53-gen som gör bara tre huvudisoformer, kallade p53-A, p53-B och p53-E. Alla tre delar en kärnregion som kan binda DNA, men de skiljer sig vid sina ändar, vilket förändrar hur de interagerar med andra proteiner. Författarna utnyttjade detta strömlinjeformade system för att uttrycka varje isoform i specifika flugvävnader och undersöka hur de påverkar två nyckelutfall efter stress eller DNA-skada: programmerad celldöd (apoptos) och ett långvarigt arresterat tillstånd som liknar cellulär åldrande (senescens) och som kan främja tumörtillväxt.
När celldelningens hastighet ändrar utgången
Gruppen testade först om cellcykeln, rytmen för celldelning, förändrar hur varje p53-isoform utlöser apoptos. De tvingade flugceller till olika tillstånd: aktivt delande, pausade i särskilda faser eller omställda till ett tillväxtmönster som hoppar över mitos. Isoformerna p53-A och p53-E uppträdde som försiktiga beslutsfattare: de kunde starkt inducera apoptos endast när cellerna var i aktiv cykling. Om cellerna var arresterade eller i ett särskilt tillväxtcykel försvann deras förmåga att utlösa celldöd i stor utsträckning. I kontrast var p53-B mycket mer kompromisslöst. Den drev robust apoptos oavsett om cellerna delade sig eller inte, både i imaginalskivor (utvecklande vävnader) och i stora, icke-delande spottkörtelceller. Detta visade att relationen mellan p53 och cellcykeln inte är universell utan isoformsspecifik.
En genväg till celldöd som kringgår gener
Det klassiska p53 fungerar som en transkriptionsfaktor: det slår på gener såsom reaper och hid som sätter igång cellens dödsmaskineri. Författarna bekräftade att p53-A och p53-E följer detta manus. När de blockerade dessa pro-dödsgener kollapsade apoptosen orsakad av p53-A och p53-E. Men p53-B bröt mot reglerna. Även när de viktigaste pro-apoptotiska generna genetiskt togs bort, dödade p53-B fortfarande kraftfullt celler. Detaljerade experiment visade varför: p53-B kan fysiskt binda till Dronc, flugans motsvarighet till en ”initierande” kaspas som sitter nära toppen av dödskaskaden. Genom biokemiska pull-downs och ett delat fluorescerande proteinprov visade de en specifik interaktion mellan p53-B och Dronc inne i cellkärnorna. Även en version av p53-B utan sin DNA-bindande kärna kunde fortfarande aktivera en specialkonstruerad Dronc-sensor och utlösa apoptos, förutsatt att Dronc var närvarande. Detta avslöjar en direkt, transkriptionsoberoende väg från p53-B till kaspasmaskineriet.
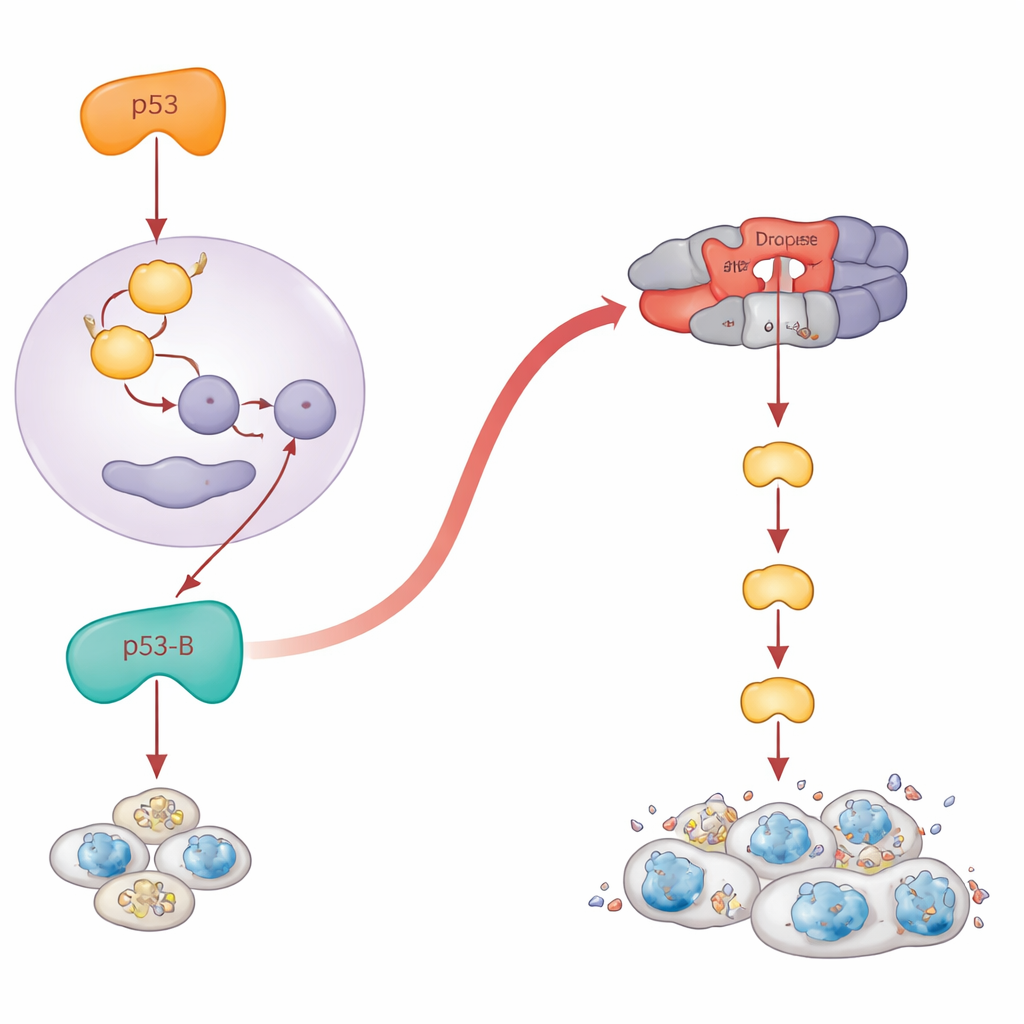
När misslyckad död blir farlig tillväxt
Paradoxalt nog kan celler som misslyckas med att dö bli långlivade, inflammerade och tumörfrämjande. Författarna undersökte vad varje p53-isoform gör i vävnader där apoptos är blockerad. De uttryckte isoformerna i den utvecklande vingen, antingen under normala förhållanden eller i flugor som saknar nyckelgener för död. När apoptos var inaktiverad krympte p53-A och p53-E inte längre vävnaden. Istället producerade de fickor av senescensliknande celler som aktiverade en stressväg kallad JNK och utsöndrade tillväxtsignaler. Dessa regioner expanderade dramatiskt och bildade överväxta, tumörlika strukturer runt de skadade cellerna. Slående nog drev p53-B också denna typ av överväxt, men endast när apoptosen var blockerad nedströms på nivån av Dronc; om de tidigare pro-dödsgenerna var inaktiverade lyckades p53-B fortfarande döda celler och ingen överväxt uppträdde. För p53-A och p53-E krävde aktiveringen av JNK och tumörtillväxt deras DNA-bindande förmåga, medan p53-B kunde aktivera JNK och främja senescenskopplad överväxt även utan DNA-bindning, vilket återigen pekar på icke-transkriptionella funktioner.
Vad flugan lär oss om mänskligt p53
Forskarna introducerade sedan en mänsklig p53-isoform (fullängds TAp53α) i flugvävnader. Mänskligt p53 uppträdde delvis som flugans p53-A: det dödade främst celler genom att slå på pro-apoptotiska gener och behövde den initierande kaspasen Dronc. Dess dödskraft minskade, men upphörde inte, när cellcykeln stoppades, och en version utan den DNA-bindande kärnan kunde fortfarande svagt aktivera Dronc direkt, vilket antyder en bevarad transkriptionsoberoende väg. Det fanns dock en viktig skillnad: i apoptosdefekt vävnad drev inte mänskligt p53 tumörlik överväxt. Istället orsakade det en kraftig cellcykelarrest, minskad DNA-replikation och höll vävnadsstorleken i schack, mycket likt dess välkända roll som broms för mänsklig celldelning.
Stora slutsatser
Detta arbete visar att inte alla p53-isoformer agerar likadant. Vissa, som flugp53-A och p53-E, förlitar sig huvudsakligen på att slå på eller av gener och svarar känsligt på om celler delar sig. Andra, som p53-B, kan kringgå DNA-kontrollen helt och hållet och koppla direkt in i kärndödsmaskineriet eller i stressvägar genom direkt protein–protein-interaktioner. I friska vävnader hjälper dessa flerskiktade mekanismer att säkerställa att skadade celler antingen dör rent eller går in i ett kontrollerat, senescent tillstånd. Men när apoptos blockeras kan exakt samma p53-aktiviteter främja kronisk stresssignalering och vävnadsöverväxt. Genom att dissekera dessa beteenden i ett enkelt djur bidrar studien till att förklara hur olika p53-versioner kan undertrycka tumörer i vissa sammanhang men främja dem i andra, och den lyfter fram specifika interaktioner — såsom den direkta länken mellan p53 och kaspaser — som kan vara viktiga mål för framtida cancerterapier.
Citering: Pérez-Aguilera, M., Ruiz-Losada, M., Gil Cortes, P. et al. Transcription-dependent and -independent functions of Drosophila p53 isoforms in the induction of apoptosis and senescence-associated tumorigenesis. Cell Death Dis 17, 367 (2026). https://doi.org/10.1038/s41419-026-08571-x
Nyckelord: p53-isoformer, apoptos, cellsenesens, Drosophila-modeller, tumörbildning