Clear Sky Science · nl
Transcriptie-afhankelijke en -onafhankelijke functies van Drosophila p53-isoformen bij de inductie van apoptose en senescentie-geassocieerde tumorgroei
Waarom deze studie ertoe doet
Onze cellen worden voortdurend blootgesteld aan schade door zonlicht, chemicaliën en normale slijtage. Een eiwit genaamd p53 is beroemd omdat het beslist of een beschadigde cel zichzelf moet repareren, stoppen met delen of moet sterven. Wanneer p53 fout gaat, ontstaan vaak kankers. Deze studie gebruikt de vruchtvlieg, Drosophila, om uit te zoeken hoe verschillende versies van p53 cellen aanzetten tot ofwel veilige zelfvernietiging, of tot een gevaarlijke, tumorgunstige toestand. Omdat vlieg- en humane p53 verrassend veel overeenkomsten vertonen, helpen deze bevindingen verklaren waarom sommige celreacties op schade kanker voorkomen terwijl andere deze juist stilletjes kunnen aanjagen.
Verschillende gezichten van een beschermend eiwit
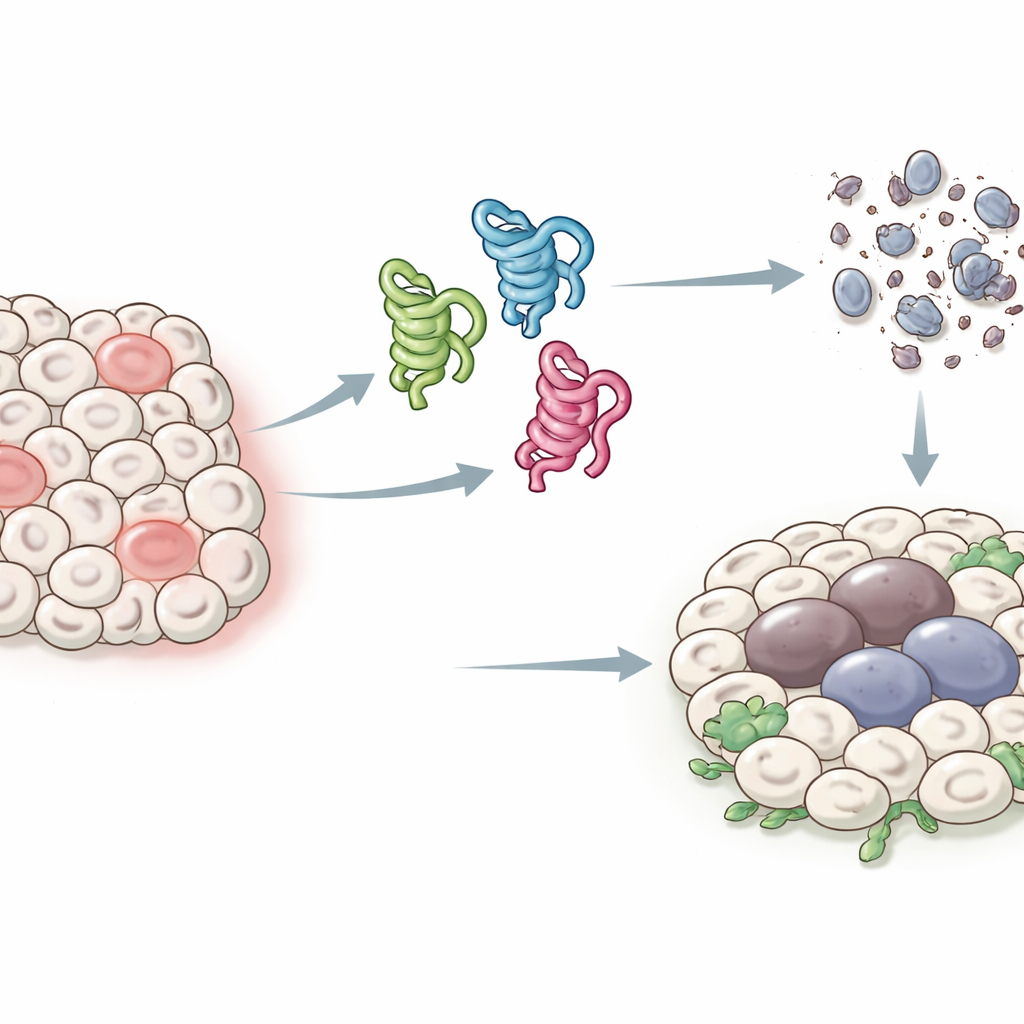
Bij mensen kan het p53-gen minstens een dozijn licht verschillende eiwitvormen produceren, of isoformen, wat het moeilijk heeft gemaakt om precies vast te stellen wat ieder van hen doet. Vruchtvliegen hebben een eenvoudiger systeem: één p53-gen dat slechts drie hoofdisoformen maakt, genoemd p53-A, p53-B en p53-E. Alle drie delen ze een kernregio die aan DNA kan binden, maar ze verschillen aan hun uiteinden, wat verandert hoe ze met andere eiwitten interageren. De auteurs maakten gebruik van dit gestroomlijnde systeem om elke isoform in specifieke vliegweefsels tot expressie te brengen en te onderzoeken hoe ze twee belangrijke uitkomsten na stress of DNA-schade beïnvloeden: geprogrammeerde celdood (apoptose) en een langdurige stilstandstoestand die op cellulaire veroudering lijkt (senescentie) en die tumorgroei kan bevorderen.
Wanneer de snelheid van celdeling de uitkomst verandert
Het team testte eerst of de celcyclus, het ritme van celdeling, verandert hoe elke p53-isoform apoptose opwekt. Ze dwongen vliegcelllen in verschillende toestanden: actief delend, gepauzeerd in bepaalde fasen, of overgeschakeld naar een groeipatroon dat mitose overslaat. Isoformen p53-A en p53-E gedroegen zich als voorzichtige beslissers: ze konden sterk apoptose induceren alleen wanneer cellen actief deelden. Als de cellen waren gestopt of in een speciale groeicyclus zaten, verdween hun vermogen om celdood te veroorzaken grotendeels. In tegenstelling daarmee was p53-B veel onverbiddelijker. Het dreef krachtige apoptose aan ongeacht of cellen deelden of niet, zowel in imaginale schijven (ontwikkelende weefsels) als in grote, niet-delende speekselkliercellen. Dit toonde aan dat de relatie tussen p53 en de celcyclus niet universeel is, maar isoformspecifiek.
Een snelkoppeling naar celdood die genen omzeilt
Het klassieke p53 uit leerboeken fungeert als transcriptiefactor: het zet genen aan zoals reaper en hid die het doodsmachinery van de cel in gang zetten. De auteurs bevestigden dat p53-A en p53-E dit script volgen. Wanneer ze deze pro-apoptotische genen blokkeerden, viel de door p53-A en p53-E veroorzaakte apoptose weg. Maar p53-B brak de regels. Zelfs wanneer de belangrijkste pro-apoptotische genen genetisch werden verwijderd, doodde p53-B nog steeds krachtig cellen. Gedetailleerde experimenten toonden waarom: p53-B kan fysiek binden aan Dronc, het vlieg-equivalent van een ‘initiator’ caspase dat hoog in de doodcascade zit. Met biochemische pull-downs en een split-fluorescent eiwitassay visualiseerden ze een specifieke interactie tussen p53-B en Dronc binnen celnucleï. Zelfs een versie van p53-B die was gestript van zijn DNA-bindende kern kon nog steeds een speciaal ontworpen Dronc-sensor activeren en apoptose veroorzaken, zolang Dronc zelf aanwezig was. Dit onthult een directe, transcriptie-onafhankelijke route van p53-B naar het caspase-machinerie.
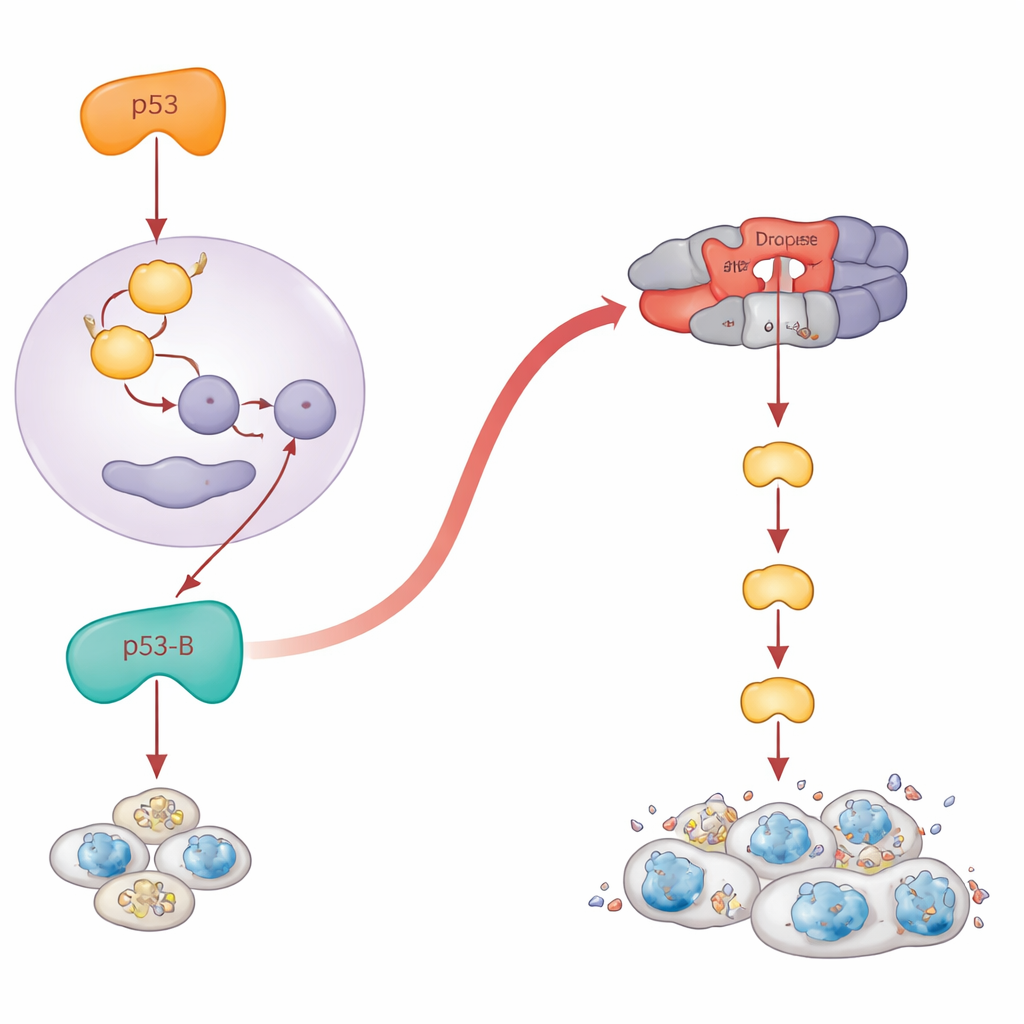
Wanneer mislukte dood verandert in gevaarlijke groei
Paradoxaal genoeg kunnen cellen die er niet in slagen te sterven langlevend, ontstoken en tumorgunstig worden. De auteurs vroegen wat elke p53-isoform doet in weefsels waar apoptose is geblokkeerd. Ze brachten de isoformen tot expressie in de ontwikkelende vleugel, zowel onder normale omstandigheden als in vliegen die sleutelgenen voor celdood misten. Wanneer apoptose was uitgeschakeld, verkleinden p53-A en p53-E het weefsel niet langer. In plaats daarvan produceerden ze pockets van senescentie-achtige cellen die een stressroute genaamd JNK inschakelden en groeisignalen uitscheiden. Deze regio’s breidden dramatisch uit en vormden overgroeide, tumorachtige structuren rond de beschadigde cellen. Opmerkelijk genoeg dreef p53-B ook dit soort overgroei aan, maar alleen wanneer apoptose was geblokkeerd downstream op het niveau van Dronc; als de eerdere pro-dood genen waren uitgeschakeld, slaagde p53-B er nog steeds in cellen te doden en trad er geen overgroei op. Voor p53-A en p53-E vereiste het inschakelen van JNK en tumorgroei hun DNA-bindende capaciteit, terwijl p53-B JNK kon activeren en senescentie-geassocieerde overgroei bevorderen zelfs zonder aan DNA te binden, wat opnieuw wijst op niet-transcriptionele acties.
Wat de vlieg ons leert over menselijk p53
De onderzoekers introduceerden vervolgens een menselijke p53-isoform (de volledige TAp53α) in vliegweefsels. Menselijk p53 gedroeg zich deels als vlieg p53-A: het doodde vooral cellen door pro-apoptotische genen aan te zetten en had de initiatorcaspase Dronc nodig. Zijn dodelijke kracht werd verminderd, maar niet opgeheven, wanneer de celcyclus werd stilgelegd, en een versie zonder de DNA-bindende kern kon nog zwak Dronc rechtstreeks activeren, wat wijst op een geconserveerde transcriptie-onafhankelijke route. Er was echter een belangrijk verschil: in apoptose-deficiënte weefsels dreef menselijk p53 geen tumorachtige overgroei aan. In plaats daarvan zette het sterk de celcyclus stop, verminderde DNA-replicatie en hield de weefselgrootte onder controle, net zoals zijn bekende rol als rem op menselijke celdeling.
Belangrijkste conclusies
Dit werk toont aan dat niet alle p53-isoformen hetzelfde doen. Sommige, zoals vlieg p53-A en p53-E, vertrouwen voornamelijk op het in- of uitschakelen van genen en reageren gevoelig op of cellen delen. Andere, zoals p53-B, kunnen DNA-controle geheel omzeilen en zich rechtstreeks aansluiten op de kern van de doodsmachinerie, of op stressroutes, via directe eiwit‑eiwitcontacten. In gezonde weefsels helpen deze gelaagde mechanismen ervoor te zorgen dat beschadigde cellen ofwel netjes sterven of in een ingeperkte, senescente staat terechtkomen. Maar wanneer apoptose is geblokkeerd, kunnen precies diezelfde p53-activiteiten chronische stresssignalisatie en weefselovergroei bevorderen. Door deze gedragingen in een eenvoudig dier te ontleden, helpt de studie verklaren hoe verschillende p53-versies in sommige contexten tumoren kunnen onderdrukken, terwijl ze in andere contexten juist kunnen bevorderen, en het benadrukt specifieke interacties — zoals de directe link tussen p53 en caspases — die belangrijke doelen kunnen zijn voor toekomstige kankertherapieën.
Bronvermelding: Pérez-Aguilera, M., Ruiz-Losada, M., Gil Cortes, P. et al. Transcription-dependent and -independent functions of Drosophila p53 isoforms in the induction of apoptosis and senescence-associated tumorigenesis. Cell Death Dis 17, 367 (2026). https://doi.org/10.1038/s41419-026-08571-x
Trefwoorden: p53-isoformen, apoptose, celsenescentie, Drosophila-modellen, tumorigenese