Clear Sky Science · tr
NLRP3 inflammasomunun etkinleşmesinin moleküler mekanizmaları
Hücrelerimiz Moleküler Bir Yangın Alarmını Neden Tetikler
Vücudumuz, önde gelen bağışıklık hücrelerine; istilacı mikropları, toksik parçacıkları veya içsel stresi fark etmeleri ve hızlıca alarm vermeleri görevini verir. En güçlü alarm anahtarlarından biri NLRP3 inflammasomu adı verilen bir protein makinesidir. Bu anahtar aktive olduğunda, bizi enfeksiyondan koruyabilecek bir inflamasyon başlatır. Ancak bu anahtar “açık” pozisyonda takılı kalırsa gut ve diyabetten nörodejenerasyona kadar uzun bir hastalık listesini tetikleyebilir. Bu derleme makalesi, NLRP3 inflammasomunun nasıl inşa edildiğini, nelerin onu açtığını ve hücrelerin aktivitesini nasıl hassas biçimde ayarladığını moleküler ayrıntılarla açıklayarak, yararlı savunmaları susturmadan zararlı iltihabı soğutacak gelecekteki ilaçlara ipuçları sunar.
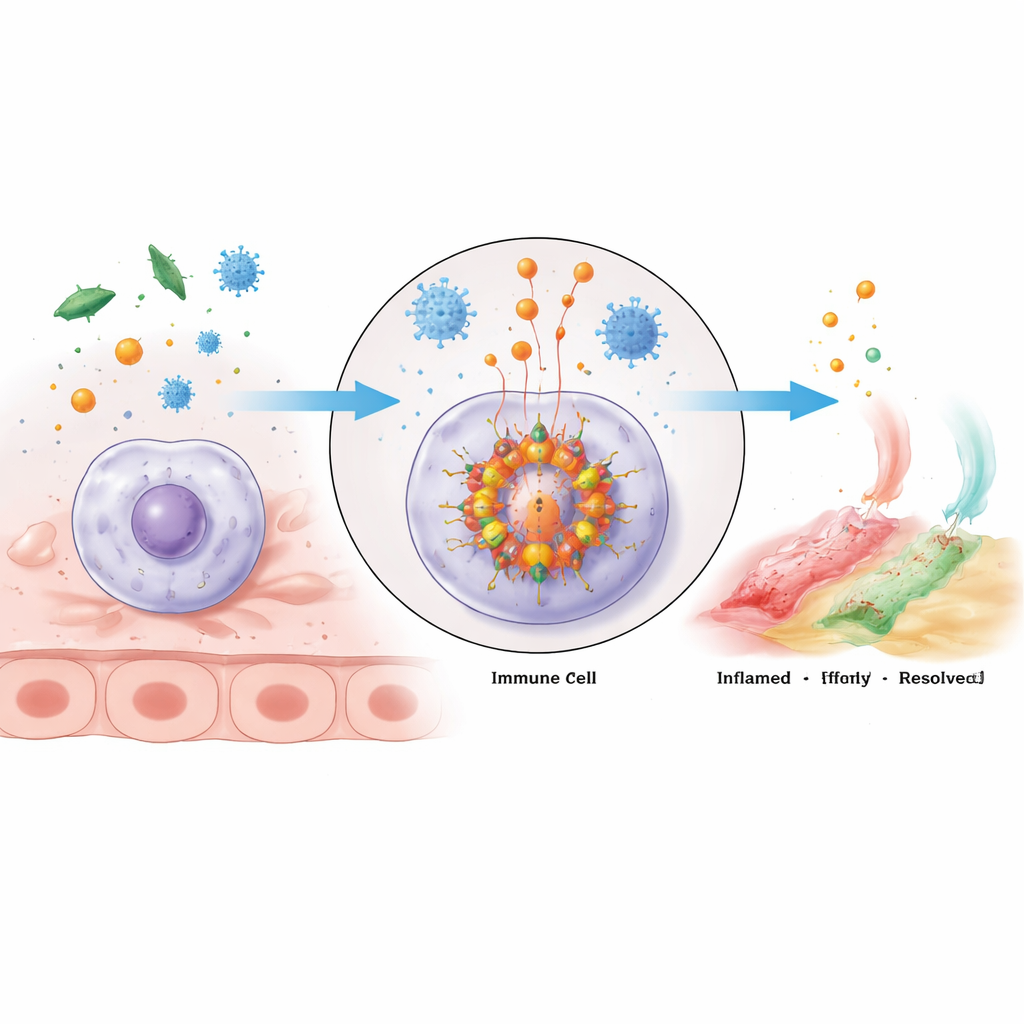
Bağışıklık Hücreleri İçinde Moleküler Bir Alarm Kümesi
NLRP3 inflammasomu, tehlike algılandığında bağışıklık hücreleri içinde bir araya gelen büyük bir çok proteinli kümedir. Çekirdeğini sensör proteini NLRP3, ASC adlı bir adaptör ve enzim caspase‑1 oluşturur. NLRP3'ün farklı görevleri olan birkaç bölgesi vardır: bir ucu ASC'ye bağlanır, orta kısmı enerji açısından zengin ATP'ye bağlanır ve NLRP3 birimlerinin kümeleşmesine yardımcı olur, kuyruk ise sensörü tehlike ortaya çıkana kadar kapalı tutmaya yardımcı olur. Aktive olduğunda NLRP3 molekülleri oligomerize—grup oluşturarak birleşir—ve ASC'yi çekerek filament benzeri iskeletler oluşturur; bunlar da caspase‑1'i içine çeker. Bir kez kümelendiğinde caspase‑1 aktive olur ve güçlü iltihap vericiler olan IL‑1β ve IL‑18'in inaktif öncüllerini, ayrıca hücre zarında delikler açabilen gasdermin D adlı proteini keser; bu, sıklıkla ölümcül olabilen şiddetli bir inflamatuar yanıt olan piroptozise yol açar.
İki Yeşil Işık: Hazırlık ve Ateşleme
NLRP3'ün açılması tek bir olay değildir; iki aşamalı bir süreçtir. Birinci aşama, priming (hazırlık) olarak adlandırılır ve mikropları veya inflamatuar hormonları algılayan reseptörler etkinleştirildiğinde oluşur. Bu sinyaller, NLRP3'ün kendisinin ve inaktif sitokin öncülleri IL‑1β ile IL‑18'in üretimini artıran transkripsiyon faktörü NF‑κB'yi aktive eder. Aynı zamanda fosfat, ubiquitin, SUMO, asetil, lipid veya ADP‑riboz gibi grupların eklenmesi veya çıkarılması gibi post‑translasyonel modifikasyonlardan oluşan bir kimyasal ağ NLRP3'e “izin” verir; bunu tehlike potansiyeline sahip ama henüz tehlikeli olmayan bir durumda konumlandırır. İkinci aşama olan aktivasyon ise hücre dışı ATP, bakteriyel toksinler, silika veya ürik asit gibi iğne benzeri kristaller, mitokondriyal stres, lizozomal yırtılma ve daha fazlası gibi çok çeşitli uyarıcılarla tetiklenir. Bu çeşitli tetikleyiciler, özellikle membran boyunca iyon hareketleri, mitokondriyal disfonksiyon ve iç bölümlerdeki hasar gibi ortak hücresel değişikliklerde birleşir; bunlar inflammasom kompleksinin fiziksel olarak toplanmasını ve caspase‑1'in tam aktivasyonunu sağlar.
İyonlar, Enerji Santralleri ve Geri Dönüşüm Merkezleri Hikâyeye Katılıyor
NLRP3 birçok farklı tehdide yanıt verse de, birkaç temel süreç sürekli ortaya çıkar. Bunlardan biri yüklü iyonların akışıdır. Hücreden potasyum kaybı en tutarlı aktivatördür; sodyum, klorür ve kalsiyum hareketleri de özel kanallar aracılığıyla buna yardımcı olur veya modüle eder. Diğeri mitokondriyal stres olup, hasar görmüş “enerji santralleri” reaktif oksijen türleri ve mitokondriyal DNA parçacıkları salar; bunlar NLRP3'ü toplayıp aktive etmeye yardımcı olur ve metformin gibi ilaçlar bu mitokondriyal sinyali azaltabilir. Üçüncüsü lizozomal hasardır; hücreler keskin parçacıkları yuttuğunda bu geri dönüşüm merkezlerinin yırtılması enzimler ve iyonlar salgılar ve bu da NLRP3 aktivasyonunu daha da destekler. Bu arada hücresel metabolizmanın—hücrelerin glukozu, yağları ve diğer yakıtları nasıl yaktığının—değişmesi inflammasom aktivitesini hızlandırabilir veya frenleyebilir; sukkinat ve palmitat gibi bazı metabolitler inflamasyonu tetiklerken, itakonat, fumarat veya keton cisimleri gibi diğerleri bunu sınırlar.
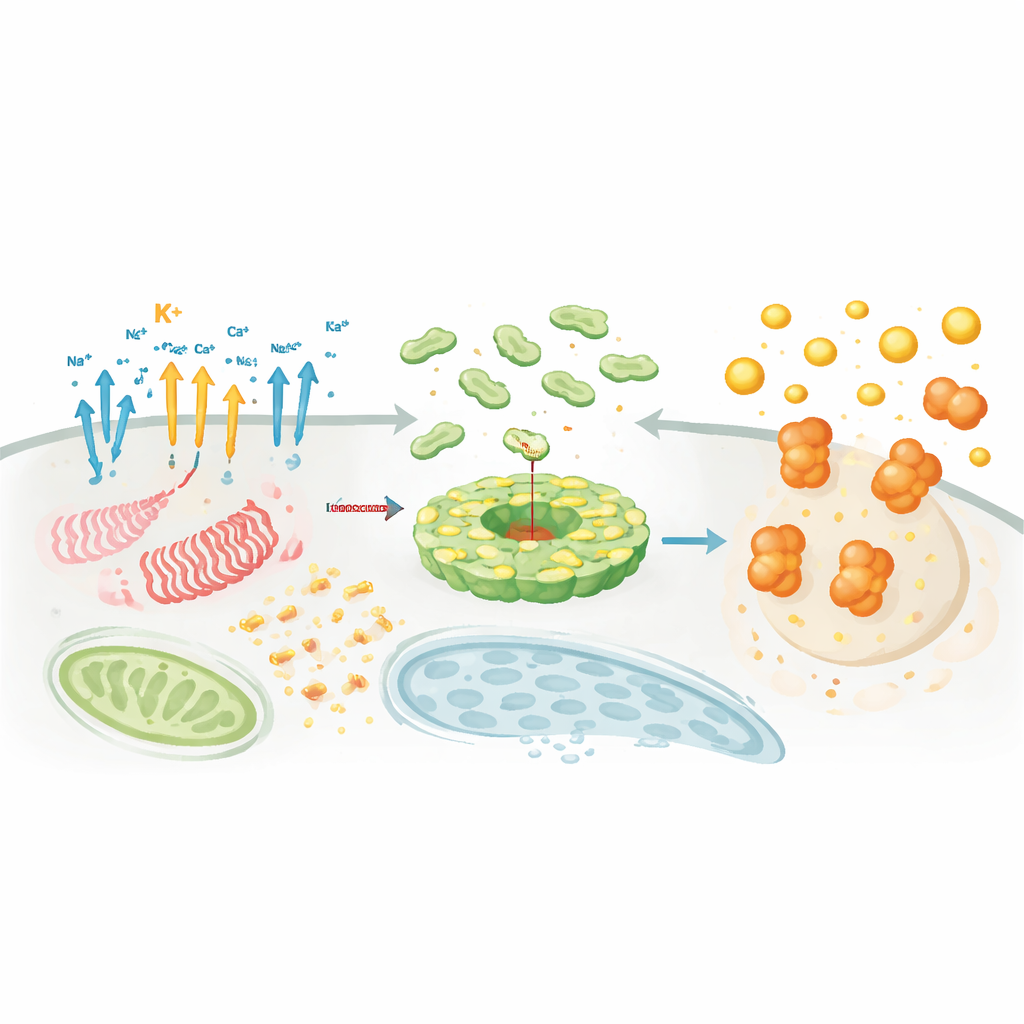
Kompleks Nerede ve Ne Zaman Birikir
Kimyasal sinyallerin ötesinde, yer ve zamanlama da kritiktir. NLRP3 ve ortakları organeller arasında hareket eder, hücrenin iç iskeleti boyunca yol alarak trans‑Golgi ağı ve mikrotübül organize edici merkez gibi belirli merkezlerde toplanır. Orada NEK7 gibi yardımcı proteinler, NLRP3'ü oto‑inhibitli kafesten ASC'ye bağlanabilen aktif bir diske dönüştüren “izin faktörleri” görevi görür. Palmitoilasyon gibi lipid modifikasyonları ve belirli membran lipidleriyle elektrostatik etkileşimler NLRP3'ü doğru zaman ve yere yönlendirir. Bu koreografiyle paralel olarak, düzinece enzim düzenleyici etiketler—ubiquitin zincirleri, fosfat grupları, asetil işaretleri ve SUMO proteinleri—ekler veya çıkarır; bunlar NLRP3 miktarını, stabilitesini ve ASC ile caspase‑1 ile birleşme yeteneğini ince şekilde ayarlar. Bu yoğun düzenleyici ağ, NLRP3'ün bağlama bağlamına, hücre tipine ve hastalık durumuna son derece duyarlı olmasını açıklar.
Yardım ve Zararı Dengelemek
Aşırı aktif bir inflammasom enfeksiyon kadar tehlikeli olabileceğinden hücreler aynı zamanda frenler de konuşlandırır. Birçok protein, NLRP3 veya ortak faktörlerine bağlanarak kilit etkileşimleri engeller, onları parçalanma yoluna yönlendirir veya kümelenmelerini önler; diğerleri ise gerçek tehditte montajını artırır. Derleme, bu pozitif ve negatif ortakları kataloglar ve çok fazla aktivasyon modifikasyonu ya da yetersiz inhibisyon gibi ince kusurların sistemi kronik inflamasyona itebileceğini gösterir. Yazarlar, bu tüm anahtarların nasıl etkileştiğini anlamanın tedaviler geliştirmenin temelinde olacağını savunuyor. NLRP3 veya yardımcılarını modifiye eden belirli enzimleri hedefleyerek, gelecekteki ilaçlar inflammasomu belirli dokularda veya hastalıklarda seçici biçimde soğutabilir; böylece konak savunmasında hayat kurtarıcı rolünü korurken pek çok inflamatuar ve dejeneratif bozuklukta görülen yan hasarı önleyebilirler.
Atıf: Shin, H.J., Kim, I.S., Kim, J.K. et al. Molecular mechanisms of NLRP3 inflammasome activation. Exp Mol Med 58, 650–663 (2026). https://doi.org/10.1038/s12276-026-01656-9
Anahtar kelimeler: NLRP3 inflammasom, doğuştan gelen bağışıklık, inflamasyon, post-translasyonel modifikasyon, immunometabolizma