Clear Sky Science · ar
الآليات الجزيئية لتنشيط مجمع الإنفلاماسوم NLRP3
لماذا تضيء خلايانا إنذارًا جزيئيًا
تعتمد أجسامنا على خلايا مناعية خط المواجهة لاكتشاف الخطر — ميكروبات غازية، جزيئات سامة، أو ضغوط داخلية — وإطلاق الإنذار بسرعة. أحد أقوى مفاتيح الإنذار هو آلة بروتينية تسمى مجمع الإنفلاماسوم NLRP3. عند تشغيله، يُطلق التهابًا قد ينقذنا من العدوى. لكن إذا ظل هذا المفتاح في وضع "تشغيل" فقد يسبب أمراضًا عديدة، من النقرس والسكري إلى التنكس العصبي. تشرح هذه المقالة الاستعراضية، بتفاصيل جزيئية، كيف يُبنى مجمع NLRP3 وما الذي يشغله، وكيف تضبط الخلايا نشاطه بدقة، موفِّرة دلائل لتطوير أدوية مستقبلية تُبرد الالتهاب الضار دون أن تُقمع الدفاعات المفيدة.
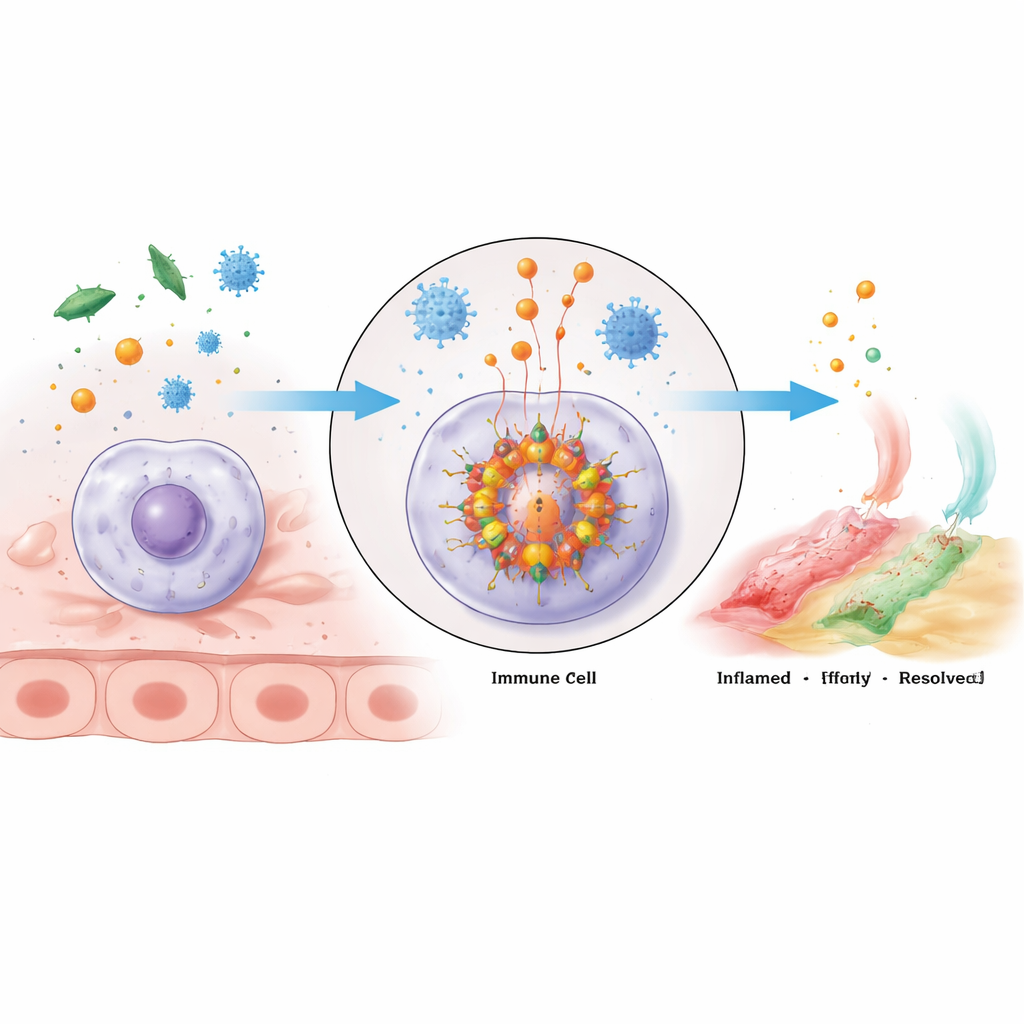
عنقود إنذار جزيئي داخل الخلايا المناعية
مجمع الإنفلاماسوم NLRP3 هو عنقود بروتيني متعدد الوحدات يتجمع داخل الخلايا المناعية عند اكتشافها للخطر. يتألف جوهره من بروتين المستشعر NLRP3، ومُحوِّل يُدعى ASC، والإنزيم كاسبيز‑1. يمتلك NLRP3 عدة مناطق ذات وظائف مميزة: أحد الأطراف يتصل بـASC، والوسط يرتبط بجزيئات ATP الغنية بالطاقة ويساعد وحدات NLRP3 على التجمع، والذيل يساهم في إبقاء المستشعر في وضع الإيقاف حتى يظهر الخطر. عند التنشيط، تتألف جزيئات NLRP3 — تتجمع — وتجذب ASC الذي يشكل هياكل شُعَيْرَية تُجتذب إليها كاسبيز‑1. وبمجرد تجمعها، ينشط كاسبيز‑1 ويقطع السلفيات غير النشطة للمرسلات الالتهابية القوية IL‑1β وIL‑18، وكذلك بروتينًا يسمى غاسدرمين D يمكنه إحداث ثقوب في غشاء الخلية، مسببًا استجابة التهابية محرقة وغالبًا مميتة تُعرف بالبيروبتوزيس.
إشارتان خضراوان: التحضير والإطلاق
تشغيل NLRP3 ليس حدثًا واحدًا بل عملية من خطوتين. الخطوة الأولى، المسماة التمهيد، تحدث عندما تُفعَّل مستقبلات تستشعر الميكروبات أو هرمونات الالتهاب. تفعّل هذه الإشارات عامل النسخ NF‑κB، الذي يعزز إنتاج NLRP3 نفسه وسلفيات السيتوكينات غير النشطة IL‑1β وIL‑18. في الوقت نفسه، شبكة من التعديلات الكيميائية المسماة التعديلات بعد الترجمة — مثل إضافة أو إزالة مجموعات الفوسفات، الأوبيكويتين، SUMO، الأسيل، الشحميات، أو ADP‑ريبوز — "ترخّص" NLRP3، واضعة إياه في حالة جاهزة لكنها ليست خطيرة بعد. الخطوة الثانية، التنشيط، تُثار بواسطة طيف واسع من المحفزات: ATP خارج الخلية، سموم بكتيرية، بلورات إبرية مثل السيليكا أو حمض البوليك، إجهاد الميتوكوندريا، تمزق الليزوزوم، والمزيد. تتقاطع هذه المحفزات المتنوعة عند تغييرات خلوية مشتركة — خصوصًا حركات الأيونات عبر الغشاء، خلل الميتوكوندريا، وتضرر الحجيرات الداخلية — التي تدفع التجميع الفيزيائي لمجمع الإنفلاماسوم والتنشيط الكامل لكاسبيز‑1.
الأيونات والمصانع الطاقية ومراكز التدوير تدخل السرد
على الرغم من أن NLRP3 يستجيب للعديد من التهديدات المختلفة، تظهر عدة عمليات أساسية بشكل متكرر. إحداها هو تدفق الأيونات المشحونة. فقدان البوتاسيوم من الخلية هو المنبه الأكثر اتساقًا، بأثر يساعده أو يعدله تحرّك الصوديوم والكلور والكالسيوم عبر قنوات متخصصة. أخرى هي ضائقة الميتوكوندريا: تُطلق "المصانع الطاقية" التالفة أنواعًا تفاعلية من الأكسجين وشظايا من DNA الميتوكوندري التي تساعد في استقطاب وتنشيط NLRP3، ويمكن لأدوية مثل الميتفورمين أن تخفف هذه الإشارة الميتوكوندرية. ثالثًا إصابة الليزوزوم، التي قد تحدث عندما تبتلع الخلايا جزيئات حادة؛ تمزق هذه المراكز التدويرية يطلق إنزيمات وأيونات تعزز أكثر تنشيط NLRP3. وفي الوقت نفسه، يمكن لتغير التمثيل الغذائي الخلوي — كيف تحرق الخلايا الغلوكوز والدهون وغيرها من الوقود — أن يسرّع أو يبطئ نشاط الإنفلاماسوم، حيث تدفع بعض المستقلبات مثل السكسينات والبالميتات الالتهاب، بينما تكبح أخرى مثل الإيتاكونيت، الفورمات، أو أجسام الكيتون النشاط.
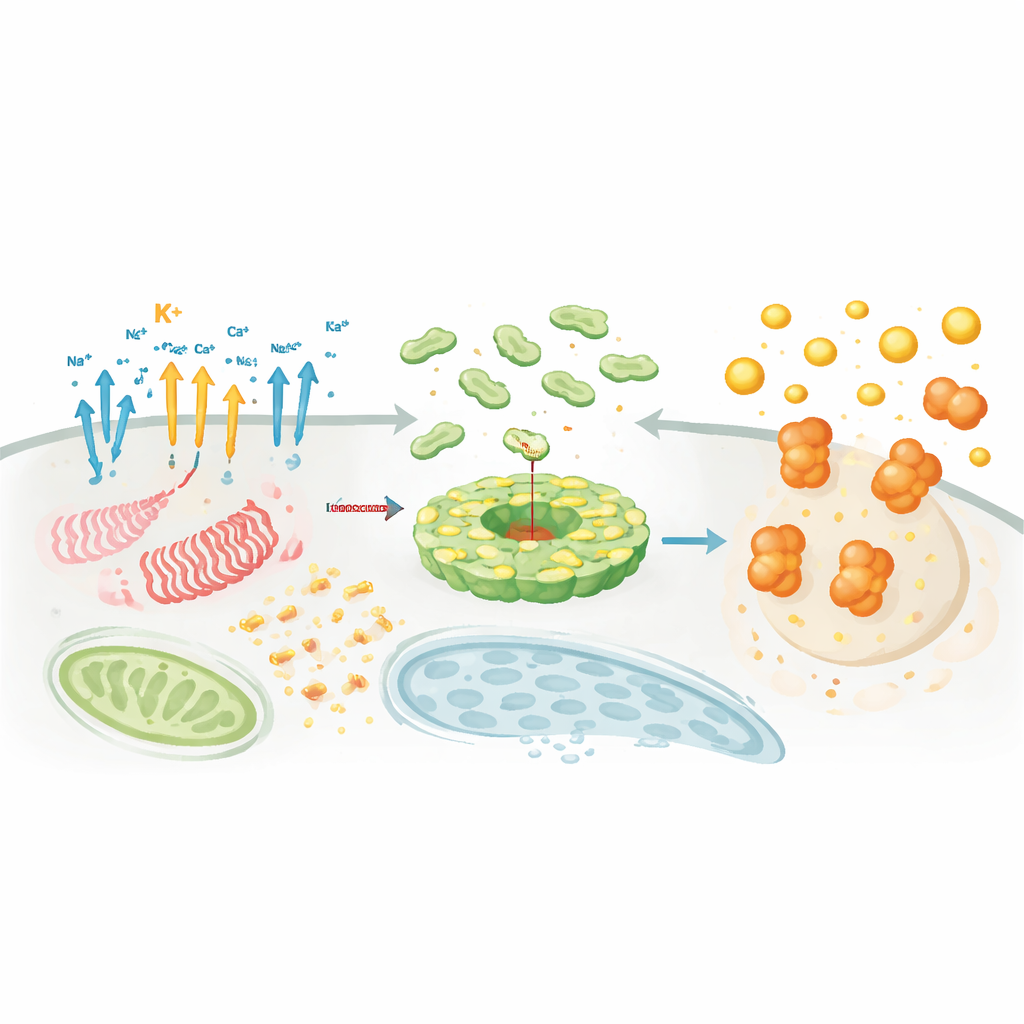
أين ومتى يتجمع المجمع
بخلاف الإشارات الكيميائية، الموقع والتوقيت محوريان. ينتقل NLRP3 وشركاؤه بين العُضيّات، متسلقين السقالات الداخلية للخلية للتجمع عند محاور محددة مثل شبكة ما بعد جهاز غولجي ومركز تنظيم الأنابيب الدقيقة. هناك، تعمل بروتينات مساعدة مثل NEK7 كـ"عوامل ترخيص" تعيد تشكيل NLRP3 من قفص مثبط ذاتيًا إلى قرص نشط قادر على الارتباط بـASC. توجه التعديلات الدهنية، مثل بالميتويليشن، والتفاعلات الكهربائية الساكنة مع شحميات غشائية معينة NLRP3 إلى المكان المناسب في الوقت المناسب. بالتوازي مع هذا الرقص، ترفق أو تزيل عشرات الإنزيمات علامات تنظيمية — سلاسل الأوبيكويتين، مجموعات الفوسفات، علامات الأسيل، وبروتينات SUMO — التي تضبط وفرة NLRP3 واستقراره وقدرته على الارتباط بـASC وكاسبيز‑1. تشرح هذه الشبكة التنظيمية الكثيفة لماذا يمكن أن يكون NLRP3 حساسًا للغاية للسياق، ونوع الخلية، وحالة المرض.
موازنة النفع والضرر
نظرًا لأن مجمع الإنفلاماسوم المفرط النشاط يمكن أن يكون خطيرًا مثل العدوى، تنشر الخلايا أيضًا مكابح. ترتبط العديد من البروتينات بـNLRP3 أو عوامله المصاحبة لحجب تفاعلات رئيسية، توجيهه نحو التحلل، أو منع تجمعه، بينما تعزز بروتينات أخرى تجميعه عند وجود تهديد حقيقي. تحصي المراجعة هذه الشركاء الإيجابيين والسلبيين وتبيّن أن عيوبًا طفيفة — الكثير من تعديل منشط أو القليل جدًا من تعديل مثبط — قد تُرجِح النظام نحو التهاب مزمن. يجادل المؤلفون بأن فهم كيفية تفاعل كل هذه المفاتيح سيكون أساسيًا لتصميم العلاجات. عن طريق استهداف إنزيمات محددة تعدل NLRP3 أو مساعديه، يمكن أن تبرد أدوية مستقبلية الإنفلاماسوم انتقائيًا في أنسجة أو أمراض معينة، مما يحافظ على دوره المنقذ للحياة في دفاع المضيف مع منع الأذى الجانبي المرصود في العديد من الاضطرابات الالتهابية والتنكسية.
الاستشهاد: Shin, H.J., Kim, I.S., Kim, J.K. et al. Molecular mechanisms of NLRP3 inflammasome activation. Exp Mol Med 58, 650–663 (2026). https://doi.org/10.1038/s12276-026-01656-9
الكلمات المفتاحية: مجمع الإنفلاماسوم NLRP3, المناعة الفطرية, الالتهاب, التعديل بعد الترجمة, التمثيل الغذائي المناعي