Clear Sky Science · pt
Mecanismos moleculares da ativação do inflamaossoma NLRP3
Por que nossas células acionam um alarme molecular
Nossos corpos dependem de células imunes de linha de frente para perceber problemas — micróbios invasores, partículas tóxicas ou estresse interno — e dar o alarme rapidamente. Um dos interruptores de alarme mais poderosos é uma máquina proteica chamada inflamaossoma NLRP3. Quando ele é ativado, desencadeia inflamação que pode nos proteger de infecções. Mas se esse interruptor ficar preso na posição “ligado”, pode provocar uma longa lista de doenças, da gota e diabetes à neurodegeneração. Esta revisão explica, em detalhe molecular, como o inflamaossoma NLRP3 é montado, o que o ativa e como as células ajustam finamente sua atividade, oferecendo pistas para fármacos futuros que esfriem a inflamação prejudicial sem calar defesas úteis.
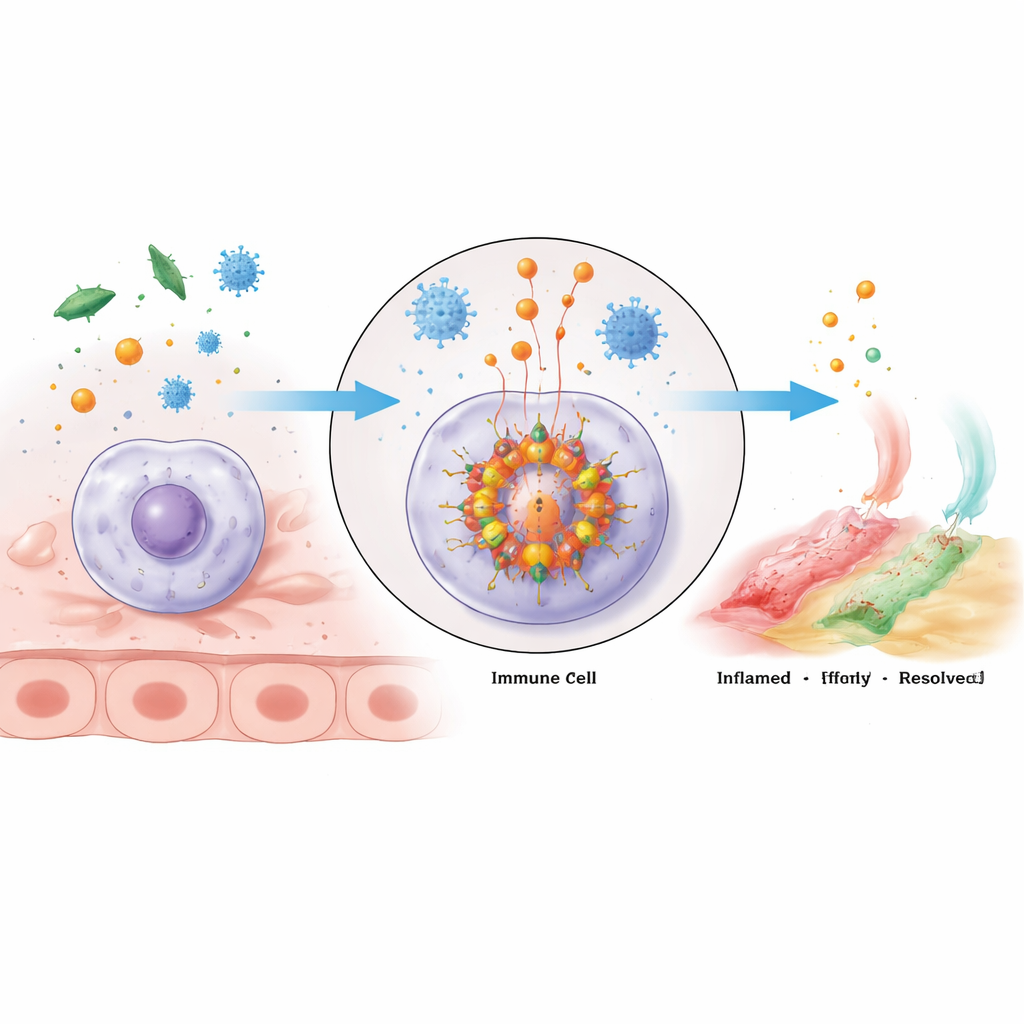
Um aglomerado de alarme molecular dentro das células imunes
O inflamaossoma NLRP3 é um grande conjunto multiproteico que se monta dentro de células imunes quando elas detectam perigo. Seu núcleo consiste na proteína sensor NLRP3, um adaptador chamado ASC e a enzima caspase‑1. NLRP3 tem várias regiões com funções distintas: uma extremidade conecta‑se ao ASC, a parte central liga ATP rico em energia e ajuda as unidades de NLRP3 a se agregarem, e a cauda ajuda a manter o sensor desligado até que o problema apareça. Quando ativadas, as moléculas de NLRP3 oligomerizam — agrupam‑se — e recrutam ASC, que forma andaimes em forma de filamento que então atraem a caspase‑1. Uma vez agrupada, a caspase‑1 é ativada e cliva precursores inativos das potentes citocinas inflamatórias IL‑1β e IL‑18, assim como uma proteína chamada gasdermina D que pode perfurar a membrana celular, produzindo uma resposta inflamatória intensa e muitas vezes letal chamada piroptose.
Dois sinais verdes: preparar e disparar
A ativação do NLRP3 não é um evento único, mas um processo em duas etapas. A primeira etapa, chamada priming (preparação), ocorre quando receptores que reconhecem micróbios ou hormônios inflamatórios são engajados. Esses sinais ativam o fator de transcrição NF‑κB, que aumenta a produção do próprio NLRP3 e dos precursores inativos das citocinas IL‑1β e IL‑18. Ao mesmo tempo, uma rede de ajustes químicos chamada modificações pós‑traducionais — como adição ou remoção de grupos fosfato, ubiquitina, SUMO, acetil, lipídio ou ADP‑ribose — “autoriza” o NLRP3, posicionando‑o em um estado pronto, mas ainda não perigoso. A segunda etapa, a ativação, é desencadeada por uma ampla gama de estímulos: ATP extracelular, toxinas bacterianas, cristais em forma de agulha como sílica ou ácido úrico, estresse mitocondrial, ruptura lisossomal e mais. Esses gatilhos diversos convergem em mudanças celulares comuns — especialmente movimentos iônicos através da membrana, disfunção mitocondrial e danos a compartimentos internos — que impulsionam a montagem física do complexo do inflamaossoma e a ativação plena da caspase‑1.
Ions, usinas de energia e centros de reciclagem entram na história
Apesar de o NLRP3 responder a muitas ameaças diferentes, vários processos centrais reaparecem. Um é o fluxo de íons carregados. A perda de potássio da célula é o ativador mais consistente, auxiliada ou modulada por movimentos de sódio, cloreto e cálcio através de canais especializados. Outro é o sofrimento mitocondrial: “usinas” danificadas liberam espécies reativas de oxigênio e fragmentos de DNA mitocondrial que ajudam a recrutar e ativar o NLRP3, e fármacos como a metformina podem atenuar esse sinal mitocondrial. Um terceiro é a lesão lisossomal, que pode ocorrer quando células engolfam partículas cortantes; a ruptura desses centros de reciclagem libera enzimas e íons que promovem ainda mais a ativação do NLRP3. Paralelamente, mudanças no metabolismo celular — como as células queimam glicose, lipídios e outros combustíveis — podem acelerar ou frear a atividade do inflamaossoma, com alguns metabólitos como succinato e palmítico estimulando a inflamação e outros como itaconato, fumarato ou corpos cetônicos a restringindo.
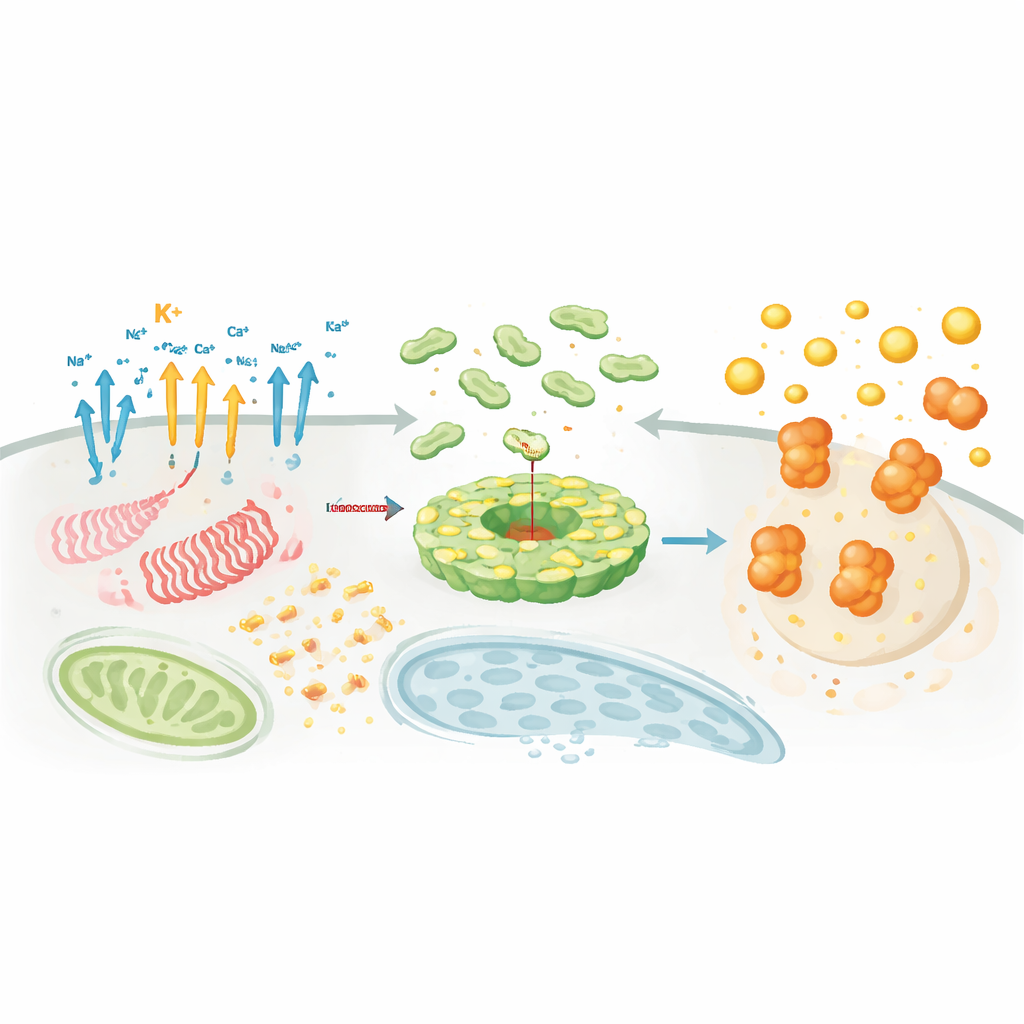
Onde e quando o complexo se monta
Além dos sinais químicos, localização e tempo são cruciais. NLRP3 e seus parceiros movem‑se entre organelas, viajando ao longo do andaime interno da célula para se reunir em pontos específicos como a rede trans‑Golgi e o centro organizador de microtúbulos. Ali, proteínas auxiliares como NEK7 atuam como “fatores de autorização” que reformulam o NLRP3 de uma gaiola autoinibida para um disco ativo capaz de se ligar ao ASC. Modificações lipídicas, como a palmitoilação, e interações eletrostáticas com lipídios de membrana particulares direcionam o NLRP3 ao lugar certo no momento certo. Paralelamente a essa coreografia, dezenas de enzimas adicionam ou removem marcas regulatórias — cadeias de ubiquitina, grupos fosfato, marcas de acetil e proteínas SUMO — que ajustam finamente a abundância do NLRP3, sua estabilidade e sua capacidade de se ligar ao ASC e à caspase‑1. Essa densa rede regulatória explica por que o NLRP3 pode ser extremamente sensível ao contexto, ao tipo celular e ao estado da doença.
Equilibrando ajuda e dano
Como um inflamaossoma hiperativo pode ser tão perigoso quanto uma infecção, as células também implementam freios. Muitas proteínas se ligam ao NLRP3 ou a seus cofatores para bloquear interações chave, encaminhá‑lo para degradação ou impedir sua agregação, enquanto outras promovem sua montagem diante de uma ameaça real. A revisão cataloga esses parceiros positivos e negativos e mostra que defeitos sutis — excesso de uma modificação ativadora ou falta de uma inibitória — podem deslocar o sistema em direção à inflamação crônica. Os autores argumentam que entender como todos esses interruptores interagem será essencial para projetar terapias. Ao direcionar enzimas específicas que modificam o NLRP3 ou seus auxiliares, futuros medicamentos poderiam resfriar seletivamente o inflamaossoma em tecidos ou doenças particulares, preservando seu papel vital na defesa do hospedeiro ao mesmo tempo em que evitam os danos colaterais observados em muitos distúrbios inflamatórios e degenerativos.
Citação: Shin, H.J., Kim, I.S., Kim, J.K. et al. Molecular mechanisms of NLRP3 inflammasome activation. Exp Mol Med 58, 650–663 (2026). https://doi.org/10.1038/s12276-026-01656-9
Palavras-chave: inflamaossoma NLRP3, imunidade inata, inflamação, modificação pós‑traducional, imunometabolismo