Clear Sky Science · es
Mecanismos moleculares de activación del inflamasoma NLRP3
Por qué nuestras células encienden una alarma molecular
Nuestros cuerpos dependen de células inmunitarias de primera línea para detectar problemas —microbios invasores, partículas tóxicas o estrés interno— y dar la alarma con rapidez. Uno de los interruptores de alarma más potentes es una maquinaria proteica llamada inflamasoma NLRP3. Cuando se activa, desencadena inflamación que puede salvarnos de una infección. Pero si este interruptor queda atascado en la posición de “encendido”, puede impulsar una larga lista de enfermedades, desde la gota y la diabetes hasta la neurodegeneración. Este artículo de revisión explica, en detalle molecular, cómo se ensambla el inflamasoma NLRP3, qué lo pone en marcha y cómo las células afinan su actividad, ofreciendo pistas para futuros fármacos que atenúen la inflamación dañina sin silenciar las defensas útiles.
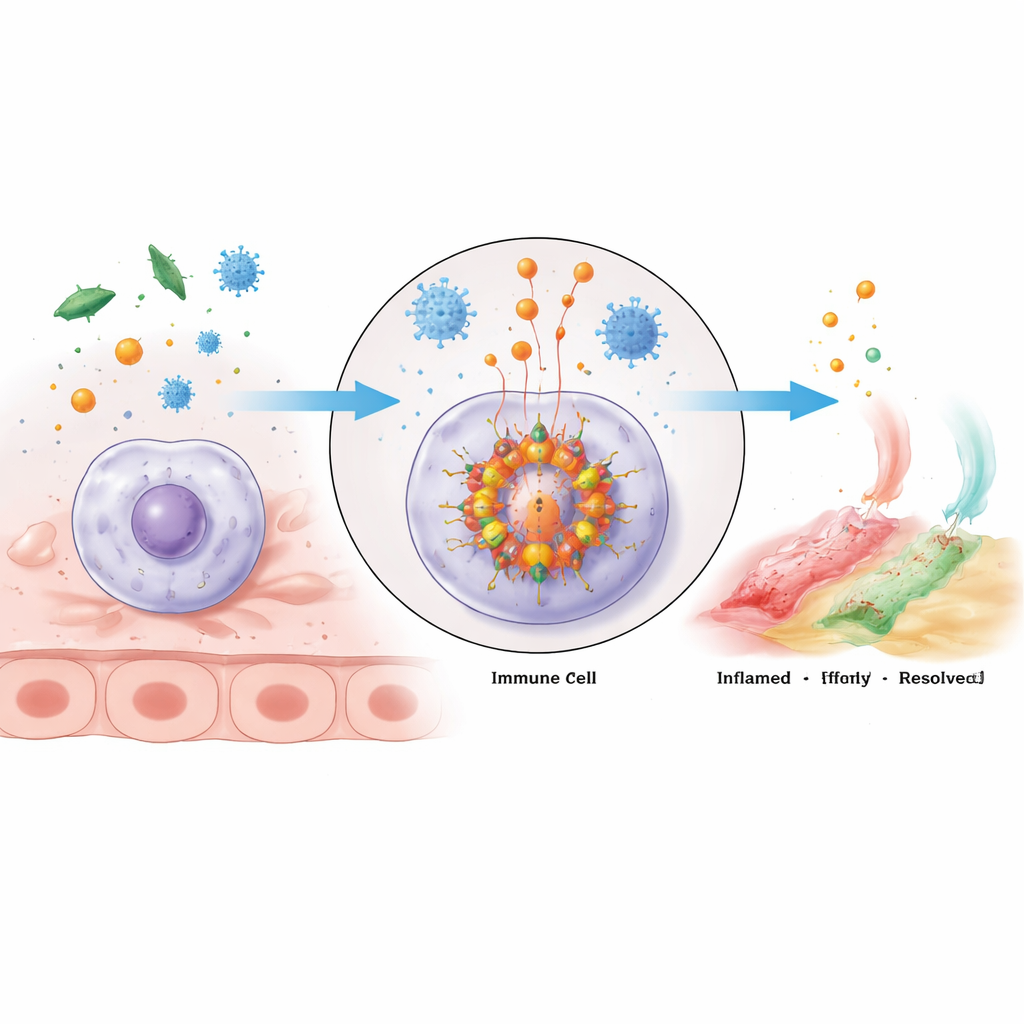
Un clúster de alarma molecular dentro de las células inmunitarias
El inflamasoma NLRP3 es un gran conjunto multiproteico que se ensambla dentro de las células inmunitarias cuando detectan peligro. Su núcleo consta de la proteína sensor NLRP3, un adaptador llamado ASC y la enzima caspasa‑1. NLRP3 tiene varias regiones con funciones distintas: un extremo conecta con ASC, la región central une ATP rico en energía y ayuda a que las unidades de NLRP3 se agrupen, y la cola contribuye a mantener el sensor apagado hasta que aparece la señal de peligro. Al activarse, las moléculas de NLRP3 se oligomerizan —se agrupan— y reclutan a ASC, que forma andamiajes filamentosos que a su vez atraen a la caspasa‑1. Una vez agrupada, la caspasa‑1 se activa y corta precursores inactivos de los potentes mensajeros inflamatorios IL‑1β e IL‑18, así como una proteína llamada gasdermina D que puede perforar la membrana celular, produciendo una respuesta inflamatoria ardiente y a menudo letal llamada piroptosis.
Dos luces verdes: preparación y disparo
La activación de NLRP3 no es un evento único sino un proceso de dos pasos. El primer paso, llamado cebado, ocurre cuando se activan receptores que detectan microbios u hormonas inflamatorias. Estas señales activan el factor de transcripción NF‑κB, que aumenta la producción del propio NLRP3 y de los precursores inactivos de las citocinas IL‑1β e IL‑18. Al mismo tiempo, una red de modificaciones químicas denominada modificaciones postraduccionales —como la adición o remoción de grupos fosfato, ubiquitina, SUMO, acetilo, lípido o ADP‑ribosa— “licencia” a NLRP3, colocándolo en un estado preparado pero aún no peligroso. El segundo paso, la activación, se desencadena por una amplia variedad de estímulos: ATP extracelular, toxinas bacterianas, cristales en forma de aguja como la sílice o el ácido úrico, estrés mitocondrial, rotura lisosomal y más. Estos diversos desencadenantes convergen en cambios celulares comunes —especialmente movimientos iónicos a través de la membrana, disfunción mitocondrial y daño a compartimentos internos— que impulsan el ensamblaje físico del complejo del inflamasoma y la activación completa de la caspasa‑1.
Iones, centrales energéticas y centros de reciclaje participan en la historia
Aunque NLRP3 responde a muchas amenazas diferentes, varios procesos centrales reaparecen con frecuencia. Uno es el flujo de iones cargados. La pérdida de potasio de la célula es el activador más constante, ayudada o modulada por movimientos de sodio, cloruro y calcio a través de canales especializados. Otro es el malestar mitocondrial: las “centrales” dañadas liberan especies reactivas de oxígeno y fragmentos de ADN mitocondrial que ayudan a reclutar y activar NLRP3, y fármacos como la metformina pueden atenuar esta señal mitocondrial. Un tercer factor es la lesión lisosomal, que puede ocurrir cuando las células fagocitan partículas afiladas; la rotura de estos centros de reciclaje libera enzimas e iones que promueven aún más la activación de NLRP3. Mientras tanto, los cambios en el metabolismo celular —cómo las células queman glucosa, grasas y otros combustibles— pueden acelerar o frenar la actividad del inflamasoma, con algunos metabolitos como el succinato y el palmitato impulsando la inflamación y otros como el itaconato, el fumarato o los cuerpos cetónicos reprimiéndola.
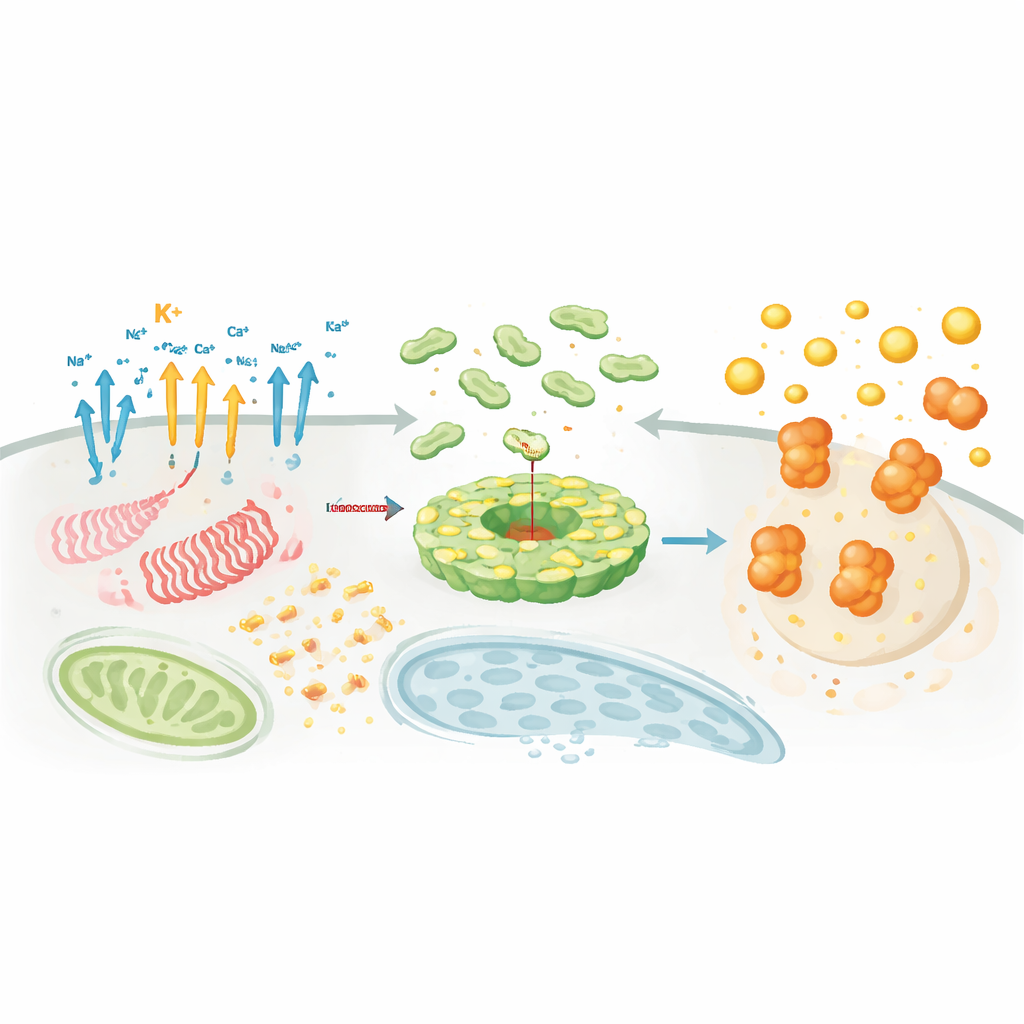
Dónde y cuándo se ensambla el complejo
Más allá de las señales químicas, la localización y el momento son cruciales. NLRP3 y sus socios se mueven entre orgánulos, desplazándose por el andamiaje interno de la célula para reunirse en centros específicos como la red trans‑Golgi y el centro organizador de microtúbulos. Allí, proteínas auxiliares como NEK7 actúan como “factores de licencia” que remodelan a NLRP3 de una jaula autoinhibida a un disco activo que puede unirse a ASC. Modificaciones lipídicas, como la palmitoilación, e interacciones electrostáticas con lípidos de membrana particulares dirigen a NLRP3 al lugar correcto en el momento oportuno. Paralelamente a esta coreografía, docenas de enzimas añaden o eliminan marcas regulatorias —cadenas de ubiquitina, grupos fosfato, marcas de acetilo y proteínas SUMO— que afinan la abundancia de NLRP3, su estabilidad y su capacidad para engancharse con ASC y caspasa‑1. Esta densa red reguladora explica por qué NLRP3 puede ser exquisitamente sensible al contexto, al tipo celular y al estado de la enfermedad.
Equilibrar ayuda y daño
Puesto que un inflamasoma hiperactivo puede ser tan peligroso como una infección, las células también despliegan frenos. Muchas proteínas se unen a NLRP3 o a sus cofactores para bloquear interacciones clave, dirigirlo hacia la degradación o impedir su agrupamiento, mientras que otras potencian su ensamblaje ante una amenaza genuina. La revisión cataloga estos socios positivos y negativos y muestra que defectos sutiles —demasiada una modificación activadora o muy poca de una inhibidora— pueden inclinar el sistema hacia la inflamación crónica. Los autores sostienen que comprender cómo interactúan todos estos interruptores será esencial para diseñar terapias. Al dirigirse a enzimas específicas que modifican a NLRP3 o a sus ayudantes, futuros fármacos podrían enfriar selectivamente el inflamasoma en tejidos o enfermedades concretas, preservando su papel salvador en la defensa del huésped mientras previenen el daño colateral observado en muchos trastornos inflamatorios y degenerativos.
Cita: Shin, H.J., Kim, I.S., Kim, J.K. et al. Molecular mechanisms of NLRP3 inflammasome activation. Exp Mol Med 58, 650–663 (2026). https://doi.org/10.1038/s12276-026-01656-9
Palabras clave: inflamasoma NLRP3, inmunidad innata, inflamación, modificación postraduccional, inmunometabolismo