Clear Sky Science · fr
Mécanismes moléculaires de l’activation de l’inflammasome NLRP3
Pourquoi nos cellules déclenchent une alarme moléculaire
Notre organisme compte sur des cellules immunitaires de première ligne pour détecter les signes de danger — microbes envahisseurs, particules toxiques ou stress interne — et déclencher l’alerte rapidement. L’un des interrupteurs d’alarme les plus puissants est une machine protéique appelée l’inflammasome NLRP3. Lorsqu’il s’active, il déclenche une inflammation qui peut nous protéger contre l’infection. Mais si cet interrupteur reste bloqué en position « marche », il peut provoquer de nombreuses maladies, de la goutte et du diabète à la neurodégénérescence. Cet article de synthèse explique, en détail moléculaire, comment l’inflammasome NLRP3 est construit, ce qui l’active et comment les cellules ajustent finement son activité, offrant des pistes pour de futurs médicaments qui calmeraient l’inflammation nuisible sans neutraliser les défenses utiles.
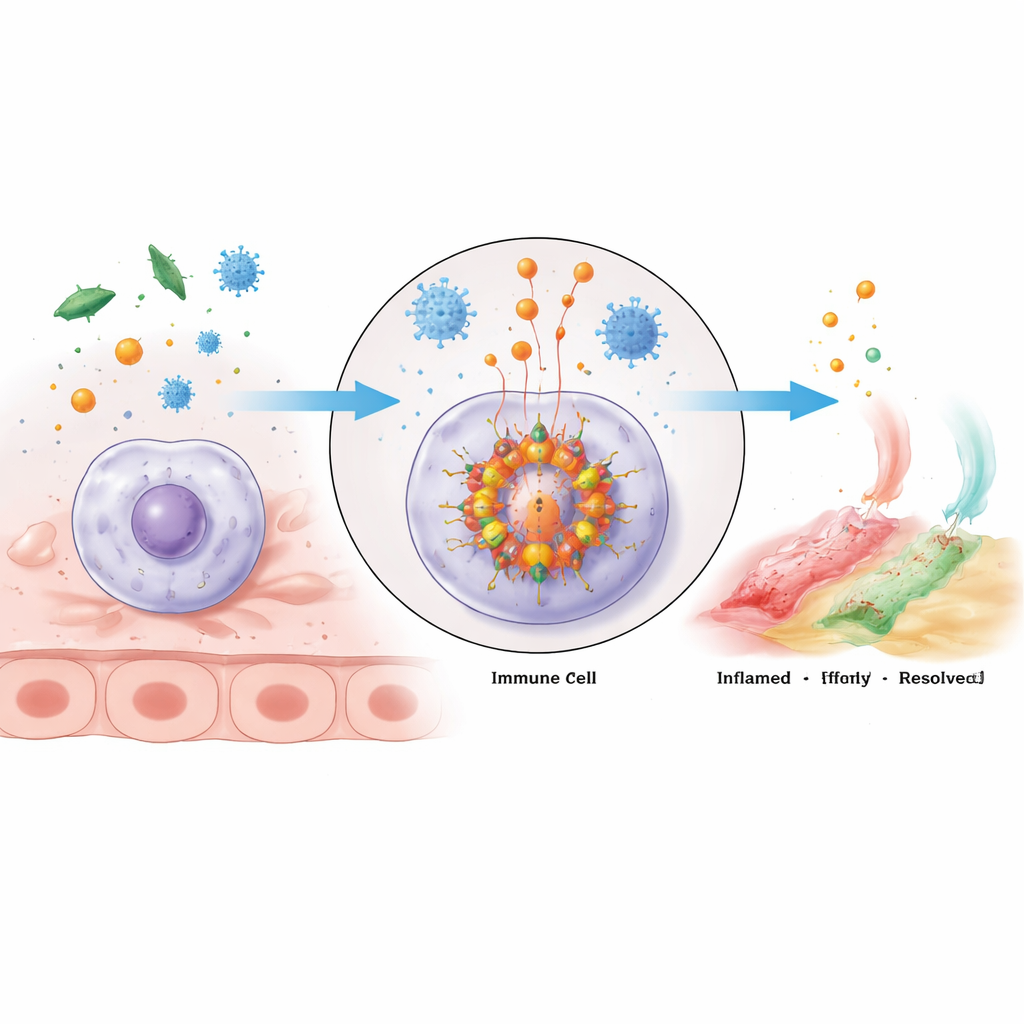
Un cluster d’alarme moléculaire à l’intérieur des cellules immunitaires
L’inflammasome NLRP3 est un large assemblage multi‑protéique qui se forme à l’intérieur des cellules immunitaires lorsqu’elles détectent un danger. Son noyau est composé de la protéine détectrice NLRP3, d’un adaptateur nommé ASC et de l’enzyme caspase‑1. NLRP3 comporte plusieurs domaines aux fonctions distinctes : une extrémité se lie à ASC, le domaine central fixe l’ATP riche en énergie et favorise l’agrégation des unités NLRP3, et la partie terminale participe au maintien du capteur en état inactif tant qu’il n’y a pas de danger. Une fois activés, les molécules NLRP3 s’oligomérisent — se regroupent — et recrutent ASC, qui forme des échafaudages en filaments attirant ensuite la caspase‑1. Une fois agrégée, la caspase‑1 s’active et clive les précurseurs inactifs des puissants médiateurs inflammatoires IL‑1β et IL‑18, ainsi qu’une protéine appelée gasdermine D capable de percer la membrane cellulaire, entraînant une réponse inflammatoire vive, souvent létale, appelée pyroptose.
Deux feux verts : préparation et déclenchement
L’activation de NLRP3 n’est pas un événement unique mais un processus en deux étapes. La première étape, dite d’amorçage, survient lorsque des récepteurs détectant des microbes ou des hormones inflammatoires sont engagés. Ces signaux activent le facteur de transcription NF‑κB, qui augmente la production de NLRP3 lui‑même et des précurseurs cytokiniques inactifs IL‑1β et IL‑18. Parallèlement, un réseau de modifications chimiques appelé modifications post‑traductionnelles — telles que l’ajout ou la suppression de groupes phosphate, ubiquitine, SUMO, acétyl, lipide ou ADP‑ribose — « autorise » NLRP3, le plaçant dans un état prêt mais pas encore dangereux. La deuxième étape, l’activation, est déclenchée par une grande variété de stimuli : ATP extracellulaire, toxines bactériennes, cristaux en forme d’aiguille comme la silice ou l’acide urique, stress mitochondrial, rupture lysosomale, et plus encore. Ces déclencheurs divers convergent vers des changements cellulaires communs — en particulier des mouvements d’ions à travers la membrane, une dysfonction mitochondriale et des dommages aux compartiments internes — qui favorisent l’assemblage physique du complexe inflammasome et l’activation complète de la caspase‑1.
Des ions, des centrales énergétiques et des centres de recyclage entrent en jeu
Même si NLRP3 répond à de nombreuses menaces différentes, plusieurs processus centraux reviennent fréquemment. L’un d’eux est le flux d’ions chargés. La perte de potassium intracellulaire est l’activateur le plus constant, modulée ou assistée par des mouvements de sodium, de chlore et de calcium via des canaux spécialisés. Un autre est la détresse mitochondriale : les « centrales » endommagées libèrent des espèces réactives de l’oxygène et des fragments d’ADN mitochondrial qui favorisent le recrutement et l’activation de NLRP3, et des médicaments comme la metformine peuvent atténuer ce signal mitochondrial. Un troisième est la lésion lysosomale, qui peut survenir lorsque les cellules phagocytent des particules tranchantes ; la rupture de ces centres de recyclage libère des enzymes et des ions qui stimulent davantage l’activation de NLRP3. Parallèlement, la modification du métabolisme cellulaire — la manière dont les cellules brûlent glucose, lipides et autres carburants — peut accélérer ou freiner l’activité de l’inflammasome, certains métabolites comme le succinate et le palmitate favorisant l’inflammation alors que d’autres, comme l’itaconate, le fumarate ou les corps cétoniques, la restreignent.
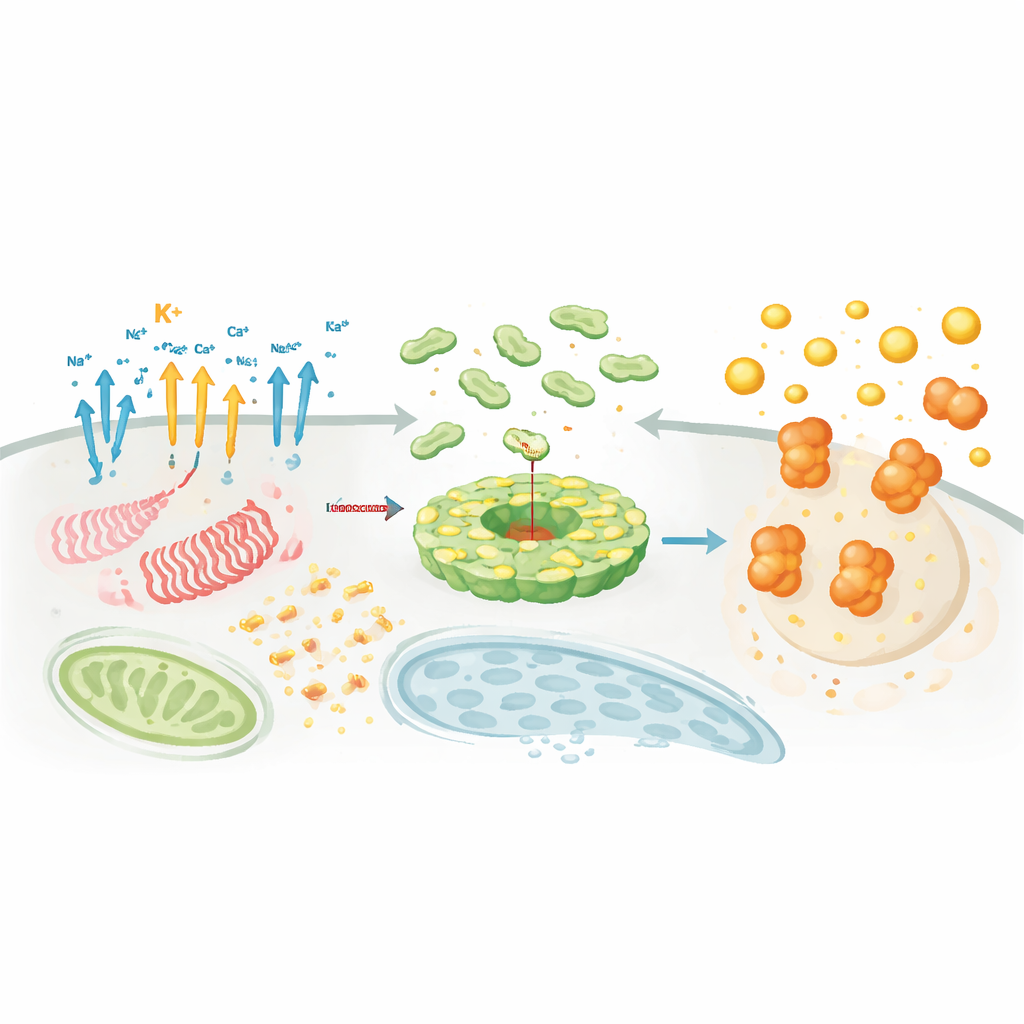
Où et quand le complexe s’assemble
Au‑delà des signaux chimiques, le lieu et le moment sont cruciaux. NLRP3 et ses partenaires se déplacent entre les organites, empruntant le réseau interne de la cellule pour se rassembler en points précis tels que le réseau trans‑Golgi et le centre organisateur des microtubules. Là, des protéines auxiliaires comme NEK7 jouent le rôle de « facteurs d’autorisation » qui transforment NLRP3 d’une cage autoinhibée en un disque actif capable de se lier à ASC. Des modifications lipidiques, comme la palmitoylation, et des interactions électrostatiques avec des lipides membranaires particuliers guident NLRP3 vers le bon endroit au bon moment. En parallèle de cette chorégraphie, des dizaines d’enzymes ajoutent ou retirent des étiquettes régulatrices — chaînes d’ubiquitine, groupes phosphate, marques d’acétyl et protéines SUMO — qui ajustent la quantité de NLRP3, sa stabilité et sa capacité à se lier à ASC et à la caspase‑1. Ce réseau régulatoire dense explique pourquoi NLRP3 peut être extrêmement sensible au contexte, au type cellulaire et à l’état pathologique.
Équilibrer aide et dommage
Parce qu’un inflammasome hyperactif peut être aussi dangereux qu’une infection, les cellules déploient aussi des freins. De nombreuses protéines se lient à NLRP3 ou à ses cofactors pour bloquer des interactions clés, diriger sa dégradation ou empêcher son agglomération, tandis que d’autres favorisent son assemblage en cas de menace réelle. La revue recense ces partenaires positifs et négatifs et montre que de subtils défauts — trop d’une modification activatrice ou trop peu d’une modification inhibitrice — peuvent faire basculer le système vers une inflammation chronique. Les auteurs soutiennent que comprendre comment toutes ces commutateurs interagissent sera essentiel pour concevoir des thérapies. En ciblant des enzymes spécifiques qui modifient NLRP3 ou ses assistants, des médicaments futurs pourraient refroidir sélectivement l’inflammasome dans des tissus ou des maladies particulières, préservant son rôle vital dans la défense de l’hôte tout en évitant les dommages collatéraux observés dans de nombreux troubles inflammatoires et dégénératifs.
Citation: Shin, H.J., Kim, I.S., Kim, J.K. et al. Molecular mechanisms of NLRP3 inflammasome activation. Exp Mol Med 58, 650–663 (2026). https://doi.org/10.1038/s12276-026-01656-9
Mots-clés: inflammasome NLRP3, immunité innée, inflammation, modification post‑traductionnelle, immunométabolisme