Clear Sky Science · he
מנגנונים מולקולריים של הפעלת ה-inflammasome NLRP3
מדוע התאים שלנו מדליקים אזעקת אש מולקולרית
הגוף שלנו נשען על תאי חיסון בקו הראשון כדי לזהות בעיות—מיקרובים פולשים, חלקיקים רעילים או מתח פנימי—ולהשמיע את האזעקה במהירות. אחד ממפסקי האזעקה החזקים ביותר הוא מכונת חלבון הנקראת inflammasome NLRP3. כשהיא נדלקת, היא מציתה דלקת שיכולה להציל אותנו מזיהום. אך אם המפסק הזה תקוע בעמדת "דלק" הוא עלול להניע רשימה ארוכה של מחלות, מגאוט וסוכרת ועד ניוון עצבי. סקירה זו מסבירה, בפרטי מולקולה, איך בנוי ה-inflammasome NLRP3, מה מפעיל אותו ואיך תאים מכוונים את פעילותו בדייקנות, ומספקת רמזים לפיתוח תרופות עתידיות שיכבות דלקת מזיקה מבלי להשתיק את ההגנות החשובות.
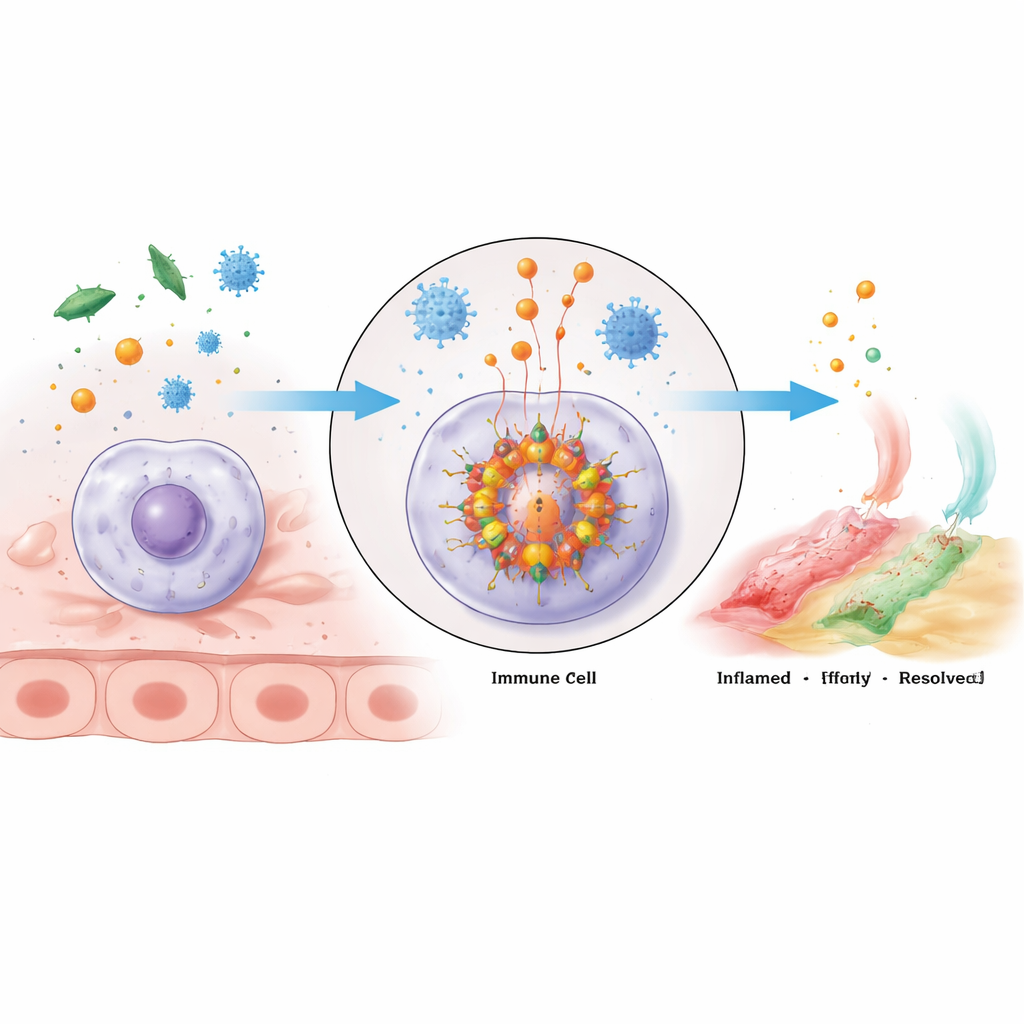
אשכול אזעקה מולקולרי בתוך תאי חיסון
ה-inflammasome NLRP3 הוא צביר רב‑חלבוני גדול שמתארגן בתוך תאים חיסוניים כאשר הם מזהים סכנה. הליבה שלו מורכבת מחלבון החיישן NLRP3, מתווך הנקרא ASC ומהאנזים קסקאז‑1. ל‑NLRP3 יש כמה אזורים עם תפקידים מובחנים: קצה אחד מתחבר ל‑ASC, האמצע קושר ATP עשיר באנרגיה ועוזר ליחידות NLRP3 להצטבר, והזנב עוזר לשמור על החיישן במצב כבוי עד להופעת הבעיה. כאשר הוא מופעל, מולקולות NLRP3 אוליגומריזציה—מתאחדות—ומגייסות את ASC, שמייצר שלד פתילי שמושך את קסקאז‑1. ברגע שהן מצטברות, קסקאז‑1 מופעל וחותך קדם‑ציטוקינים לא פעילים של שליחי דלקת רבי‑עוצמה IL‑1β ו‑IL‑18, וכן חותך חלבון בשם gasdermin D שיכול ליצור חורים בממברנת התא, מה שמוביל לתגובה דלקתית לוחמנית ולעתים קטלנית הנקראת פיירופטוזיס.
שני אור ירוק: ההכנה והירי
הפעלה של NLRP3 אינה אירוע יחיד אלא תהליך בן שני שלבים. השלב הראשון, שנקרא priming, מתרחש כאשר קולטנים החושיים למיקרובים או הורמוני דלקת מופעלים. אותות אלה מפעילים את גורם השעתוק NF‑κB, שמגביר את ייצורו של NLRP3 עצמו ואת קדם‑הציטוקינים הלא פעילים IL‑1β ו‑IL‑18. במקביל, רשת של תיקונים כימיים שנקראת שינויים אחרי תרגום—כמו הוספה או חיתוך של קבוצות זרחן, ubiquitin, SUMO, אצטיל, ליפיד או ADP‑ריבוז—"מאשרת" את NLRP3, מציבה אותו במצב ער אך עוד לא מסוכן. השלב השני, ההפעלה, מזורז על ידי מגוון רחב של גירויים: ATP חוץ‑תאי, רעלני חיידקים, גבישים מחודדים כמו סיליקה או חומצת שתן, מתח מיטוכונדריאלי, קריעת הליזוזומים ועוד. טריגרים מגוונים אלה מתנקזים לשינויים תאיים משותפים—ובמיוחד לתנועת יונים דרך הממברנה, לבעיה בתפקוד המיטוכונדריה ולנזק למחלקות פנימיות—שמעוררים את ההרכבה הפיזית של קומפלקס ה‑inflammasome ואת ההפעלה המלאה של קסקאז‑1.
יונים, תחנות כוח ומרכזי מיחזור מצטרפים לסיפור
למרות ש‑NLRP3 מגיב לאיומים שונים, כמה תהליכים מרכזיים חוזרים. אחד מהם הוא זרימת היונים המנטענים. אובדן אשלגן מהתא הוא המפעיל העקבי ביותר, כשהוא מסייע או מתווך על ידי תנועות נתרן, כלוריד וסידן דרך תעלות מיוחדות. נוסף על כך, מתח מיטוכונדריאלי: "תחנות הכוח" שנפגעו משחררות סוגים פעילים של חמצן וקטעי DNA מיטוכונדריאלי שמסייעים לגיוס ולהפעלת NLRP3, ותרופות כמו מטפורמין יכולות להחליש את האות המיטוכונדריאלי הזה. שלישי הוא פגיעה בליזוזום, שיכולה להתרחש כאשר תאים בולעים חלקיקים חדים; קריעת מרכזי המיחזור הללו משחררת אנזימים ויונים שמקדמים עוד יותר את הפעלת NLRP3. בינתיים, שינויים במטבוליזם התאי—איך תאים שורפים גלוקוז, שומנים ודלקים אחרים—יכולים להאיץ או לבלום את פעילות ה‑inflammasome, כאשר מטבוליטים מסוימים כמו succinate ו‑palmitate מדרבנים דלקת ואחרים כמו itaconate, fumarate או גופי קטון מעכבים אותה.
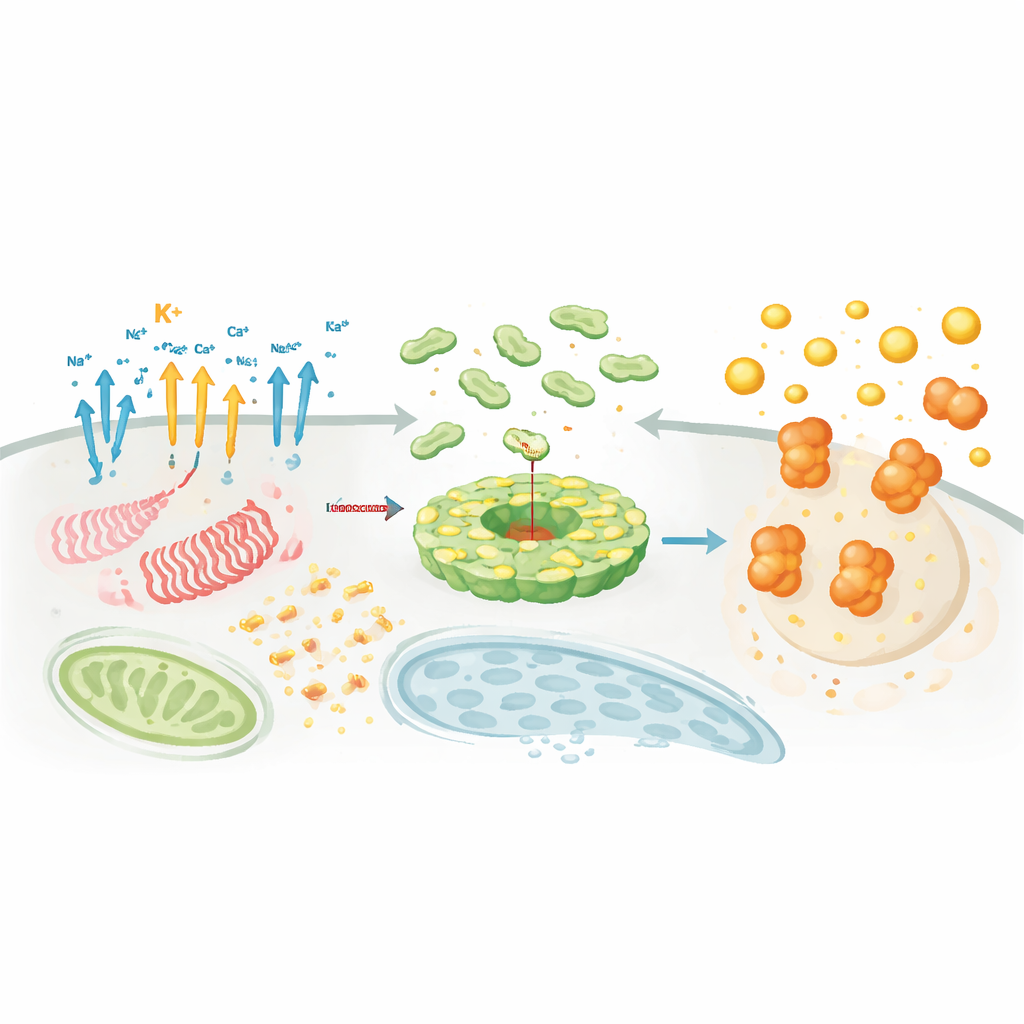
איפה ומתי הקומפלקס מתארגן
מעבר לאותות הכימיים, מיקום ותזמון הם קריטיים. NLRP3 ושותפיו נעים בין אברונים, נוסעים לאורך השלד הפנימי של התא כדי להתאסף בצמתים ספציפיים כגון רשת הטרנס‑גולג'י ומרכז ארגון המיקרוטובולים. שם, חלבונים מסייעים כמו NEK7 פועלים כ"גורמי אישור" שמעצבנים את NLRP3 מכלוב אוטו‑מעכב לדיסק פעיל שיכול לקשור את ASC. שינויים בליפידים, כמו פלמיטואילציה, ואינטראקציות אלקטרוסטטיות עם ליפידים ממברנליים מסוימים מכוונים את NLRP3 למקום ולזמן הנכונים. במקביל לכוריאוגרפיה זו, עשרות אנזימים מצמידים או מסירים תגי בקרה—שרשראות ubiquitin, קבוצות זרחן, סימני אצטיל ו‑SUMO—שמכוננים את שפעו של NLRP3, יציבותו ויכולתו להתחבר ל‑ASC ולקסקאז‑1. רשת בקרה צפופה זו מסבירה מדוע NLRP3 יכול להיות רגיש להקשר, לסוג התא ולמצב המחלה.
איזון בין עזרה ונזק
מכיוון ש‑inflammasome פעיל יתר על המידה יכול להיות מסוכן כמו זיהום, תאים מפעילים גם בלמים. חלבונים רבים נקשרים ל‑NLRP3 או לקושרותיו כדי לחסום אינטראקציות מפתח, לשלוח אותו לפירוק או למנוע את הצטברותו, בעוד אחרים משפרים את הרכבתו תחת איום אמיתי. הסקירה מונה את השותפים החיוביים והשליליים הללו ומראה שמפגעים עדינים—יותר מדי של שינוי מפעיל או מעט מדי של שינוי מעכב—יכולים להזיז את המערכת לכיוון דלקת כרונית. המחברים טוענים שהבנת האופן שבו כל המתגים האלה פועלים יחד תהיה חיונית לעיצוב טיפולים. על ידי מיקוד באנזימים ספציפיים שמתקנים את NLRP3 או את העוזרים שלו, תרופות עתידיות עשויות לקרר באופן סלקטיבי את ה‑inflammasome ברקמות או במחלות מסוימות, ולשמר את תפקידו המציל חיים בהגנה על המאחסן תוך מניעת הנזק הצדדי הנראה בהרבה הפרעות דלקתיות וניווניות.
ציטוט: Shin, H.J., Kim, I.S., Kim, J.K. et al. Molecular mechanisms of NLRP3 inflammasome activation. Exp Mol Med 58, 650–663 (2026). https://doi.org/10.1038/s12276-026-01656-9
מילות מפתח: inflammasome NLRP3, חיסון מולד, דלקת, שינוי אחרי תרגום, אימונומטבוליזם