Clear Sky Science · pl
Mechanizmy molekularne aktywacji inflamasomu NLRP3
Dlaczego nasze komórki włączają molekularny alarm
Nasze ciało polega na komórkach układu odpornościowego na pierwszej linii, które wykrywają zagrożenia — drobnoustroje, toksyczne cząstki lub wewnętrzny stres — i szybko podnoszą alarm. Jednym z najsilniejszych przełączników alarmowych jest białkowa maszyna zwana inflamasomem NLRP3. Gdy się włącza, wywołuje zapalenie, które może nas uchronić przed infekcją. Ale gdy ten przełącznik utknie w pozycji „włączonej”, może napędzać długą listę chorób, od dny moczanowej i cukrzycy po neurodegenerację. Ten przegląd wyjaśnia, w szczegółach molekularnych, jak zbudowany jest inflamasom NLRP3, co go uruchamia i jak komórki precyzyjnie regulują jego aktywność, dostarczając wskazówek do przyszłych leków, które ostudzą szkodliwe zapalenie bez wyciszania pożytecznej obrony.
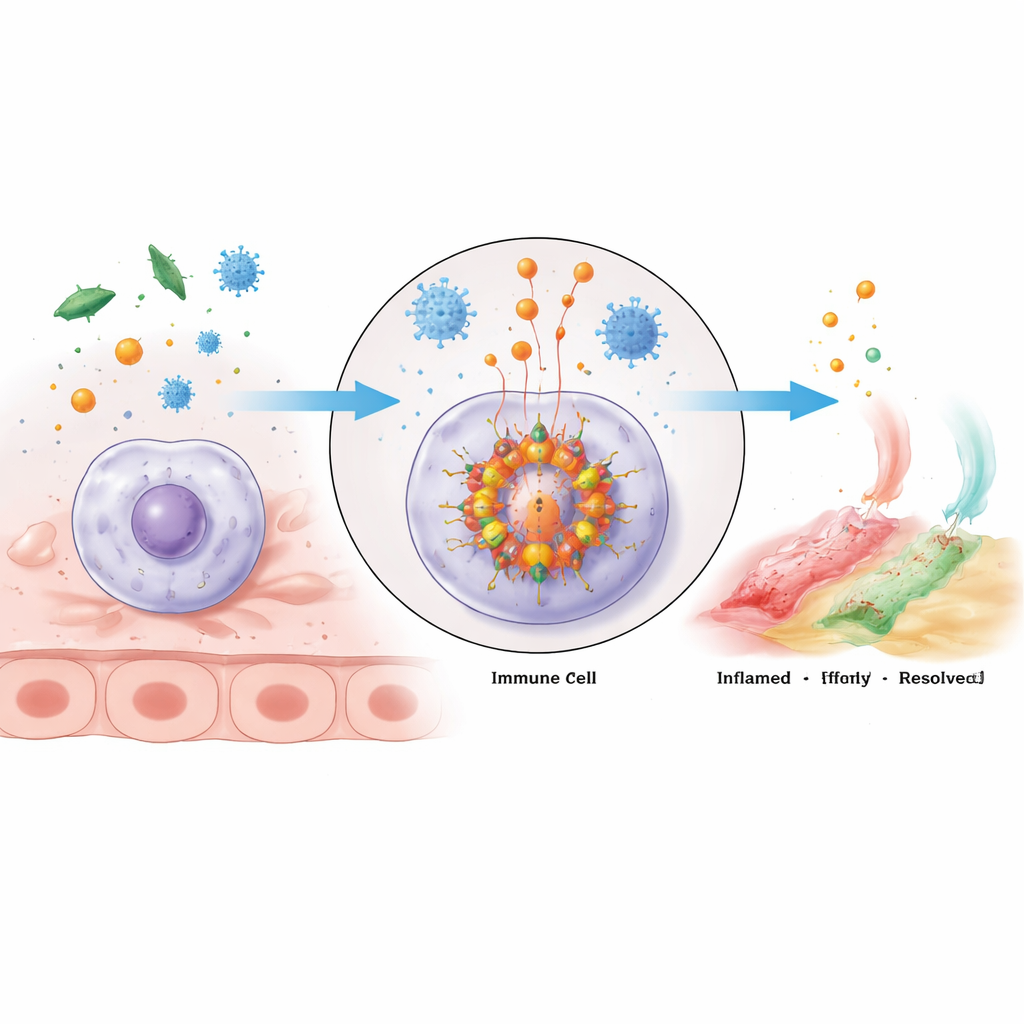
Klastrowy alarm molekularny wewnątrz komórek odpornościowych
Inflamasom NLRP3 to duży, wielobiałkowy kompleks, który składa się wewnątrz komórek odpornościowych po wykryciu zagrożenia. Jego rdzeń tworzą białko-sensor NLRP3, adaptor ASC oraz enzym kaspaza-1. NLRP3 ma kilka domen o odmiennych funkcjach: jeden koniec łączy się z ASC, środkowa część wiąże ATP bogate w energię i pomaga jednostkom NLRP3 skupiać się, a ogon pomaga utrzymywać sensor w stanie wyciszonym, dopóki nie pojawi się zagrożenie. Po aktywacji cząsteczki NLRP3 oligomeryzują — łączą się — i rekrutują ASC, które tworzy filamentowe rusztowania przyciągające kaspazę-1. Gdy kompleks jest zgrupowany, kaspaza-1 ulega aktywacji i przecina nieaktywne prekursory silnych mediatorów zapalenia IL-1β i IL-18 oraz białko gasderminę D, które potrafi tworzyć otwory w błonie komórkowej, wywołując gwałtowną, często śmiertelną reakcję zapalną zwaną pyroptozą.
Dwa zielone światła: przygotowanie i wyzwolenie
Włączenie NLRP3 nie jest jednorazowym zdarzeniem, lecz procesem dwuetapowym. Pierwszy etap, zwany przygotowaniem (priming), zachodzi, gdy aktywowane są receptory rozpoznające drobnoustroje lub hormony zapalne. Sygnały te aktywują czynnik transkrypcyjny NF-κB, który zwiększa produkcję samego NLRP3 oraz nieaktywnych prekursorów cytokin IL-1β i IL-18. Równocześnie sieć chemicznych modyfikacji zwanych modyfikacjami potranslacyjnymi — takich jak dodawanie lub usuwanie grup fosforanowych, ubikwityny, SUMO, acetylu, lipidów czy ADP-rybozy — „uprawnia” NLRP3, umieszczając go w stanie przygotowanym, lecz jeszcze nieszkodliwym. Drugi etap, aktywacja, wyzwalają różnorodne bodźce: zewnątrzkomórkowe ATP, toksyny bakteryjne, igiełkowate kryształy, takie jak krzemionka lub kwas moczowy, stres mitochondrialny, pęknięcie lizosomów i inne. Te rozmaite sygnały zbiegają się na wspólnych zmianach komórkowych — zwłaszcza przepływach jonów przez błonę, dysfunkcji mitochondriów i uszkodzeniu przedziałów wewnętrznych — które napędzają fizyczne składanie się kompleksu inflamasomu i pełną aktywację kaspazy-1.
Jony, elektrownie i centra recyklingu włączają się do opowieści
Mimo że NLRP3 odpowiada na wiele różnych zagrożeń, kilka podstawowych procesów pojawia się wielokrotnie. Jednym z nich jest przepływ jonów. Utrata potasu z komórki jest najbardziej spójnym czynnikiem aktywującym, modyfikowanym lub wspieranym przez ruchy sodu, chloru i wapnia przez wyspecjalizowane kanały. Kolejnym jest stres mitochondrialny: uszkodzone „elektrownie” uwalniają reaktywne formy tlenu i fragmenty mitochondrialnego DNA, które pomagają rekrutować i aktywować NLRP3, a leki takie jak metformina mogą osłabiać ten sygnał mitochondrialny. Trzecim jest uszkodzenie lizosomów, które może nastąpić, gdy komórki pochłaniają ostre cząstki; pęknięcie tych centrów recyklingu uwalnia enzymy i jony, które dalej sprzyjają aktywacji NLRP3. Tymczasem zmiana metabolizmu komórkowego — sposób, w jaki komórki spalają glukozę, tłuszcze i inne paliwa — może przyspieszać lub hamować aktywność inflamasomu; niektóre metabolity, jak bursztynian i palmitynian, napędzają zapalenie, podczas gdy inne, jak itakonian, fumarat czy ciała ketonowe, je ograniczają.
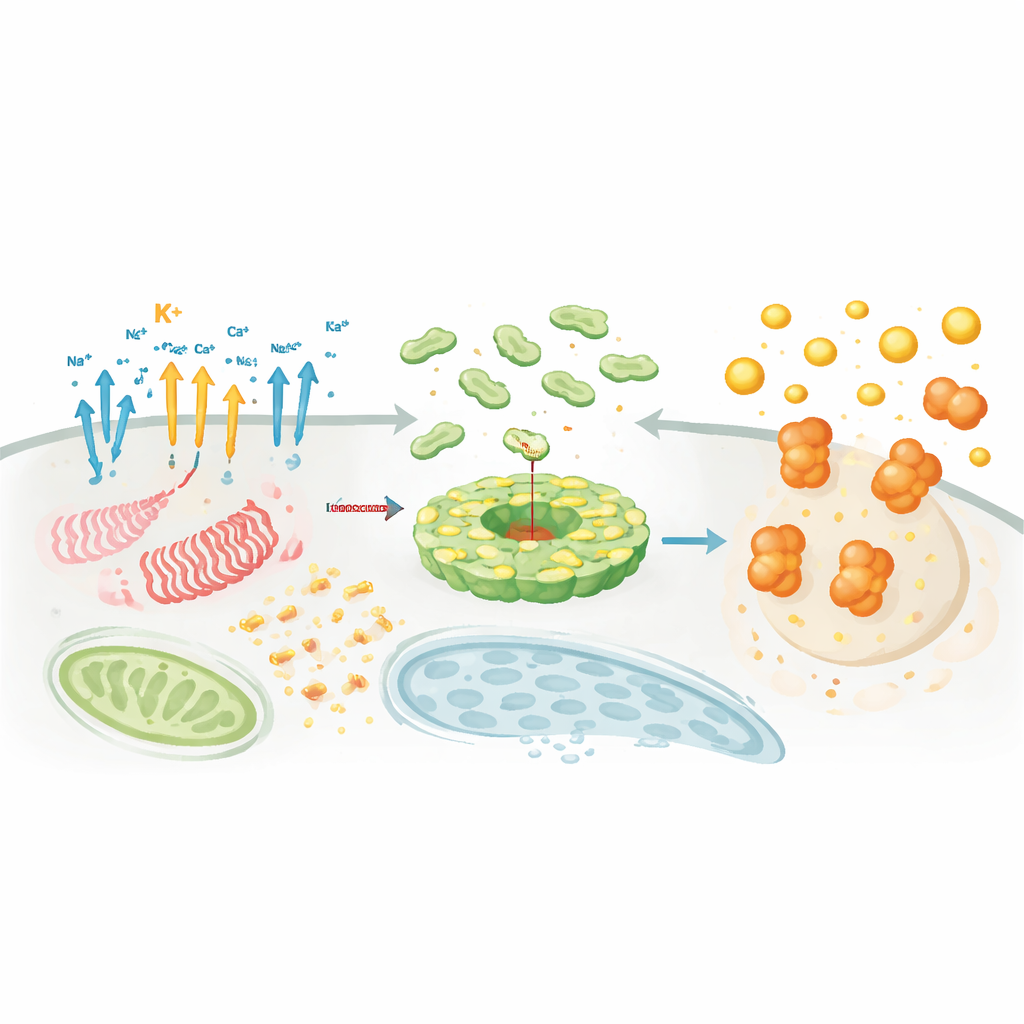
Gdzie i kiedy kompleks się składa
Ponad sygnałami chemicznymi, kluczowe są lokalizacja i czas. NLRP3 i jego partnerzy przemieszczają się między organellami, przemieszczając się po wewnętrznym szkielecie komórki, aby gromadzić się w określonych węzłach, takich jak sieć trans-Golgiego i ośrodek organizacji mikrotubul. Tam białka pomocnicze, jak NEK7, działają jako „czynniki uprawniające”, które przekształcają NLRP3 z autozahamowanej klatki w aktywną formę zdolną do wiązania ASC. Modyfikacje lipidowe, takie jak palmitoilacja, oraz oddziaływania elektrostatyczne z określonymi lipidami błonowymi kierują NLRP3 we właściwe miejsce we właściwym czasie. Równolegle do tej choreografii dziesiątki enzymów przyłączają lub usuwają regulatoryczne znaczniki — łańcuchy ubikwityny, grupy fosforanowe, znaki acetylowe i białka SUMO — które doprecyzowują ilość NLRP3, jego stabilność i zdolność do łączenia się z ASC i kaspazą-1. Gęsta sieć regulacyjna tłumaczy, dlaczego NLRP3 może być wyjątkowo wrażliwy na kontekst, typ komórki i stan chorobowy.
Równoważenie pomocy i szkody
Ponieważ nadaktywność inflamasomu może być równie niebezpieczna jak infekcja, komórki stosują także hamulce. Wiele białek wiąże się z NLRP3 lub jego kofaktorami, blokując kluczowe interakcje, kierując go do degradacji lub zapobiegając jego agregacji, podczas gdy inne wzmacniają jego składanie w obliczu rzeczywistego zagrożenia. Przegląd kataloguje tych pozytywnych i negatywnych partnerów i pokazuje, że subtelne defekty — zbyt dużo modyfikacji aktywujących lub zbyt mało hamujących — mogą przesunąć system w stronę przewlekłego zapalenia. Autorzy argumentują, że zrozumienie współdziałania tych wszystkich przełączników będzie kluczowe dla projektowania terapii. Celując w konkretne enzymy modyfikujące NLRP3 lub jego pomocników, przyszłe leki mogłyby selektywnie stłumić inflamasom w określonych tkankach lub chorobach, zachowując jego ratującą życie rolę w obronie gospodarza i jednocześnie zapobiegając szkodom ubocznym obserwowanym w wielu schorzeniach zapalnych i zwyrodnieniowych.
Cytowanie: Shin, H.J., Kim, I.S., Kim, J.K. et al. Molecular mechanisms of NLRP3 inflammasome activation. Exp Mol Med 58, 650–663 (2026). https://doi.org/10.1038/s12276-026-01656-9
Słowa kluczowe: inflammasom NLRP3, odporność wrodzona, zapalenie, modyfikacja potranslacyjna, immunometabolizm