Clear Sky Science · ja
NLRP3インフラマソーム活性化の分子機構
なぜ細胞は分子レベルの火災報知器を鳴らすのか
私たちの体は、最前線に立つ免疫細胞に侵入する微生物、有害な粒子、あるいは内部のストレスを素早く察知して警報を上げてもらうことに頼っています。最も強力な警報スイッチの一つがNLRP3インフラマソームと呼ばれるタンパク質装置です。これが作動すると、感染から守る炎症反応が引き起こされます。しかし、このスイッチが「オン」のまま固定されると、痛風や糖尿病から神経変性まで幅広い疾患を促進する可能性があります。本レビューは、NLRP3インフラマソームがどのように構成され、何がこれを作動させ、細胞がその活性をどのように精密に調整しているかを分子レベルで解説し、有益な防御を損なうことなく有害な炎症を抑える将来の薬剤設計に示唆を与えます。
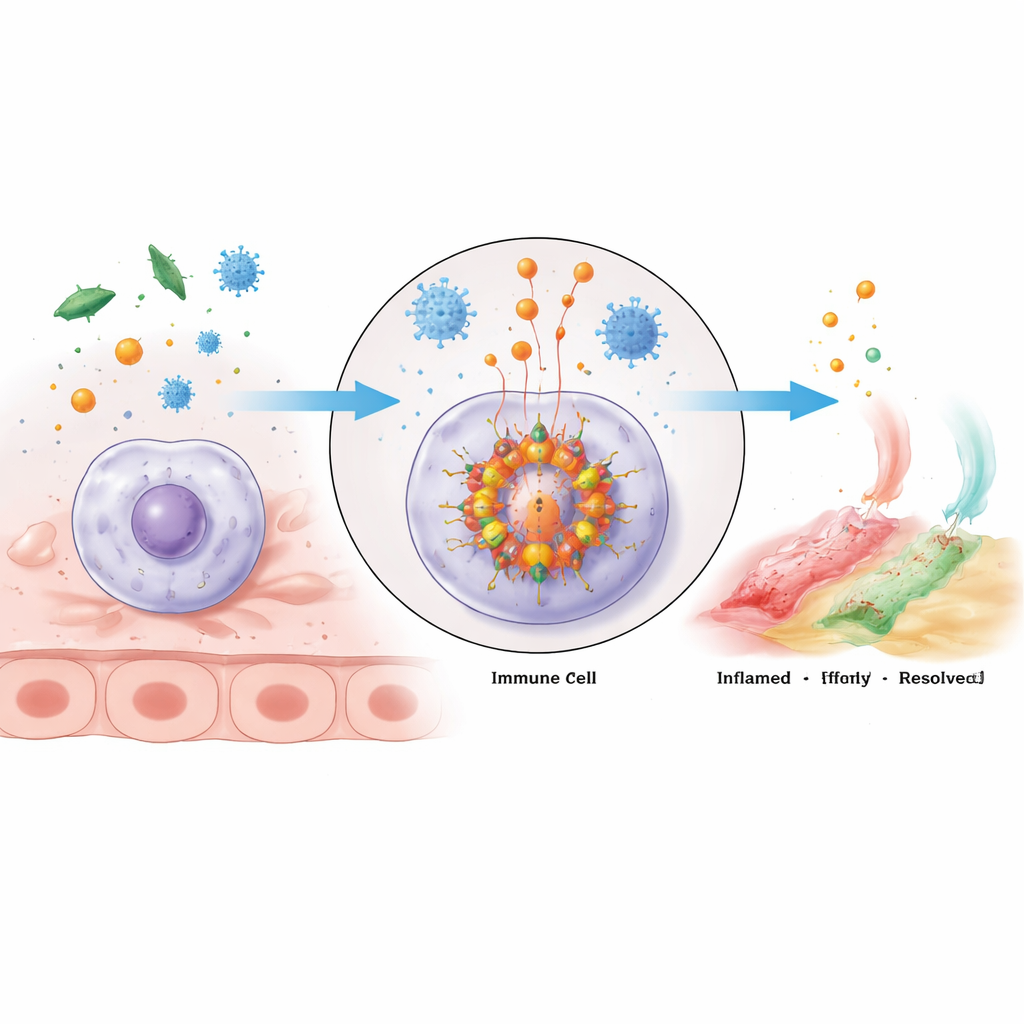
免疫細胞内の分子アラームクラスター
NLRP3インフラマソームは、危険を感知した免疫細胞内で組み立てられる大型の多タンパク質クラスターです。その中核はセンサータンパク質NLRP3、アダプターであるASC、酵素カスパーゼ‑1で構成されます。NLRP3は複数の領域を持ち、それぞれ異なる役割を担います:一端はASCと結合し、中間領域はエネルギーを持つATPを結合してNLRP3ユニットの集合を促し、末端は危険が現れるまでセンサーを抑制するのに寄与します。活性化されるとNLRP3分子はオリゴマー化して集合し、ASCを呼び寄せます。ASCはフィラメント状の足場を形成してカスパーゼ‑1を引き込みます。こうして集合したカスパーゼ‑1は活性化され、強力な炎症性メッセンジャーであるIL‑1βやIL‑18の不活性前駆体を切断するとともに、細胞膜に穴を開けることができるガスデルミンDというタンパク質を切断します。これが発火的でしばしば致死的な炎症反応、すなわちパイロトーシスを生み出します。
二つの青信号:準備と発火
NLRP3のオン化は単一のイベントではなく、二段階のプロセスです。第一段階のプライミングは、微生物や炎症性ホルモンを感知する受容体が働いたときに起こります。これらのシグナルは転写因子NF‑κBを活性化し、NLRP3そのものや不活性のサイトカイン前駆体であるIL‑1βやIL‑18の産生を増加させます。同時に、リン酸化、ユビキチン付加・切除、SUMO、アセチル、脂質、ADP‑リボースといった化学的な修飾群(翻訳後修飾)の網がNLRP3に「認可」を与え、危険の直前であるがまだ有害でない準備状態に置きます。第二段階の活性化は、細胞外ATP、細菌毒素、シリカや尿酸のような針状結晶、ミトコンドリアストレス、リソソーム破裂など多様な刺激によって引き起こされます。これら異なるトリガーは、特に膜を横切るイオン移動、ミトコンドリア機能障害、内部コンパートメントの損傷などの共通する細胞変化に収束し、インフラマソーム複合体の物理的な組み立てとカスパーゼ‑1の完全な活性化を促します。
イオン、発電所、リサイクル施設が物語に加わる
NLRP3は多様な脅威に反応しますが、繰り返し現れるいくつかの核心的プロセスがあります。ひとつは電荷を持つイオンの流れです。細胞からのカリウムの損失は最も一貫した活性化因子であり、ナトリウム、塩化物、カルシウムの特殊なチャネルを介した移動によって補助または調節されます。別の重要因子はミトコンドリアの障害で、損傷した「発電所」は活性酸素種やミトコンドリアDNAの断片を放出してNLRP3のリクルートと活性化を助けます。メトホルミンのような薬剤はこのミトコンドリアシグナルを弱めることができます。三つ目はリソソームの損傷で、細胞が鋭利な粒子を貪食した際に起こりうるこのリサイクル施設の破裂は、酵素やイオンを放出してさらにNLRP3活性化を促進します。一方で、細胞代謝の変化――細胞がグルコース、脂肪、その他の燃料を燃やす方法――はインフラマソーム活性を加速または抑制し得ます。スクシネートやパルミチン酸のようないくつかの代謝産物は炎症を駆動し、イタコネート、フマル酸、ケトン体のような別の代謝物はそれを抑える働きを持ちます。
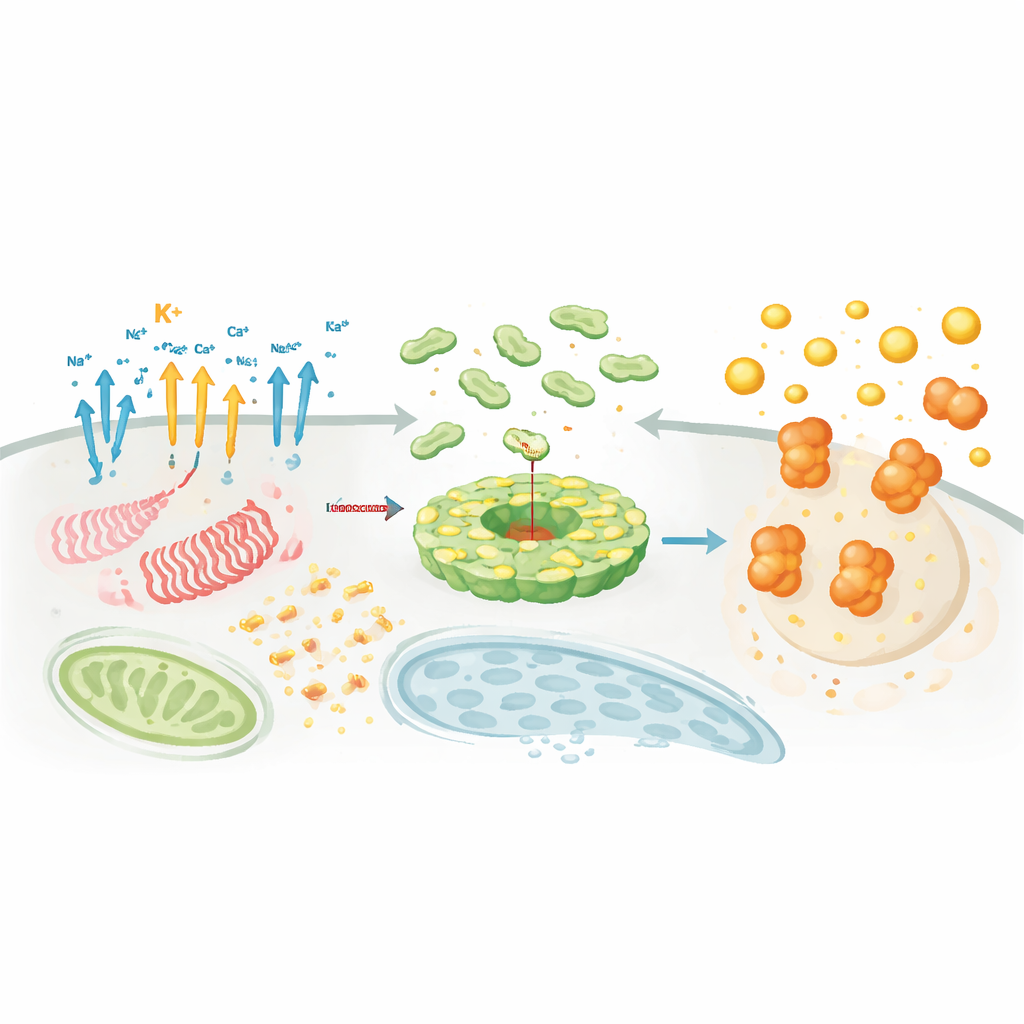
複合体が組み立てられる場所とタイミング
化学的シグナルを超えて、場所と時間は重要です。NLRP3とそのパートナーは細胞小器官間を移動し、細胞内部の足場に沿って輸送されてトランス‑ゴルジ網や微小管組織化中心のような特定のハブに集まります。そこでNEK7のような補助タンパク質が「認可因子」として働き、自己抑制された籠からASCと結合可能な活性型の円盤へとNLRP3の形を変えます。パルミトイル化のような脂質修飾や特定の膜脂質との静電相互作用は、NLRP3を適切な場所に適切なタイミングで導きます。並行して、数十種類の酵素がユビキチン鎖、リン酸基、アセチル基、SUMOといった調節タグを付加または除去し、NLRP3の量、安定性、ASCやカスパーゼ‑1との結合能を精密に調整します。この濃密な調節ネットワークが、NLRP3が文脈、細胞種、疾患状態に非常に敏感に反応する理由を説明します。
助けと害のバランスを取る
過剰に活性化したインフラマソームは感染と同じくらい危険であり得るため、細胞はブレーキも備えています。多くのタンパク質がNLRP3やその共役因子に結合して重要な相互作用を阻害したり、分解へ向けて経路付けしたり、クラスター化を防いだりします。一方で、真正の脅威下では組み立てを促進する因子も存在します。本レビューはこれらの促進的および抑制的パートナーを列挙し、活性化修飾の過剰や抑制修飾の不足といった微妙な欠陥が慢性炎症へと傾け得ることを示します。著者らは、これらすべてのスイッチがどのように相互作用するかを理解することが治療法設計に不可欠であると論じます。NLRP3やその補助因子を修飾する特定の酵素を標的にすることで、将来の薬剤は特定の組織や疾患においてインフラマソームを選択的に抑え、宿主防御という生命維持的役割を残しつつ多くの炎症性・変性疾患で見られる副次的な損傷を防げる可能性があります。
引用: Shin, H.J., Kim, I.S., Kim, J.K. et al. Molecular mechanisms of NLRP3 inflammasome activation. Exp Mol Med 58, 650–663 (2026). https://doi.org/10.1038/s12276-026-01656-9
キーワード: NLRP3インフラマソーム, 自然免疫, 炎症, 翻訳後修飾, 免疫代謝