Clear Sky Science · ru
Молекулярные механизмы активации инфламмасомы NLRP3
Зачем нашим клеткам молекулярная пожарная сигнализация
Наш организм рассчитывает на передовые иммунные клетки, которые замечают угрозу — вторжение микробов, токсичные частицы или внутренний стресс — и быстро поднимают тревогу. Один из самых мощных переключателей тревоги — белковая машина, называемая инфламмасомой NLRP3. Когда она включается, это вызывает воспаление, которое может спасти нас от инфекции. Но если этот переключатель застрянет в положении «включено», он способен привести к множеству заболеваний — от подагры и диабета до нейродегенерации. В этом обзоре подробно объясняется, как устроена инфламмасома NLRP3, что её включает и как клетки тонко регулируют её активность, давая подсказки для будущих препаратов, которые остудят вредное воспаление, не подавив полезную защиту.
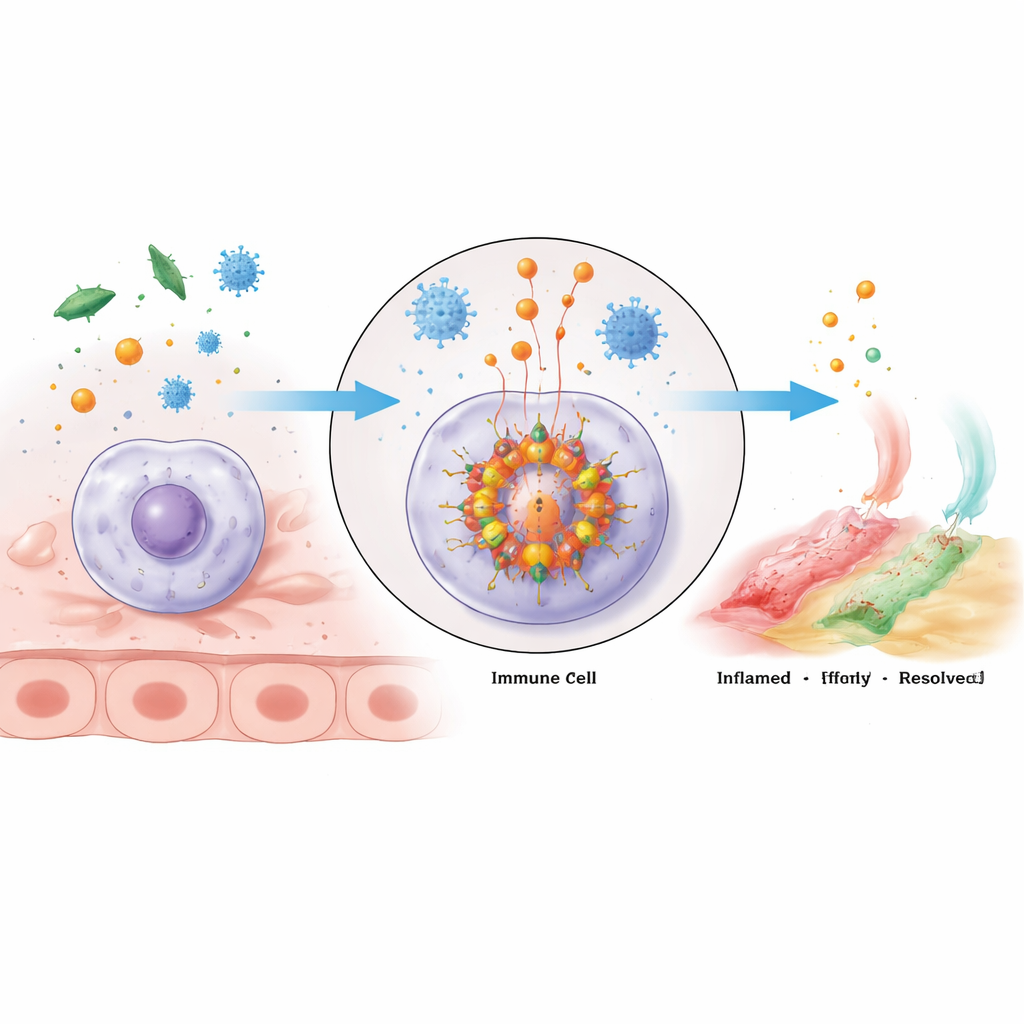
Молекулярный кластер‑сигнал внутри иммунных клеток
Инфламмасома NLRP3 — это большой многобелковый кластер, который собирается внутри иммунных клеток при обнаружении опасности. В его ядре находятся сенсорный белок NLRP3, адаптер ASC и фермент каспаза‑1. У NLRP3 есть несколько областей с разными функциями: один конец связывается с ASC, средняя часть связывает энергоёмкий ATP и помогает единицам NLRP3 объединяться, а хвост помогает держать сенсор в выключенном состоянии до появления беды. При активации молекулы NLRP3 олигомеризуются — собираются в комплексы — и привлекают ASC, который формирует нитевидные каркасы, затем привлекающие каспазу‑1. Оказавшись в кластере, каспаза‑1 активируется и расщепляет неактивные прекурсоры мощных провоспалительных медиаторов IL‑1β и IL‑18, а также белок газдермин D, который может проделывать отверстия в мембране клетки, вызывая яркую, часто смертельную воспалительную реакцию — пироптоз.
Два зелёных сигнала: подготовка и выстрел
Включение NLRP3 — это не единичное событие, а двухэтапный процесс. Первый этап, называемый праймингом, происходит, когда активируются рецепторы, распознающие микробы или воспалительные гормоны. Эти сигналы активируют фактор транскрипции NF‑κB, который усиливает синтез самого NLRP3 и неактивных прекурсоров цитокинов IL‑1β и IL‑18. Одновременно сеть химических модификаций, называемых посттрансляционными модификациями — таких как добавление или удаление фосфата, убиквитина, SUMO, ацетил, липидных или ADP‑рибозных групп — «лицензирует» NLRP3, переводя его в готовое, но ещё не опасное состояние. Второй этап, активация, вызывается широким набором стимулов: внеклеточным ATP, бактериальными токсинами, игольчатыми кристаллами, такими как кремнезём или мочевая кислота, митохондриальным стрессом, разрывом лизосом и другими. Эти разнообразные триггеры сходятся в общих клеточных изменениях — особенно в ионных потоках через мембрану, дисфункции митохондрий и повреждении внутренних компартментов — которые стимулируют физическую сборку комплекса инфламмасомы и полную активацию каспазы‑1.
Ионы, энергетические станции и перерабатывающие центры входят в игру
Хотя NLRP3 реагирует на множество угроз, несколько ключевых процессов повторяются. Один из них — поток заряженных ионов. Потеря калия из клетки — наиболее последовательный активатор, которому помогают или которым модулируют натрий, хлор и кальций, перемещающиеся через специализированные каналы. Другой — дисфункция митохондрий: повреждённые «электростанции» высвобождают реактивные формы кислорода и фрагменты митохондриальной ДНК, которые способствуют рекрутированию и активации NLRP3, и такие препараты, как метформин, могут ослаблять этот митохондриальный сигнал. Третья — повреждение лизосом, которое может возникать при поглощении острых частиц; разрыв этих перерабатывающих центров высвобождает ферменты и ионы, дополнительно стимулирующие активацию NLRP3. Параллельно изменения клеточного метаболизма — то, как клетки расщепляют глюкозу, жиры и другие топлива — могут либо ускорять, либо тормозить активность инфламмасомы: некоторые метаболиты, такие как сукцинат и пальмитат, усиливают воспаление, тогда как другие, например итаконат, фумарат или кетоновые тела, сдерживают его.
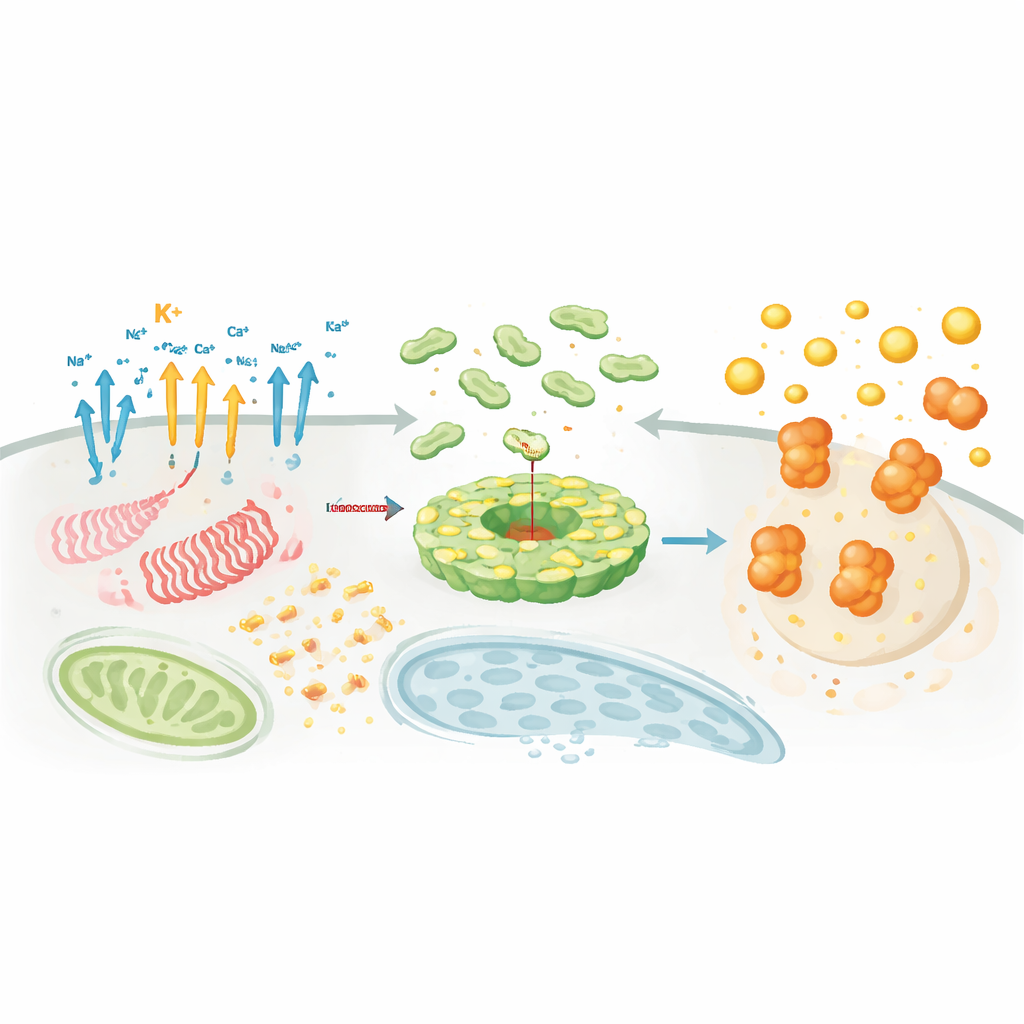
Где и когда собирается комплекс
Помимо химических сигналов, важны местоположение и время. NLRP3 и его партнёры перемещаются между органеллами, используя внутренний каркас клетки, чтобы собираться в специфических узлах, таких как транс‑Гольджи сеть и центр организации микротрубочек. Там вспомогательные белки, например NEK7, действуют как «факторы лицензирования», перестраивая NLRP3 из автоингибированной клетки в активный диск, способный связываться с ASC. Липидные модификации, такие как палмитоилация, и электростатические взаимодействия с определёнными липидами мембраны направляют NLRP3 в нужное место в нужное время. Параллельно десятки ферментов присоединяют или удаляют регуляторные метки — убиквитиновые цепи, фосфатные группы, ацетильные метки и SUMO — которые точно настраивают количество NLRP3, его стабильность и способность взаимодействовать с ASC и каспазой‑1. Эта плотная сеть регуляции объясняет, почему NLRP3 может быть исключительно чувствителен к контексту, типу клетки и состоянию болезни.
Баланс между помощью и вредом
Поскольку гиперактивная инфламмасома может быть так же опасна, как и инфекция, клетки также располагают тормозами. Многие белки связываются с NLRP3 или его кофакторами, чтобы блокировать ключевые взаимодействия, направлять его на деградацию или предотвращать его кластеризацию, в то время как другие усиливают его сборку при реальной угрозе. Обзор систематизирует эти положительные и отрицательные партнёрские взаимодействия и показывает, что тонкие дефекты — слишком много активирующей модификации или недостаток ингибирующей — могут сдвинуть систему в сторону хронического воспаления. Авторы утверждают, что понимание того, как взаимодейстуют все эти переключатели, будет жизненно важно для разработки терапий. Нацелив конкретные ферменты, которые модифицируют NLRP3 или его вспомогательные белки, будущие препараты могли бы избирательно охлаждать инфламмасому в определённых тканях или при конкретных заболеваниях, сохраняя её жизненно важную роль в защите хозяина и предотвращая сопутствующее повреждение, наблюдаемое при многих воспалительных и дегенеративных расстройствах.
Цитирование: Shin, H.J., Kim, I.S., Kim, J.K. et al. Molecular mechanisms of NLRP3 inflammasome activation. Exp Mol Med 58, 650–663 (2026). https://doi.org/10.1038/s12276-026-01656-9
Ключевые слова: инфламмасома NLRP3, врожденный иммунитет, воспаление, посттрансляционная модификация, иммунометаболизм