Clear Sky Science · it
Meccanismi molecolari dell’attivazione dell’inflammasoma NLRP3
Perché le nostre cellule accendono un allarme molecolare
I nostri corpi si affidano alle cellule immunitarie di prima linea per riconoscere i pericoli—microrganismi invasivi, particelle tossiche o stress interno—e dare l’allarme rapidamente. Uno degli interruttori d’allarme più potenti è una macchina proteica chiamata inflammasoma NLRP3. Quando si attiva, innesca un’infiammazione che può salvarci dalle infezioni. Ma se questo interruttore resta bloccato nella posizione “acceso”, può alimentare una lunga lista di malattie, dalla gotta e il diabete alla neurodegenerazione. Questo articolo di recensione spiega, in dettaglio molecolare, come è costruito l’inflammasoma NLRP3, cosa lo attiva e come le cellule ne regolano finemente l’attività, offrendo indizi per futuri farmaci che raffreddino l’infiammazione dannosa senza spegnere le difese utili.
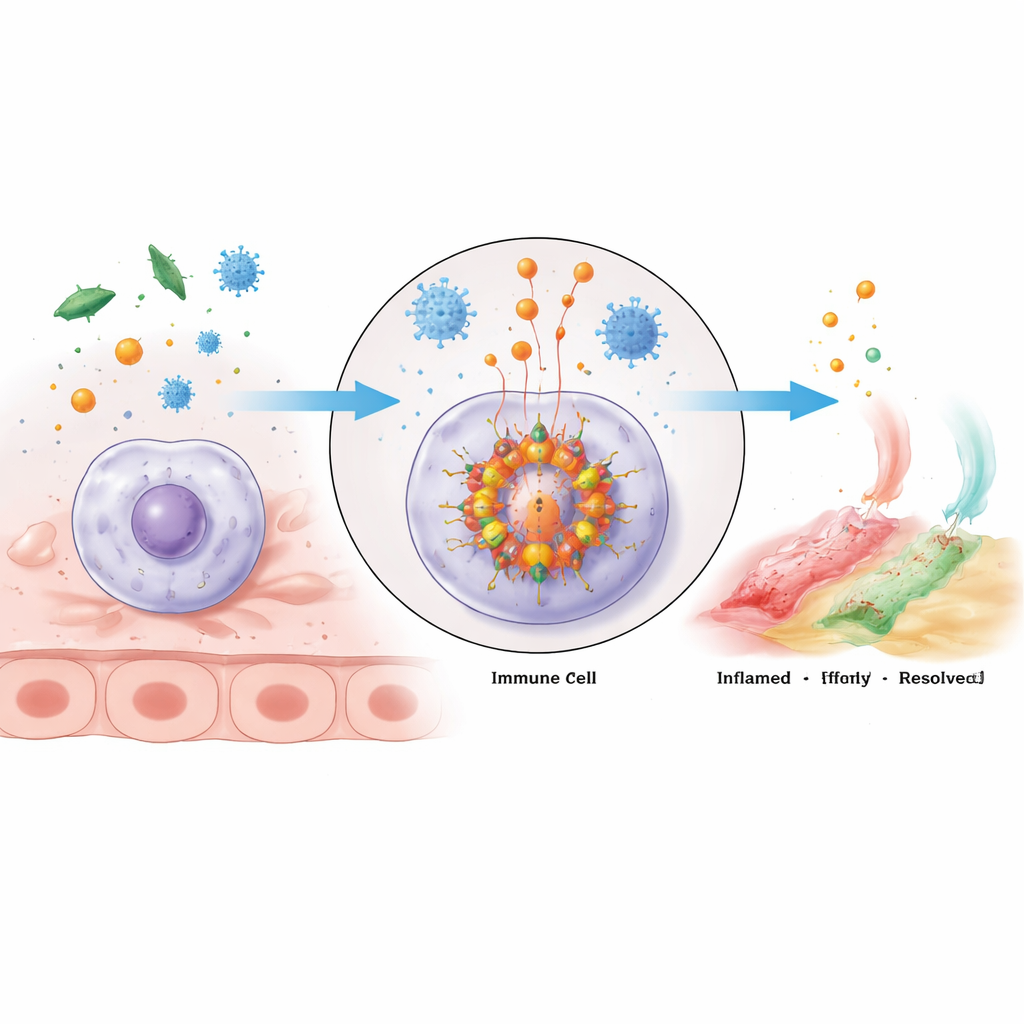
Un ammasso di allarme molecolare all’interno delle cellule immunitarie
L’inflammasoma NLRP3 è un grande ammasso multiproteico che si assembla all’interno delle cellule immunitarie quando queste rilevano un pericolo. Il suo nucleo è costituito dalla proteina sensore NLRP3, da un adattatore chiamato ASC e dall’enzima caspasi‑1. NLRP3 possiede diverse regioni con compiti distinti: un’estremità si collega ad ASC, la porzione centrale lega l’ATP ricco di energia e favorisce l’aggregazione delle unità NLRP3, e la coda contribuisce a mantenere il sensore spento finché non compare il pericolo. Quando si attiva, le molecole di NLRP3 oligomerizzano—si raggruppano—e reclutano ASC, che forma impalcature filiformi che attirano poi la caspasi‑1. Una volta radunata, la caspasi‑1 si attiva e taglia i precursori inattivi dei potenti messaggeri infiammatori IL‑1β e IL‑18, oltre a una proteina chiamata gasdermina D che può perforare la membrana cellulare, producendo una risposta infiammatoria intensa e spesso letale chiamata piroptosi.
Due semafori verdi: preparazione e scatto
L’attivazione di NLRP3 non è un singolo evento ma un processo in due fasi. Il primo passo, detto priming, si verifica quando vengono attivati recettori che riconoscono microbi o ormoni infiammatori. Questi segnali attivano il fattore di trascrizione NF‑κB, che aumenta la produzione dello stesso NLRP3 e dei precursori inattivi delle citochine IL‑1β e IL‑18. Contemporaneamente, una rete di modifiche chimiche chiamate modificazioni post‑traduzionali—come l’aggiunta o la rimozione di gruppi fosfato, ubiquitina, SUMO, acetile, lipidi o ADP‑ribosio—“autorizzano” NLRP3, collocandolo in uno stato pronto ma non ancora pericoloso. Il secondo passo, l’attivazione, è innescato da una vasta gamma di stimoli: ATP extracellulare, tossine batteriche, cristalli appuntiti come silice o acido urico, stress mitocondriale, rottura lisosomiale e altro. Questi diversi segnali convergono su cambiamenti cellulari comuni—soprattutto movimenti ionici attraverso la membrana, disfunzione mitocondriale e danni agli compartimenti interni—che guidano l’assemblaggio fisico del complesso inflammasoma e l’attivazione completa della caspasi‑1.
Ioni, centrali energetiche e centri di riciclaggio entrano in scena
Anche se NLRP3 risponde a molteplici minacce, emergono ricorrentemente alcuni processi fondamentali. Uno è il flusso di ioni carichi. La perdita di potassio dalla cellula è l’attivatore più coerente, modulata o sostenuta dai movimenti di sodio, cloruro e calcio attraverso canali specializzati. Un altro è il disagio mitocondriale: i “motori” danneggiati rilasciano specie reattive dell’ossigeno e frammenti di DNA mitocondriale che favoriscono il reclutamento e l’attivazione di NLRP3, e farmaci come la metformina possono attenuare questo segnale mitocondriale. Un terzo è il danno lisosomiale, che può verificarsi quando le cellule ingestiscono particelle appuntite; la rottura di questi centri di riciclaggio libera enzimi e ioni che promuovono ulteriormente l’attivazione di NLRP3. Nel frattempo, il cambiamento del metabolismo cellulare—come la cellula brucia glucosio, lipidi e altri carburanti—può accelerare o frenare l’attività dell’inflammasoma: alcuni metaboliti come succinato e palmitato guidano l’infiammazione, mentre altri come itaconato, fumarato o corpi chetonici la limitano.
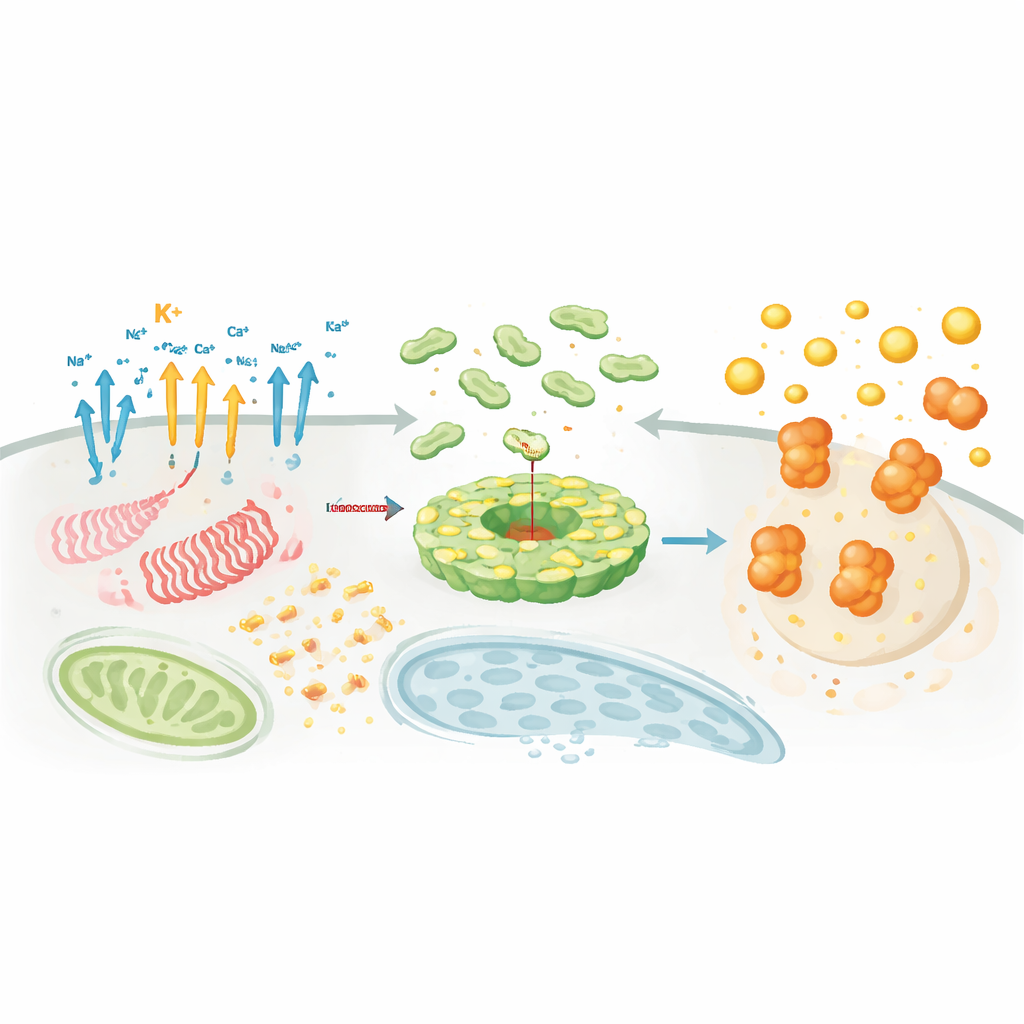
Dove e quando il complesso si assembla
Oltre ai segnali chimici, posizione e tempistica sono cruciali. NLRP3 e i suoi partner si spostano tra gli organelli, viaggiando lungo lo scheletro interno della cellula per radunarsi in hub specifici come il trans‑Golgi network e il centro organizzatore dei microtubuli. In questi siti, proteine ausiliarie come NEK7 agiscono come “fattori di autorizzazione” che rimodellano NLRP3 da una gabbia autoinibita a un disco attivo in grado di legare ASC. Modifiche lipidiche, come la palmitoilazione, e interazioni elettrostatiche con particolari lipidi di membrana indirizzano NLRP3 nel posto giusto al momento giusto. Parallelamente a questa coreografia, dozzine di enzimi aggiungono o rimuovono etichette regolatorie—catene di ubiquitina, gruppi fosfato, marche acetiliche e proteine SUMO—that modulano la quantità di NLRP3, la sua stabilità e la capacità di associarsi con ASC e caspasi‑1. Questa rete regolatoria densa spiega perché NLRP3 può essere estremamente sensibile al contesto, al tipo cellulare e allo stato di malattia.
Bilanciare aiuto e danno
Poiché un inflammasoma iperattivo può essere pericoloso quanto un’infezione, le cellule dispongono anche di freni. Molte proteine si legano a NLRP3 o ai suoi co‑fattori per bloccare interazioni chiave, indirizzarlo alla degradazione o impedire la sua aggregazione, mentre altre ne favoriscono l’assemblaggio in presenza di una minaccia reale. La recensione cataloga questi partner positivi e negativi e mostra che difetti sottili—troppa di una modifica attivante o troppo poca di una inibitoria—possono spingere il sistema verso un’infiammazione cronica. Gli autori sostengono che comprendere come tutti questi interruttori interagiscono sarà fondamentale per progettare terapie. Mirando a enzimi specifici che modificano NLRP3 o i suoi aiutanti, i farmaci futuri potrebbero raffreddare selettivamente l’inflammasoma in tessuti o malattie particolari, preservando il suo ruolo vitale nella difesa dell’ospite e prevenendo il danno collaterale osservato in molte patologie infiammatorie e degenerative.
Citazione: Shin, H.J., Kim, I.S., Kim, J.K. et al. Molecular mechanisms of NLRP3 inflammasome activation. Exp Mol Med 58, 650–663 (2026). https://doi.org/10.1038/s12276-026-01656-9
Parole chiave: inflammasoma NLRP3, immunità innata, infiammazione, modificazione post‑traduzionale, immunometabolismo