Clear Sky Science · de
Molekulare Mechanismen der Aktivierung des NLRP3-Inflammasoms
Warum unsere Zellen einen molekularen Feuermelder auslösen
Unser Körper ist auf Abwehrzellen an der Frontlinie angewiesen, die Probleme bemerken — eindringende Mikroben, giftige Partikel oder innerer Stress — und schnell Alarm schlagen. Einer der stärksten Alarmknöpfe ist eine Proteineinheit namens NLRP3-Inflammasom. Sobald sie aktiviert ist, löst sie eine Entzündungsreaktion aus, die uns vor Infektionen retten kann. Bleibt dieser Schalter jedoch dauerhaft an, kann er eine Vielzahl von Erkrankungen antreiben, von Gicht und Diabetes bis hin zu Neurodegeneration. Dieser Übersichtsartikel erklärt auf molekularer Ebene, wie das NLRP3-Inflammasom aufgebaut ist, was es aktiviert und wie Zellen seine Aktivität feinregeln — Hinweise, die künftige Medikamente liefern könnten, um schädliche Entzündungen zu dämpfen, ohne nützliche Abwehrmechanismen stummzuschalten.
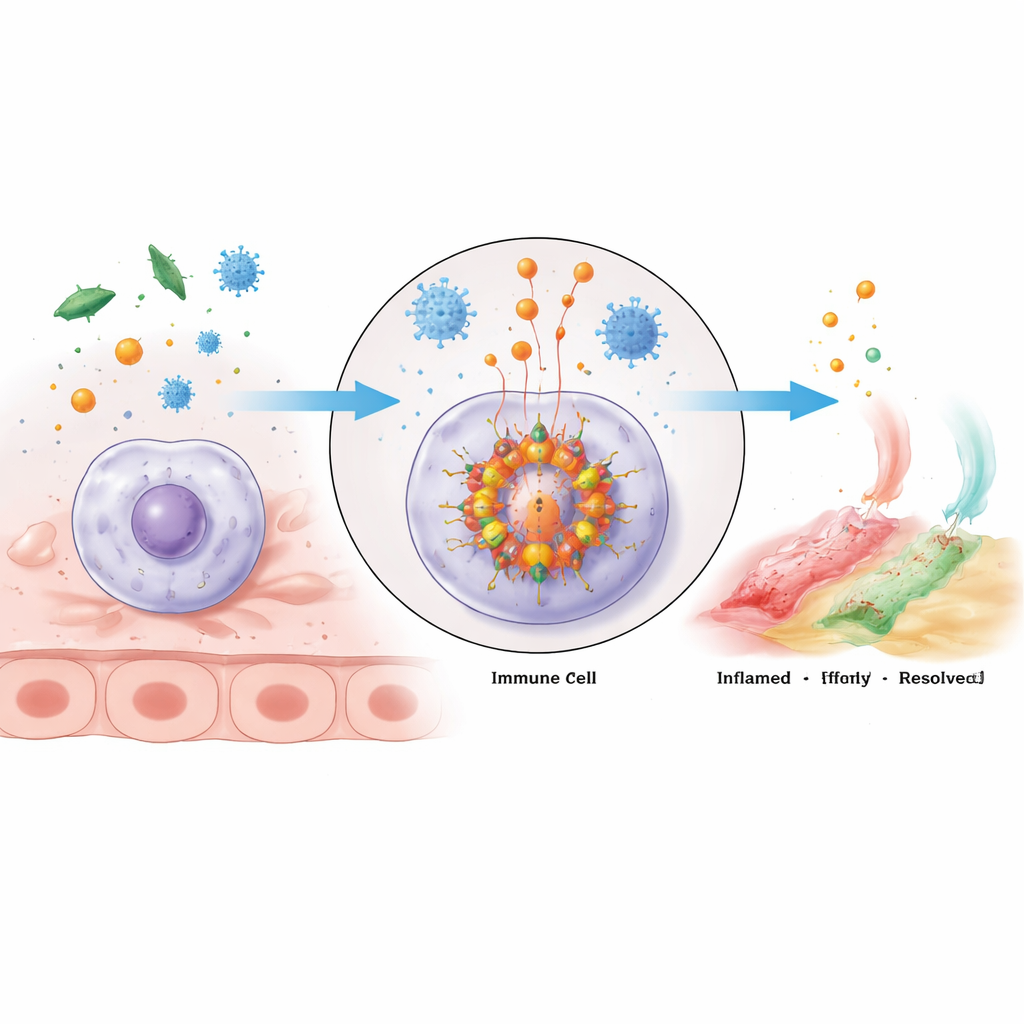
Ein molekularer Alarmschalter in Immunzellen
Das NLRP3-Inflammasom ist ein großer Mehrprotein-Komplex, der sich in Immunzellen zusammenbaut, wenn diese Gefahr erkennen. Sein Kern besteht aus dem Sensorprotein NLRP3, einem Adapter namens ASC und dem Enzym Caspase‑1. NLRP3 besitzt mehrere Domänen mit unterschiedlichen Aufgaben: ein Ende verbindet sich mit ASC, der Mittelteils bindet energiereiches ATP und fördert die Zusammenlagerung der NLRP3-Einheiten, und das C-Terminus hilft, den Sensor ausgeschaltet zu halten, bis Gefahr eintritt. Bei Aktivierung oligomerisieren NLRP3-Moleküle — sie gruppieren sich — und rekrutieren ASC, das filamentartige Gerüste bildet, die dann Caspase‑1 anziehen. Einmal zusammengeführt, wird Caspase‑1 aktiviert und spaltet inaktive Vorläufer der potenten Entzündungsmediatoren IL‑1β und IL‑18 sowie ein Protein namens Gasdermin D, das Poren in die Zellmembran schlagen kann und so eine heftige, oft tödliche inflammatorische Reaktion namens Pyroptose erzeugt.
Zwei grüne Signale: Vorbereitung und Auslösung
Die Aktivierung von NLRP3 ist kein Einzelereignis, sondern ein zweistufiger Prozess. Der erste Schritt, Priming genannt, erfolgt, wenn Rezeptoren, die Mikroben oder entzündliche Hormone erkennen, aktiviert werden. Diese Signale aktivieren den Transkriptionsfaktor NF‑κB, der die Produktion von NLRP3 selbst sowie der inaktiven Zytokinvorstufen IL‑1β und IL‑18 erhöht. Gleichzeitig „lizenzieren“ ein Netz chemischer Modifikationen — posttranslationale Modifikationen wie Hinzufügen oder Entfernen von Phosphat-, Ubiquitin-, SUMO-, Acetyl-, Lipid- oder ADP‑Ribose-Gruppen — NLRP3 und bringen es in einen bereitstehenden, aber noch nicht gefährlichen Zustand. Der zweite Schritt, die Aktivierung, wird durch eine breite Palette von Stimuli ausgelöst: extrazelluläres ATP, bakterielle Toxine, nadelähnliche Kristalle wie Silika oder Harnsäure, mitochondriale Stresssignale, Lysosomenriss und mehr. Diese unterschiedlichen Auslöser laufen auf gemeinsame zelluläre Veränderungen hinaus — insbesondere Ionenbewegungen über die Membran, mitochondriale Dysfunktion und Beschädigung interner Kompartimente — die den physischen Zusammenbau des Inflammasomkomplexes und die vollständige Aktivierung von Caspase‑1 vorantreiben.
Ionen, Kraftwerke und Recyclingzentren spielen mit
Obwohl NLRP3 auf viele verschiedene Gefahren reagiert, tauchen mehrere Kernprozesse immer wieder auf. Einer ist der Fluss geladener Ionen. Der Verlust von Kalium aus der Zelle ist der beständigste Aktivator, unterstützt oder moduliert durch Bewegungen von Natrium, Chlorid und Calcium über spezialisierte Kanäle. Ein anderer ist mitochondriale Belastung: beschädigte ‘‘Kraftwerke‘‘ setzen reaktive Sauerstoffspezies und Fragmente mitochondrialer DNA frei, die helfen, NLRP3 zu rekrutieren und zu aktivieren, und Wirkstoffe wie Metformin können dieses mitochondriale Signal abschwächen. Drittens kann lysosomale Schädigung auftreten, wenn Zellen scharfe Partikel aufnehmen; das Aufbrechen dieser Recyclingzentren setzt Enzyme und Ionen frei, die die NLRP3-Aktivierung weiter fördern. Parallel dazu kann sich der zelluläre Stoffwechsel — wie Zellen Glukose, Fette und andere Brennstoffe verstoffwechseln — entweder beschleunigend oder hemmend auf das Inflammasom auswirken: manche Metaboliten wie Succinat und Palmitat fördern Entzündung, andere wie Itaconat, Fumarat oder Ketonkörper dämpfen sie.
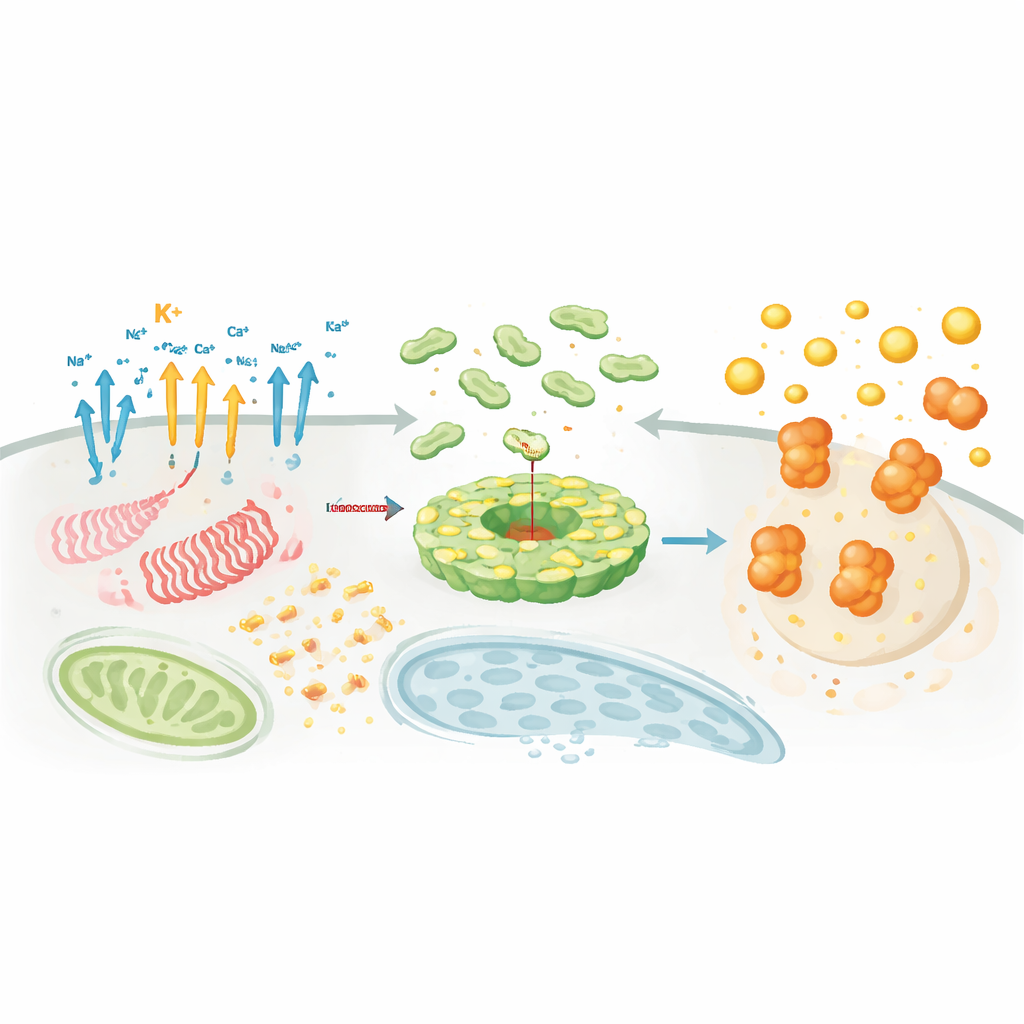
Wo und wann sich der Komplex zusammenfindet
Über chemische Signale hinaus sind Ort und Zeitpunkt entscheidend. NLRP3 und seine Partner bewegen sich zwischen Organellen und reisen entlang des zellulären Gerüsts, um sich an bestimmten Knotenpunkten wie dem trans‑Golgi‑Netzwerk und dem Mikrotubuli‑Organisationszentrum zu versammeln. Dort wirken Hilfsproteine wie NEK7 als „Lizenzfaktoren“, die NLRP3 von einem autoinhibierten Käfig in eine aktive Scheibe umbauen, die ASC binden kann. Lipidmodifikationen, etwa Palmitoylierung, und elektrostatische Wechselwirkungen mit bestimmten Membranlipiden lenken NLRP3 zum richtigen Ort zur richtigen Zeit. Parallel zu dieser Choreografie heften dutzende Enzyme regulatorische Markierungen an oder entfernen sie — Ubiquitinketten, Phosphatgruppen, Acetylreste und SUMO‑Proteine — die NLRP3-Menge, Stabilität und seine Fähigkeit, mit ASC und Caspase‑1 zu interagieren, feinjustieren. Dieses dichte Regulationsnetz erklärt, warum NLRP3 äußerst sensitiv gegenüber Kontext, Zelltyp und Krankheitszustand sein kann.
Hilfe und Schaden ausbalancieren
Da ein überaktives Inflammasom ebenso gefährlich sein kann wie eine Infektion, setzen Zellen auch Bremsen ein. Viele Proteine binden NLRP3 oder seine Cofaktoren, um Schlüsselinteraktionen zu blockieren, es für den Abbau zu markieren oder seine Aggregation zu verhindern, während andere seine Assemblierung bei echter Bedrohung fördern. Die Übersicht katalogisiert diese positiven und negativen Partner und zeigt, dass subtile Defekte — zu viel einer aktivierenden Modifikation oder zu wenig einer hemmenden — das System in Richtung chronischer Entzündung kippen können. Die Autoren argumentieren, dass das Verständnis, wie all diese Schalter zusammenwirken, entscheidend für die Entwicklung von Therapien sein wird. Durch das gezielte Ansteuern bestimmter Enzyme, die NLRP3 oder seine Helfer modifizieren, könnten künftige Medikamente das Inflammasom in bestimmten Geweben oder Krankheiten selektiv dämpfen, seine lebensrettende Rolle in der Wirtsabwehr erhalten und zugleich die Kollateralschäden verhindern, die bei vielen entzündlichen und degenerativen Erkrankungen auftreten.
Zitation: Shin, H.J., Kim, I.S., Kim, J.K. et al. Molecular mechanisms of NLRP3 inflammasome activation. Exp Mol Med 58, 650–663 (2026). https://doi.org/10.1038/s12276-026-01656-9
Schlüsselwörter: NLRP3-Inflammasom, angeborene Immunität, Entzündung, posttranslationale Modifikation, Immunmetabolismus