Clear Sky Science · sv
Molekylära mekanismer för aktivering av NLRP3‑inflammasomen
Varför våra celler tänder ett molekylärt brandlarm
Våra kroppar förlitar sig på immunsystemets förtruppsceller för att upptäcka fara — invaderande mikrober, giftiga partiklar eller inre stress — och snabbt larma. En av de mest kraftfulla nödsignalerna är en proteinkomplex som kallas NLRP3‑inflammasom. När den slås på utlöser den inflammation som kan rädda oss från infektion. Men om denna brytare sitter fast i läget ”på” kan den driva ett långt register av sjukdomar, från gikt och diabetes till neurodegeneration. Denna översiktsartikel förklarar på molekylär nivå hur NLRP3‑inflammasomen är uppbyggd, vad som sätter igång den och hur cellerna finslipar dess aktivitet, med ledtrådar för framtida läkemedel som kan dämpa skadlig inflammation utan att tysta användbara försvar.
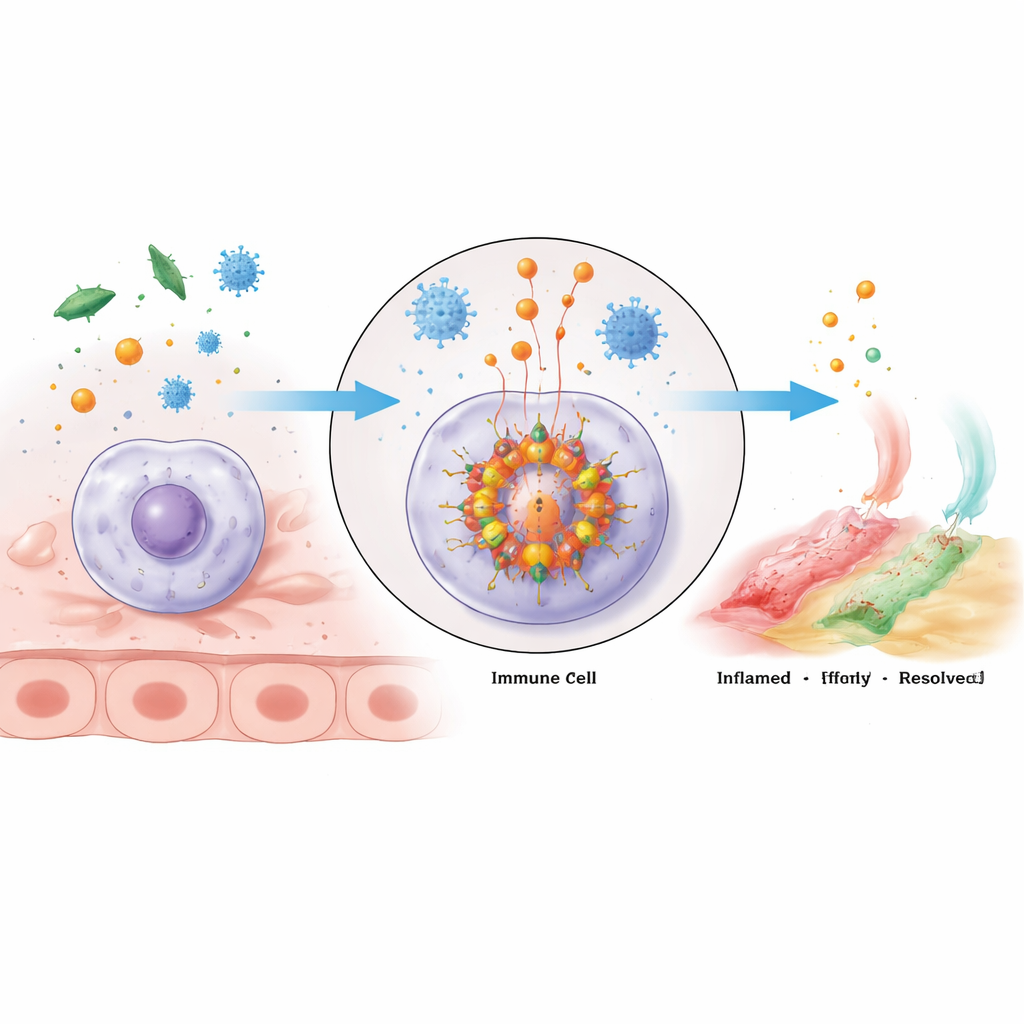
En molekylär larmsamling inne i immunceller
NLRP3‑inflammasomen är en stor multiproteinkluster som monteras i immunceller när de upptäcker fara. Dess kärna består av sensorsproteinet NLRP3, en adapter som heter ASC och enzymet kaspas‑1. NLRP3 har flera regioner med olika uppgifter: ena änden kopplar till ASC, mitten binder energirika ATP‑molekyler och hjälper NLRP3‑enheterna att klustra, och svansen bidrar till att hålla sensorn avstängd tills fara uppstår. När den aktiveras oligomeriserar NLRP3‑molekylerna — grupperar sig — och rekryterar ASC, som bildar filamentliknande skelett som sedan drar till sig kaspas‑1. När de väl är samlade blir kaspas‑1 aktivt och klyver inaktiva prekursorer till de kraftfulla inflammatoriska budbärarna IL‑1β och IL‑18, liksom ett protein kallat gasdermin D som kan skapa hål i cellmembranet och ge upphov till en intensiv, ofta dödlig inflammatorisk reaktion kallad pyroptos.
Två gröna lampor: förberedelse och avfyrning
Att slå på NLRP3 är inte en enstaka händelse utan en tvåstegsprocess. Det första steget, priming, sker när receptorer som känner igen mikrober eller inflammatoriska hormoner aktiveras. Dessa signaler aktiverar transkriptionsfaktorn NF‑κB, vilket ökar produktionen av NLRP3 självt och av de inaktiva cytokinprekursorerna IL‑1β och IL‑18. Samtidigt placeras NLRP3 i ett förberett men ännu ofarligt tillstånd genom ett nätverk av kemiska justeringar — posttranslationella modifieringar — såsom tillsättning eller borttagning av fosfat, ubiquitin, SUMO, acetylgrupper, lipider eller ADP‑ribosgrupper. Det andra steget, aktivering, triggas av en mängd olika stimuli: extracellulärt ATP, bakteriella toxiner, nålliknande kristaller som kiseldioxid eller urinsyra, mitokondriell stress, lysosomal ruptur med mera. Dessa divergerande signaler konvergerar till gemensamma cellulära förändringar — särskilt jonrörelser över membranet, mitokondriell dysfunktion och skador på inre kompartiment — som driver den fysiska monteringen av inflammasomkomplexet och full aktivering av kaspas‑1.
Joner, kraftverk och återvinningscentraler går in i handlingen
Även om NLRP3 svarar på många olika hot återkommer flera kärnprocesser. En är flödet av laddade joner. Förlust av kalium från cellen är den mest konsekventa aktivatorn, med påverkan eller modulation från natrium, klorid och kalciumrörelser genom specialiserade kanaler. En annan är mitokondriell stress: skadade ”kraftverk” frigör reaktiva syrearter och fragment av mitokondriellt DNA som hjälper till att rekrytera och aktivera NLRP3, och läkemedel som metformin kan dämpa denna mitokondriella signal. En tredje är lysosomal skada, som kan uppstå när celler omsluter vassa partiklar; ruptur av dessa återvinningscentra släpper ut enzymer och joner som ytterligare främjar NLRP3‑aktivering. Samtidigt kan förändrad cellmetabolism — hur celler förbränner glukos, fetter och andra bränslen — antingen accelerera eller bromsa inflammasomaktiviteten, där vissa metaboliter som succinat och palmitat driver inflammation och andra som itakonat, fumarat eller ketonkroppar hämmar den.
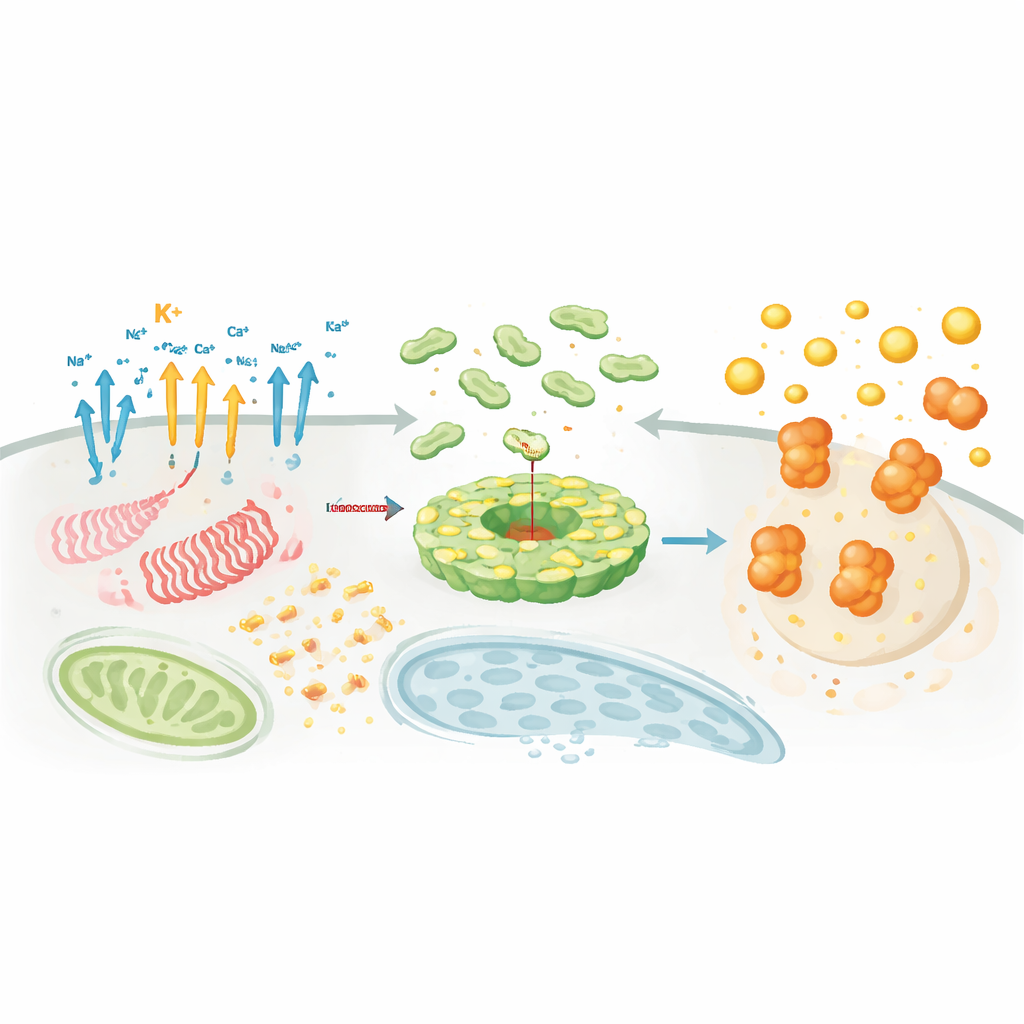
Var och när komplexet monteras
Utöver kemiska signaler är läge och timing avgörande. NLRP3 och dess partner rör sig mellan organeller och åker med cellens interna skelett för att samlas vid specifika nav som trans‑Golgi‑nätverket och det mikrotubuli‑organiserande centret. Där fungerar hjälpproteiner som NEK7 som ”licensieringsfaktorer” som omformar NLRP3 från ett autoinhiberat burformat tillstånd till en aktiv skiva som kan binda ASC. Lipidmodifieringar, som palmitoylering, och elektrostatisk interaktion med särskilda membranlipider styr NLRP3 till rätt plats vid rätt tid. Parallellt med denna koreografi fäster eller tar av dussintals enzymer bort eller sätter på reglerande taggar — ubiquitinkedjor, fosfatgrupper, acetylmärken och SUMO‑proteiner — som finjusterar NLRP3:s mängd, stabilitet och dess förmåga att koppla ihop med ASC och kaspas‑1. Detta täta regleringsnätverk förklarar varför NLRP3 kan vara ytterst känslig för kontext, celltyp och sjukdomstillstånd.
Att väga hjälp mot skada
Eftersom ett överaktivt inflammasom kan vara lika farligt som en infektion använder cellerna också bromsar. Många proteiner binder NLRP3 eller dess kofaktorer för att blockera viktiga interaktioner, leda det till nedbrytning eller förhindra dess klustring, medan andra gynnar dess montering vid verkligt hot. Översikten katalogiserar dessa positiva och negativa partners och visar att subtila defekter — för mycket av en aktiverande modifiering eller för lite av en hämmande — kan tippa systemet mot kronisk inflammation. Författarna menar att förståelsen för hur alla dessa brytare samverkar blir avgörande för att utveckla terapier. Genom att rikta in sig på specifika enzymer som modifierar NLRP3 eller dess medhjälpare skulle framtida läkemedel kunna selektivt dämpa inflammasomet i särskilda vävnader eller sjukdomar, bevara dess livräddande roll i värdförsvaret samtidigt som man förebygger de sidoeffekter som ses vid många inflammatoriska och degenerativa störningar.
Citering: Shin, H.J., Kim, I.S., Kim, J.K. et al. Molecular mechanisms of NLRP3 inflammasome activation. Exp Mol Med 58, 650–663 (2026). https://doi.org/10.1038/s12276-026-01656-9
Nyckelord: NLRP3‑inflammasom, medfödd immunitet, inflammation, posttranslationell modifiering, immunometabolism