Clear Sky Science · nl
Moleculaire mechanismen van activatie van het NLRP3‑inflammasoom
Waarom onze cellen een moleculaire brandalarm aandoen
Ons lichaam vertrouwt op de voorhoede van immuuncellen om problemen te herkennen—indringers zoals microben, giftige deeltjes of interne stress—en snel alarm te slaan. Een van de krachtigste alarmschakelaars is een eiwitmachine die het NLRP3‑inflammasoom wordt genoemd. Wanneer het wordt ingeschakeld, veroorzaakt het ontsteking die ons kan redden van infectie. Maar als die schakel vastzit in de "aan"‑stand, kan dat een lange lijst ziekten aansturen, van jicht en diabetes tot neurodegeneratie. Dit overzichtsartikel legt op moleculair niveau uit hoe het NLRP3‑inflammasoom is opgebouwd, wat het activeert en hoe cellen zijn activiteit fijnafstellen, en biedt aanwijzingen voor toekomstige geneesmiddelen die schadelijke ontsteking kunnen koelen zonder nuttige afweer stil te leggen.
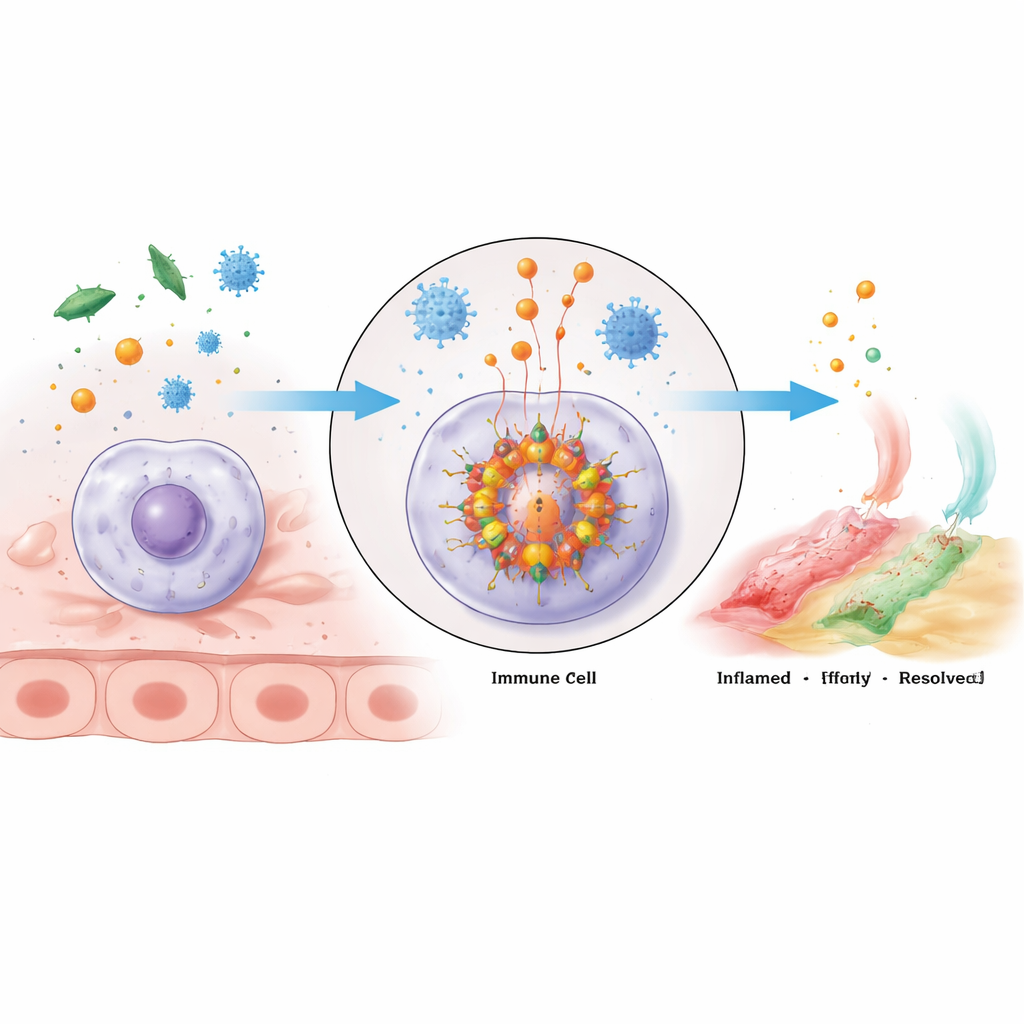
Een moleculair alarmcluster binnen immuuncellen
Het NLRP3‑inflammasoom is een groot multi‑eiwitcomplex dat zich in immuuncellen assembleert wanneer zij gevaar detecteren. De kern bestaat uit het sensor‑eiwit NLRP3, een adapter genaamd ASC en het enzym caspase‑1. NLRP3 heeft meerdere domeinen met verschillende taken: het ene uiteinde koppelt aan ASC, het midden bindt energierijk ATP en helpt NLRP3‑eenheden te clusteren, en de staart helpt de sensor uit te schakelen totdat er probleem optreedt. Wanneer het geactiveerd wordt, oligomeriseren NLRP3‑moleculen—ze groeperen zich—en rekruteren ASC, dat filamentachtige steigers vormt die vervolgens caspase‑1 aantrekken. Eenmaal gebundeld schakelt caspase‑1 in en knipt het inactieve voorlopers van de potente ontstekingsboodschappers IL‑1β en IL‑18, evenals een eiwit genaamd gasdermine D dat gaten in het celmembraan kan slaan, wat resulteert in een brandende, vaak dodelijke ontstekingsreactie die pyroptose wordt genoemd.
Twee groene lichten: klaarzetten en afvuren
Het inschakelen van NLRP3 is geen enkelvoudige gebeurtenis maar een tweestappenproces. De eerste stap, priming genoemd, vindt plaats wanneer receptoren die microben of ontstekingshormonen detecteren worden geactiveerd. Deze signalen activeren de transcriptiefactor NF‑κB, die de productie van NLRP3 zelf en van de inactieve cytokinevoorlopers IL‑1β en IL‑18 verhoogt. Tegelijkertijd plaatst een web van chemische aanpassingen, post‑translationele modificaties genoemd—zoals het toevoegen of verwijderen van fosfaat, ubiquitine, SUMO, acetyl, lipide‑ of ADP‑ribosegroepen—een "vergunning" op NLRP3, waardoor het in een gereedstaande maar nog niet gevaarlijke toestand komt. De tweede stap, activatie, wordt getriggerd door een breed scala aan stimuli: extracellulair ATP, bacteriële toxines, naaldachtige kristallen zoals silica of urinezuur, mitochondriale stress, lysosomale ruptuur en meer. Deze uiteenlopende triggers convergeren naar gemeenschappelijke cellulaire veranderingen—vooral ionbewegingen over het membraan, mitochondriale disfunctie en beschadiging van interne compartimenten—die de fysieke assemblage van het inflammasoomcomplex en de volledige activatie van caspase‑1 aansturen.
Ionentransport, energiecentrales en recyclecentra spelen mee
Hoewel NLRP3 op veel verschillende bedreigingen reageert, blijven enkele kernprocessen steeds terugkomen. Eén daarvan is de stroom geladen ionen. Verlies van kalium uit de cel is de meest consistente activator, geholpen of gemoduleerd door natrium-, chloride‑ en calciumbewegingen via gespecialiseerde kanalen. Een andere is mitochondriale stress: beschadigde "energiecentrales" geven reactieve zuurstofsoorten en fragmenten van mitochondriaal DNA af die helpen NLRP3 te rekruteren en te activeren, en geneesmiddelen zoals metformine kunnen dit mitochondriale signaal dempen. Een derde is lysosomale beschadiging, die kan optreden wanneer cellen scherpe deeltjes opnemen; het scheuren van deze recyclecentra laat enzymen en ionen vrij die NLRP3‑activatie verder bevorderen. Ondertussen kan veranderde cellulaire stofwisseling—hoe cellen glucose, vetten en andere brandstoffen verbranden—het inflammasoom versnellen of remmen, waarbij sommige metabolieten zoals succinaat en palmitaat ontsteking aanwakkeren en andere zoals itaconaat, fumaraat of ketonlichamen deze beperken.
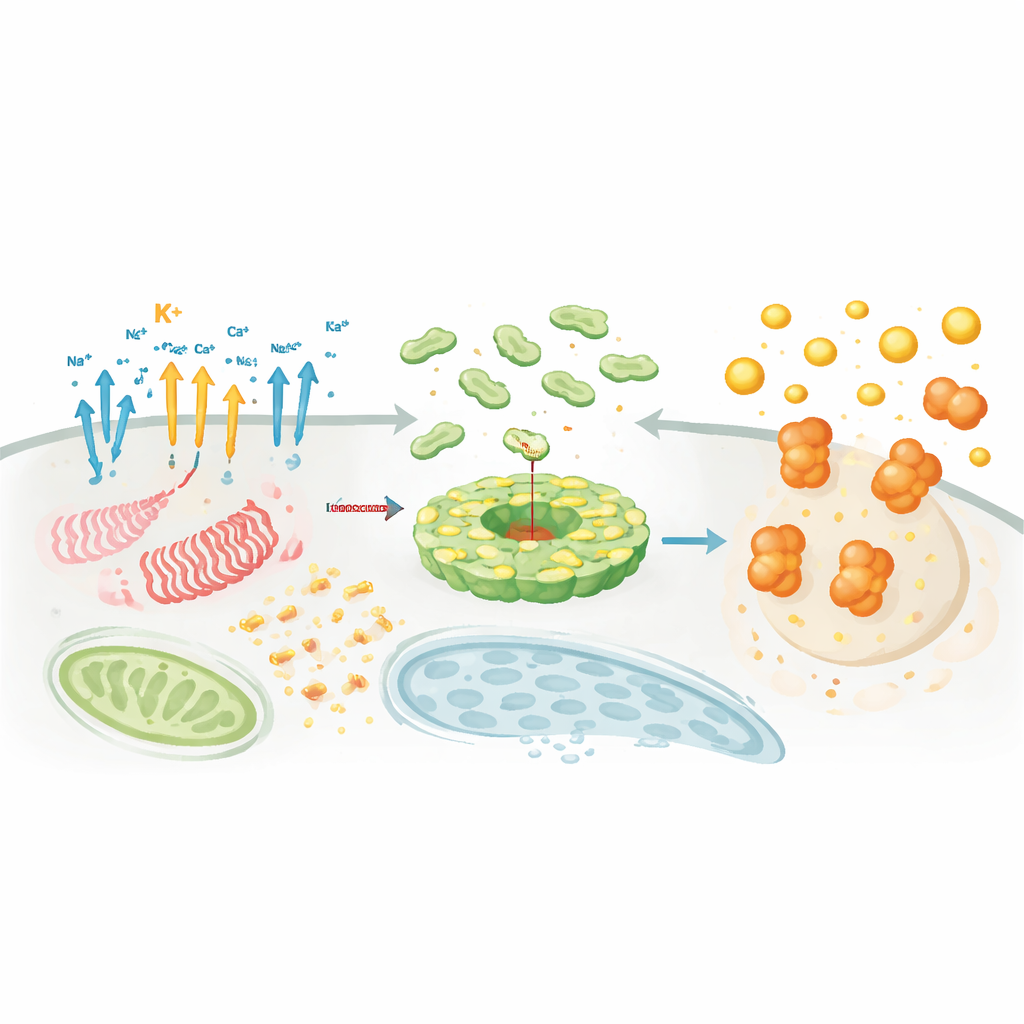
Waar en wanneer het complex samenkomt
Buiten chemische signalen zijn locatie en timing cruciaal. NLRP3 en zijn partners bewegen tussen organellen en reizen mee langs het interne skelet van de cel om zich te verzamelen op specifieke knooppunten zoals het trans‑Golgi‑netwerk en het microtubule‑organiserende centrum. Daar fungeren hulp‑eiwitten zoals NEK7 als "licentiefactoren" die NLRP3 omvormen van een auto‑geïnactiveerde kooi tot een actieve schijf die aan ASC kan binden. Lipidemodificaties, zoals palmitoylering, en elektrostatische interacties met bepaalde membraanlipiden sturen NLRP3 op de juiste plaats op het juiste moment. Parallel aan deze choreografie hechten of verwijderen tientallen enzymen regulerende labels—ubiquitineketens, fosfaatgroepen, acetylmerken en SUMO‑eiwitten—die de hoeveelheid NLRP3, de stabiliteit en het vermogen om met ASC en caspase‑1 te koppelen, fijnregelen. Dit dichte regelnetwerk verklaart waarom NLRP3 uitermate gevoelig kan zijn voor context, celtype en ziektebeeld.
Balanceren tussen hulp en schade
Aangezien een overactief inflammasoom even gevaarlijk kan zijn als een infectie, zetten cellen ook remmen in. Veel eiwitten binden NLRP3 of zijn co‑factoren om cruciale interacties te blokkeren, het eiwit naar degradatie te leiden of clustering te voorkomen, terwijl andere de assemblage versterken bij reële dreiging. Het overzicht rangschikt deze positieve en negatieve partners en toont aan dat subtiele defecten—te veel van een activerende modificatie of te weinig van een remmende—het systeem naar chronische ontsteking kunnen kantelen. De auteurs betogen dat begrip van hoe al deze schakelaars samenwerken essentieel zal zijn voor het ontwerpen van therapieën. Door specifieke enzymen te richten die NLRP3 of zijn helpers modificeren, zouden toekomstige medicijnen het inflammasoom selectief kunnen afkoelen in bepaalde weefsels of ziekten, waarbij de levensreddende rol in de gastheer‑verdediging behouden blijft en de nevenschade die bij veel ontstekings- en degeneratieve aandoeningen wordt gezien, wordt voorkomen.
Bronvermelding: Shin, H.J., Kim, I.S., Kim, J.K. et al. Molecular mechanisms of NLRP3 inflammasome activation. Exp Mol Med 58, 650–663 (2026). https://doi.org/10.1038/s12276-026-01656-9
Trefwoorden: NLRP3 inflammasoom, aangeboren immuniteit, ontsteking, post‑translationele modificatie, immunometabolisme