Clear Sky Science · pt
Otimização estrutural de moléculas medicamentosas com modelos de linguagem treinados incrementalmente
Ensinando computadores a modificar medicamentos
Medicamentos modernos frequentemente começam como moléculas promissoras, porém imperfeitas, que químic@s precisam ajustar meticulosamente para se tornarem fármacos seguros e eficazes. Este estudo mostra como um sistema de inteligência artificial que “lê” fórmulas químicas como uma linguagem pode aprender a realizar parte desse ajuste por conta própria, propondo novos candidatos a fármaco que são ainda mais potentes do que os melhores exemplos conhecidos — sem depender de ferramentas de pontuação externas ou de tentativa e erro baseada em palpites.
Por que otimizar moléculas é tão difícil
Uma vez que os pesquisadores encontram uma molécula inicial que afeta um alvo biológico, o trabalho real começa: transformar esse primeiro “hit” em algo potente, seletivo e adequado como medicamento. Tradicionalmente, químicos desenham dezenas ou centenas de parentes próximos da estrutura original, os sintetizam no laboratório e testam cada um. Esses ciclos de projetar–fazer–testar exigem anos de experiência e grandes esforços experimentais. Métodos computacionais tentaram ajudar, mas muitos se concentram em propriedades simples, como a lipofilicidade da molécula, em vez do efeito biológico completo que ela produz. Outros métodos dependem de ferramentas de predição separadas (“oráculos”) que estimam atividade e podem ser pouco confiáveis ou indisponíveis para muitos alvos.
Usando sentenças químicas para orientar o desenho
Os autores trabalham com modelos de linguagem química, um tipo de sistema de aprendizado profundo que trata moléculas como sequências de caracteres (SMILES) e aprende a “gramática” e os padrões que tornam uma estrutura quimicamente plausível e biologicamente interessante. Primeiro, eles pré-treinam um modelo em centenas de milhares de moléculas bioativas conhecidas, filtrando deliberadamente qualquer coisa relacionada aos alvos específicos que serão estudados depois. Isso produz um modelo generalista que entende química, mas não tem conhecimento prévio dos receptores escolhidos, garantindo que qualquer sucesso posterior venha realmente do novo treino recebido, e não de viés oculto nos dados iniciais.
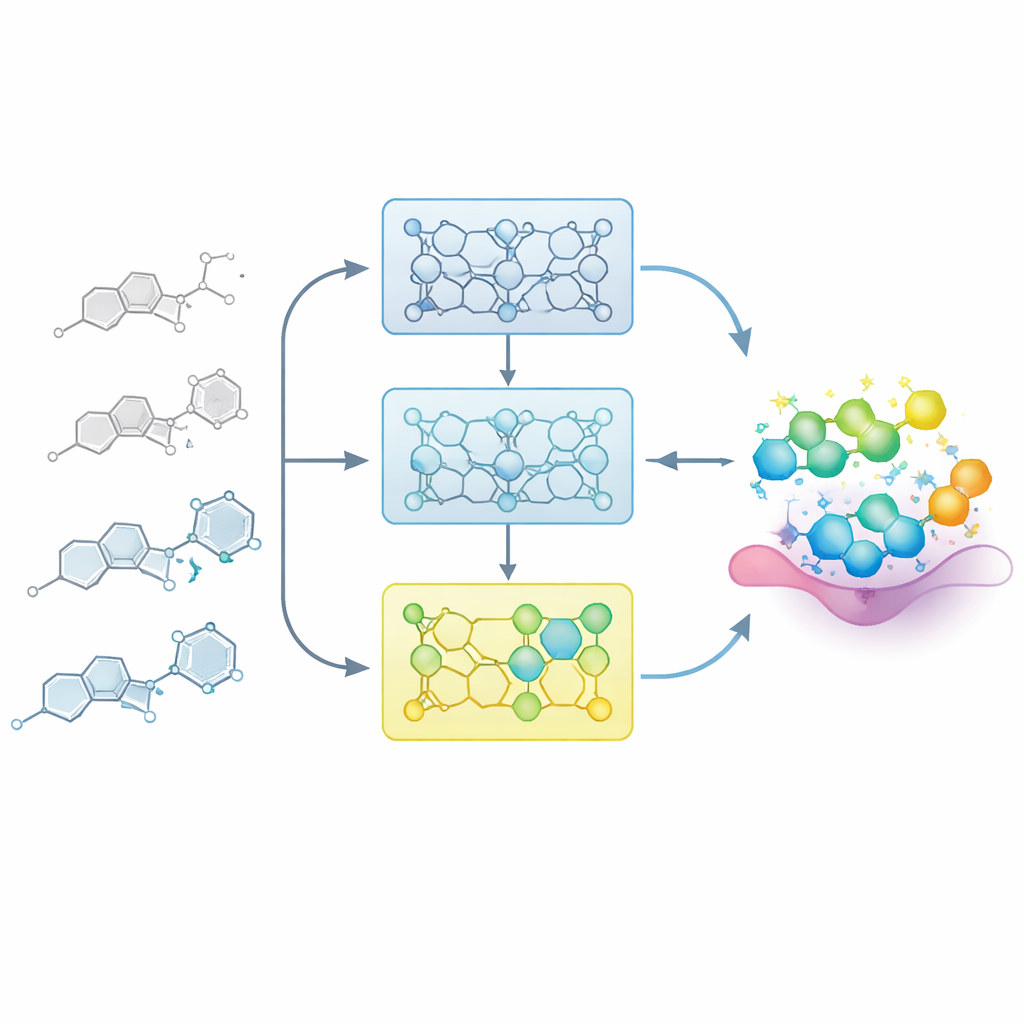
Deixando o modelo aprender como um químico medicinal
Em projetos reais de fármacos, químic@s constroem gradualmente um mapa entre estrutura e atividade: pequenas alterações em um esqueleto central podem tornar um composto mais fraco ou mais forte. Os pesquisadores imitam esse processo alimentando o modelo com séries de moléculas relacionadas cuidadosamente ordenadas, chamadas séries de relação estrutura–atividade (SAR). Em vez de ajustar finamente o modelo de uma só vez com todos os exemplos conhecidos, eles dividem cada série em etapas com base na potência, dos membros mais fracos aos mais potentes. O modelo é primeiro exposto aos compostos menos ativos e depois refinado sucessivamente com subconjuntos que contêm exemplos mais potentes. Esse “treinamento incremental” cria uma trajetória de aprendizado na qual o modelo é guiado suavemente em direção à região do espaço químico onde residem as melhores moléculas.
Da teoria a novos candidatos a fármacos mais potentes
Para testar se essa estratégia de treinamento realmente ajuda, a equipe primeiro verifica se o modelo pode “redescobrir” moléculas altamente ativas que foram deliberadamente retidas fora do treinamento. Com o treinamento incremental, o modelo gera designs bem ranqueados que coincidem com esses compostos potentes ocultos muito mais frequentemente do que modelos treinados em um único passo, indicando que internalizou os padrões que impulsionam alta atividade. Os autores então passam ao desenho em contexto real para dois alvos de relevância médica: PPARγ, envolvido em metabolismo e inflamação, e RORγ, implicado na regulação imune. Após o treinamento incremental com ligantes conhecidos para cada alvo, o modelo propõe novos análogos de esqueletos selecionados. Quando vários desses são sintetizados e testados em laboratório, os nove designs para PPARγ mostram-se agonistas altamente potentes, muitos superando em muito a melhor molécula anterior, e um novo design para RORγ quase alcança a potência do composto mais forte conhecido em sua série, sendo estruturalmente distinto.
O que isso significa para futuros medicamentos
Ao demonstrar que um modelo em estilo de linguagem pode não apenas inventar moléculas, mas também refinar esqueletos existentes para superar os melhores exemplos conhecidos — sem depender de ferramentas de pontuação externas — este trabalho aponta para uma nova forma de fazer química medicinal. A abordagem de treinamento incremental permite que o modelo absorva regras sutis de relação estrutura–atividade e suas interdependências de longo alcance, e então as estenda para territórios inexplorados. Para não especialistas, a conclusão principal é que a IA pode agora agir menos como um gerador aleatório de ideias e mais como um assistente treinado digitalmente do químico, propondo melhorias focadas e testáveis em moléculas promissoras e potencialmente acelerando o caminho de hits iniciais a medicamentos otimizados.
Citação: Hörmann, T., Mayer, D., Lewandowski, M. et al. Structural optimization of drug molecules with incrementally trained language models. Nat Commun 17, 3456 (2026). https://doi.org/10.1038/s41467-026-71591-w
Palavras-chave: modelos de linguagem química, delineamento de fármacos de novo, relação estrutura–atividade, química generativa, IA em química medicinal