Clear Sky Science · pl
Montelukast łagodzi kardiotoksyczność wywołaną diklofenakiem sodowym u samców szczurów poprzez celowanie w szlak Wnt/β-katenina
Dlaczego leki przeciwbólowe i zdrowie serca mają znaczenie
Wiele osób polega na niesteroidowych lekach przeciwzapalnych (NLPZ), takich jak diklofenak, aby radzić sobie z codziennymi bólami, chorobą zwyrodnieniową stawów i urazami. Coraz więcej dowodów wskazuje jednak, że długotrwałe stosowanie niektórych z tych leków może podstępnie obciążać serce. W niniejszym badaniu sprawdzono, czy montelukast — lek na astmę powszechnie przepisywany — może chronić serce przed uszkodzeniem związanym z diklofenakiem, oraz ujawniono kluczową ścieżkę sygnałową komórek, która może wyjaśniać zarówno szkodę, jak i ochronę.
Bliższe spojrzenie na powszechny lek przeciwbólowy
Diklofenak jest jednym z najczęściej stosowanych leków przeciwbólowych i przeciwzapalnych na świecie. Działa poprzez blokowanie enzymów biorących udział w wytwarzaniu prostaglandyn — substancji związanych z bólem, gorączką i zapaleniem. Jednak ta sama aktywność może zaburzać delikatne mechanizmy ochronne żołądka, nerek, wątroby i serca. Wcześniejsze badania na zwierzętach i ludziach wiązały długotrwałe stosowanie diklofenaku z problemami sercowymi, w tym z uszkodzeniem tkanek i zaburzeniem funkcji. Naukowcy podejrzewają, że do tego uszkodzenia przyczynia się toksyczne połączenie nadmiaru reaktywnych cząsteczek tlenu, niekontrolowanego zapalenia, włóknienia tkanki sercowej oraz programowanej śmierci komórek mięśnia sercowego.
Przełącznik sygnałowy wewnątrz komórek serca
Aby zrozumieć, jak diklofenak uszkadza serce, badacze skupili się na szlaku komunikacji komórkowej znanym jako szlak Wnt/β‑katenina. Szlak ten pomaga kontrolować wzrost, podział i przeżycie komórek. W zdrowym sercu dorosłego zazwyczaj działa na niskim poziomie, ale w wielu formach chorób serca staje się nadmiernie aktywny i łączy się ze stresem oksydacyjnym, zapaleniem, śmiercią komórek i włóknieniem (gromadzeniem się sztywnej tkanki bliznowatej). U samców szczurów otrzymujących diklofenak przez dwa tygodnie zespół zaobserwował wyraźne oznaki aktywacji tego szlaku: kluczowe białka systemu Wnt były istotnie zwiększone w tkance serca. Jednocześnie badania krwi i próbki tkanek wykazały wyraźne dowody uszkodzenia serca, w tym przedostawanie się enzymów sercowych do krwiobiegu, obrzęk i degenerację włókien mięśnia sercowego oraz zwiększenie masy serca w stosunku do masy ciała.
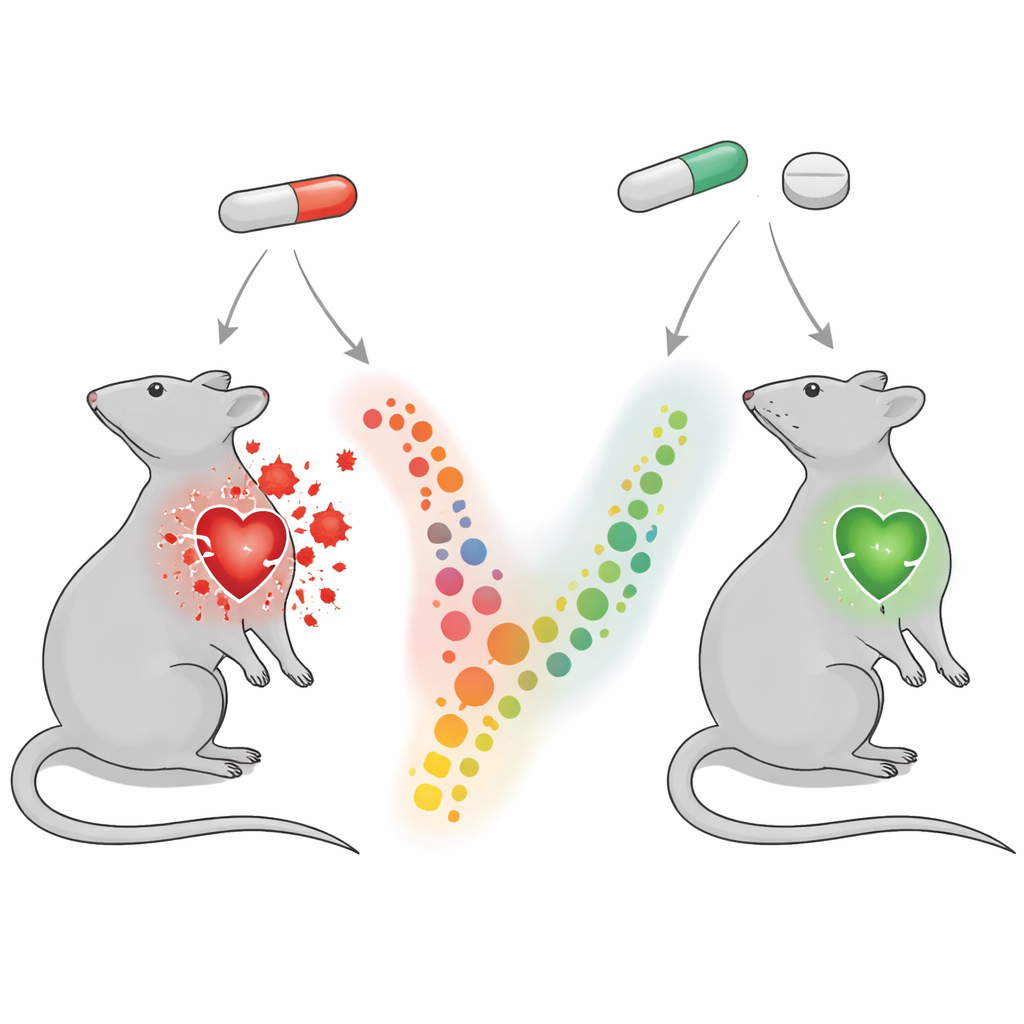
Testowanie ochrony: lek na astmę montelukast
Montelukast jest znany przede wszystkim jako tabletka blokująca leukotrieny — chemiczne przekaźniki biorące udział w astmie i alergiach. Co ciekawe, wcześniejsze badania na zwierzętach sugerowały, że montelukast także łagodzi zapalenie i stres oksydacyjny w sercu. W tym badaniu szczury otrzymywały montelukast razem z diklofenakiem. W porównaniu ze zwierzętami leczonymi samym diklofenakiem, szczury otrzymujące terapię skojarzoną miały znacznie niższe poziomy markerów uszkodzenia serca we krwi i zdrowszy wygląd tkanki sercowej w mikroskopie. Ich stosunek masy serca do masy ciała był bliższy normie, co sugeruje mniejsze obrzęki i pogrubienie. W mięśniu sercowym zmniejszyły się szkodliwe zmiany oksydacyjne: spadł marker uszkodzenia lipidów (malondialdehyd), podczas gdy naturalne mechanizmy antyoksydacyjne (glutation i dysmutaza ponadtlenkowa) odbudowały się.
Wyhamowanie zapalenia, włóknienia i śmierci komórek
Diklofenak samodzielnie wywołał wzrost sygnałów zapalnych w sercu i zwiększoną aktywność kaspazy‑3, białka prowadzącego komórki do autodestrukcji. Obniżył też poziomy Bcl‑2, białka, które normalnie pomaga komórkom przetrwać. Na poziomie tkankowym między komórkami mięśnia sercowego gromadziły się włókna kolagenowe — cecha włóknienia, która może usztywniać serce i upośledzać jego kurczliwość. Leczenie skojarzone z montelukastem odwróciło wiele z tych zmian: cytokiny zapalne spadły, poziomy kaspazy‑3 zmalały, Bcl‑2 wzrósł, a nagromadzenie kolagenu było wyraźnie mniejsze. Co ważne, to samo leczenie znacznie stłumiło wzrost wywołany diklofenakiem Wnt‑1, aktywnej β‑kateniny oraz receptora FZD‑1, łącząc efekt ochronny leku z osłabieniem sygnału Wnt/β‑katenina w komórkach serca.
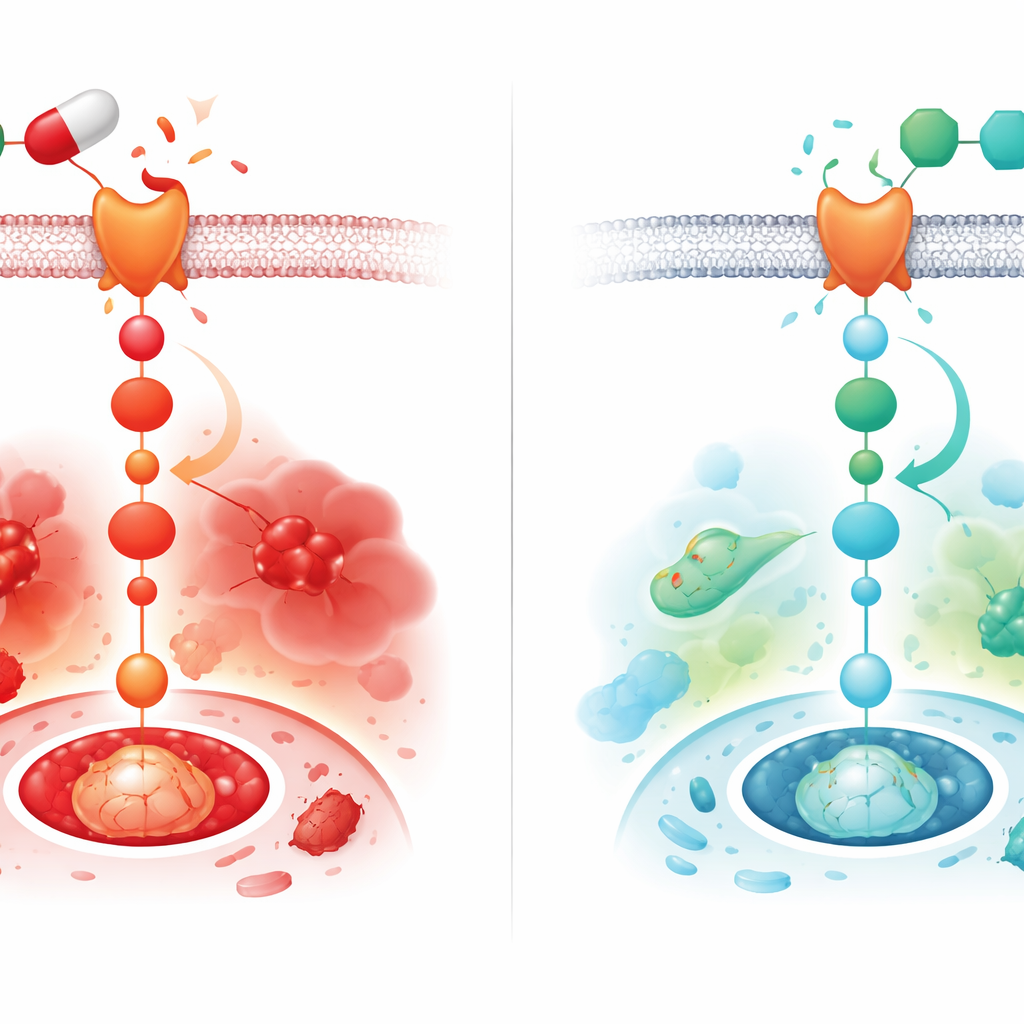
Co to może oznaczać dla osób stosujących leki przeciwbólowe
Wyniki sugerują, że diklofenak uszkadza serce częściowo poprzez aktywację przełącznika Wnt/β‑katenina, co z kolei napędza stres oksydacyjny, zapalenie, włóknienie i śmierć komórek. U szczurów montelukast wyciszył ten przełącznik i złagodził uszkodzenia na wielu frontach. Ponieważ montelukast jest już szeroko stosowany u ludzi i ma znany profil bezpieczeństwa, wyłania się tutaj jako obiecujący kandydat do ochrony serca podczas długotrwałej terapii NLPZ. Należy jednak pamiętać, że badanie przeprowadzono na samcach szczurów i koncentrowało się na zmianach molekularnych i tkankowych, a nie bezpośredniej funkcji serca. Zanim lekarze mogliby rozważyć łączenie tych leków u pacjentów, przyszłe badania będą musiały potwierdzić rolę tego szlaku przy użyciu specyficznych blokerów Wnt, testować samice, mierzyć wydolność serca i ustalić, czy podobne korzyści — oraz bezpieczne dawki — przekładają się na ludzi.
Cytowanie: Alsanea, S., Albuhayri, S., Alkharashi, L. et al. Montelukast attenuates diclofenac sodium-induced cardiotoxicity in male rats via targeting Wnt/β-catenin pathway. Sci Rep 16, 11717 (2026). https://doi.org/10.1038/s41598-026-46514-w
Słowa kluczowe: kardiotoksyczność diklofenaku, montelukast, zapalenie serca, stres oksydacyjny, szlak Wnt beta-katenina