Clear Sky Science · de
Montelukast mildert diclofenac‑natrium‑induzierte Kardiotoxizität bei männlichen Ratten durch Zielsteuerung des Wnt/β‑Catenin‑Signalwegs
Warum Schmerzmittel und Herzgesundheit wichtig sind
Viele Menschen greifen auf nichtsteroidale Antirheumatika (NSAR) wie Diclofenac zurück, um Alltagsbeschwerden, Arthrose und Verletzungsschmerzen zu lindern. Zunehmende Hinweise deuten jedoch darauf hin, dass die langfristige Einnahme einiger dieser Medikamente das Herz stillschweigend belasten kann. Diese Studie untersucht, ob Montelukast — ein bereits weit verbreitet verschriebenes Asthmamedikament — das Herz vor diclofenac‑bedingten Schäden schützen kann, und sie identifiziert einen wichtigen zellulären Signalweg, der sowohl die Schädigung als auch den Schutz erklären könnte.
Ein genauerer Blick auf ein verbreitetes Schmerzmittel
Diclofenac gehört zu den weltweit am häufigsten verwendeten Schmerz‑ und Entzündungshemmern. Es wirkt, indem es Enzyme blockiert, die Prostaglandine produzieren — Botenstoffe, die an Schmerz, Fieber und Entzündung beteiligt sind. Dieselbe Wirkung kann jedoch empfindliche Gleichgewichte stören, die Magen, Nieren, Leber und Herz schützen. Frühere Arbeiten an Tieren und Menschen haben eine Verbindung zwischen langfristiger Diclofenac‑Anwendung und Herzproblemen hergestellt, einschließlich Gewebeschäden und eingeschränkter Funktion. Forscher vermuten, dass diese Schäden durch eine toxische Kombination aus überschüssigen reaktiven Sauerstoffspezies, übermäßiger Entzündung, Vernarbung des Herzgewebes und programmierter Zellselbsttötung der Herzmuskelzellen hervorgerufen werden.
Der Signalumschalter in Herzmuskelzellen
Um zu verstehen, wie Diclofenac das Herz schädigt, konzentrierten sich die Forschenden auf einen zellulären Kommunikationsweg, der als Wnt/β‑Catenin‑Signalweg bekannt ist. Dieser Weg hilft zu steuern, wie Zellen wachsen, sich teilen und überleben. In einem gesunden erwachsenen Herzen ist er in der Regel eher niedrig aktiviert, wird jedoch in vielen Formen von Herzerkrankungen abnorm aktiv und steht im Zusammenhang mit oxidativem Stress, Entzündung, Zelltod und Fibrose (Ablagerung starrer Narben). Bei männlichen Ratten, die zwei Wochen lang Diclofenac erhielten, fand das Team deutliche Hinweise auf eine Aktivierung dieses Weges: Schlüsselproteine des Wnt‑Systems waren im Herzgewebe deutlich erhöht. Gleichzeitig zeigten Bluttests und Gewebeproben klare Zeichen von Herzschäden, darunter Austreten von Herzenzymen ins Blut, geschwollene und degenerierende Herzmuskelbündel sowie eine erhöhte Herz‑zu‑Körper‑Gewichts‑Relation.
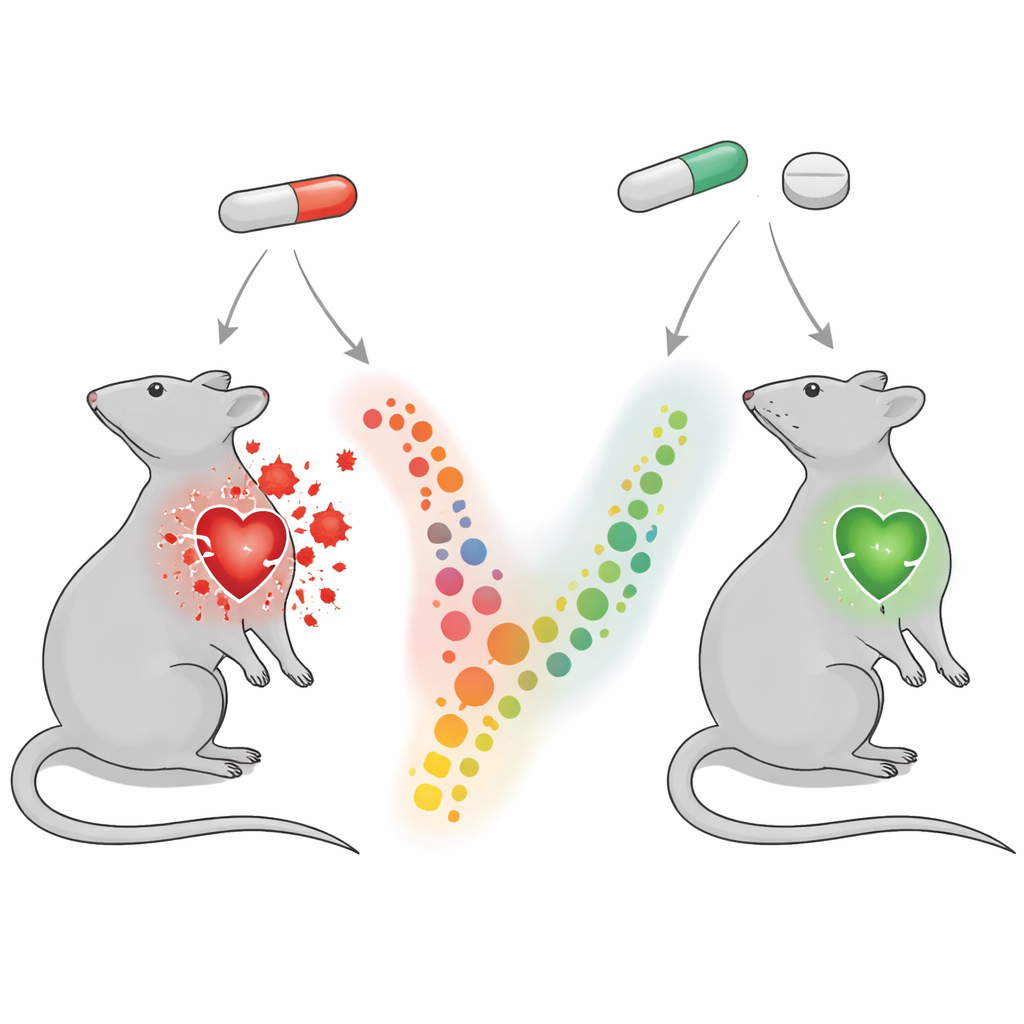
Prüfung eines Schutzmittels: das Asthmamedikament Montelukast
Montelukast ist vor allem als Tablette bekannt, die Leukotriene blockiert — chemische Botenstoffe, die bei Asthma und Allergien eine Rolle spielen. Interessanterweise deuteten frühere Tierstudien darauf hin, dass Montelukast auch Entzündungen und oxidativen Stress im Herzen dämpfen kann. In dieser Studie erhielten Ratten Montelukast zusammen mit Diclofenac. Im Vergleich zu Tieren, die nur Diclofenac bekamen, wiesen die gemeinsam behandelten Ratten deutlich geringere Werte von Herzschadensmarkern im Blut und unter dem Mikroskop gesünder erscheinendes Herzgewebe auf. Ihr Verhältnis von Herz‑ zu Körpergewicht näherte sich dem Normalbereich an, was auf weniger Schwellung und Verdickung hinweist. Im Herzmuskel waren schädliche oxidative Veränderungen reduziert: ein Marker für Fett‑Schädigung (Malondialdehyd) sank, während die natürlichen antioxidativen Abwehrmechanismen (Glutathion und Superoxiddismutase) sich erholten.
Entzündung, Vernarbung und Zelltod verringern
Diclofenac allein löste einen Anstieg entzündlicher Botenstoffe im Herzen aus und erhöhte die Aktivität von Caspase‑3, einem Protein, das Zellen in Richtung Selbstzerstörung treibt. Gleichzeitig sanken die Spiegel von Bcl‑2, einem Protein, das normalerweise das Überleben von Zellen fördert. Auf Gewebeebene sammelten sich Kollagenfasern zwischen den Herzmuskelzellen an — ein Kennzeichen der Fibrose, das das Herz versteifen und die Pumpleistung beeinträchtigen kann. Die Co‑Behandlung mit Montelukast kehrte viele dieser Veränderungen um: Entzündungszytokine sanken, Caspase‑3‑Spiegel fielen, Bcl‑2 stieg und die Kollagenablagerung war deutlich vermindert. Wichtig ist, dass dieselbe Behandlung den diclofenac‑induzierten Anstieg von Wnt‑1, aktivem β‑Catenin und dem Rezeptor FZD‑1 erheblich abschwächte, wodurch der schützende Effekt des Medikaments mit einer gedämpften Wnt/β‑Catenin‑Signalgebung in Herzmuskelzellen verknüpft wurde.
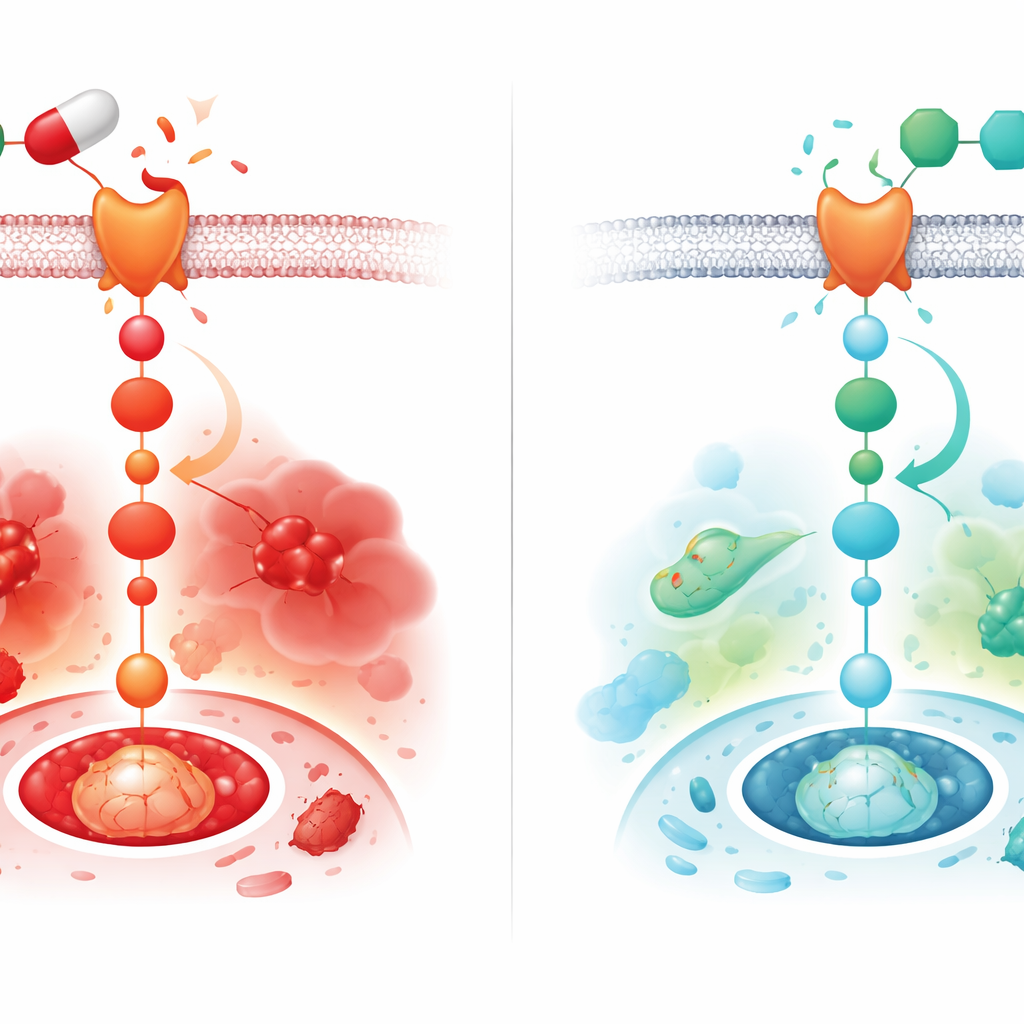
Was das für Menschen bedeuten könnte, die Schmerzmittel verwenden
Die Ergebnisse legen nahe, dass Diclofenac das Herz teilweise schädigt, indem es den Wnt/β‑Catenin‑Schalter einschaltet, was wiederum oxidativen Stress, Entzündung, Vernarbung und Zelltod fördert. Bei Ratten drehte Montelukast diesen Schalter herunter und milderte die Schäden auf mehreren Ebenen. Da Montelukast bereits breit beim Menschen eingesetzt wird und ein bekanntes Sicherheitsprofil besitzt, stellt es hier einen vielversprechenden Kandidaten dar, das Herz während einer langfristigen NSAR‑Therapie zu schützen. Dennoch wurde die Arbeit an männlichen Ratten durchgeführt und konzentrierte sich auf molekulare und Gewebeveränderungen statt auf direkte Herzfunktion. Bevor Ärztinnen und Ärzte in Erwägung ziehen könnten, diese Medikamente bei Patienten zu kombinieren, müssen zukünftige Studien die Rolle des Signalwegs mit spezifischen Wnt‑Blockern bestätigen, weibliche Tiere testen, die Herzleistung messen und klären, ob ähnliche Vorteile — und sichere Dosierungen — auf Menschen übertragbar sind.
Zitation: Alsanea, S., Albuhayri, S., Alkharashi, L. et al. Montelukast attenuates diclofenac sodium-induced cardiotoxicity in male rats via targeting Wnt/β-catenin pathway. Sci Rep 16, 11717 (2026). https://doi.org/10.1038/s41598-026-46514-w
Schlüsselwörter: diclofenac Kardiotoxizität, montelukast, Herzentzündung, oxidativer Stress, Wnt‑beta‑Catenin‑Signalweg