Clear Sky Science · fr
Le montélukast atténue la cardiotoxicité induite par le diclofénac sodique chez le rat mâle en ciblant la voie Wnt/β-caténine
Pourquoi les analgésiques et la santé cardiaque comptent
Beaucoup de personnes comptent sur les anti‑inflammatoires non stéroïdiens (AINS) comme le diclofénac pour gérer les douleurs quotidiennes, l’arthrite et les blessures. Mais des preuves croissantes indiquent qu’une utilisation prolongée de certains de ces médicaments peut mettre insidieusement le cœur à rude épreuve. Cette étude examine si le montélukast — un médicament pour l’asthme déjà largement prescrit — peut protéger le cœur des dommages liés au diclofénac, et elle met en lumière une voie de signalisation cellulaire clé susceptible d’expliquer à la fois le dommage et la protection.
Un examen approfondi d’un antalgique courant
Le diclofénac est l’un des médicaments analgésiques et anti‑inflammatoires les plus utilisés dans le monde. Il agit en bloquant des enzymes responsables de la production de prostaglandines, des substances impliquées dans la douleur, la fièvre et l’inflammation. Cependant, cette même action peut perturber des équilibres délicats qui protègent l’estomac, les reins, le foie et le cœur. Des travaux antérieurs chez l’animal et chez l’humain ont relié une utilisation prolongée du diclofénac à des problèmes cardiaques, notamment des lésions tissulaires et une fonction altérée. Les chercheurs soupçonnent que ces lésions résultent d’une combinaison toxique d’excès de molécules réactives de l’oxygène, d’inflammation incontrôlée, de fibrose du tissu cardiaque et de mort programmée des cellules du muscle cardiaque.
L’interrupteur de signalisation à l’intérieur des cellules cardiaques
Pour comprendre comment le diclofénac blesse le cœur, les auteurs se sont intéressés à une voie de communication cellulaire connue sous le nom de voie Wnt/β‑caténine. Cette voie aide à contrôler la croissance, la division et la survie des cellules. Dans un cœur adulte sain, elle est généralement maintenue à faible niveau, mais dans de nombreuses formes de maladie cardiaque elle devient anormalement active et est associée au stress oxydatif, à l’inflammation, à la mort cellulaire et à la fibrose (accumulation de tissu cicatriciel raide). Chez des rats mâles recevant du diclofénac pendant deux semaines, l’équipe a observé des signes nets d’activation de cette voie : des protéines clés du système Wnt étaient fortement augmentées dans le tissu cardiaque. Dans le même temps, les analyses sanguines et les prélèvements tissulaires ont montré des preuves claires de lésion cardiaque, y compris une fuite d’enzymes cardiaques dans la circulation, des fibres musculaires cardiaques enflées et dégénérées, et une augmentation de la taille du cœur par rapport au poids corporel.
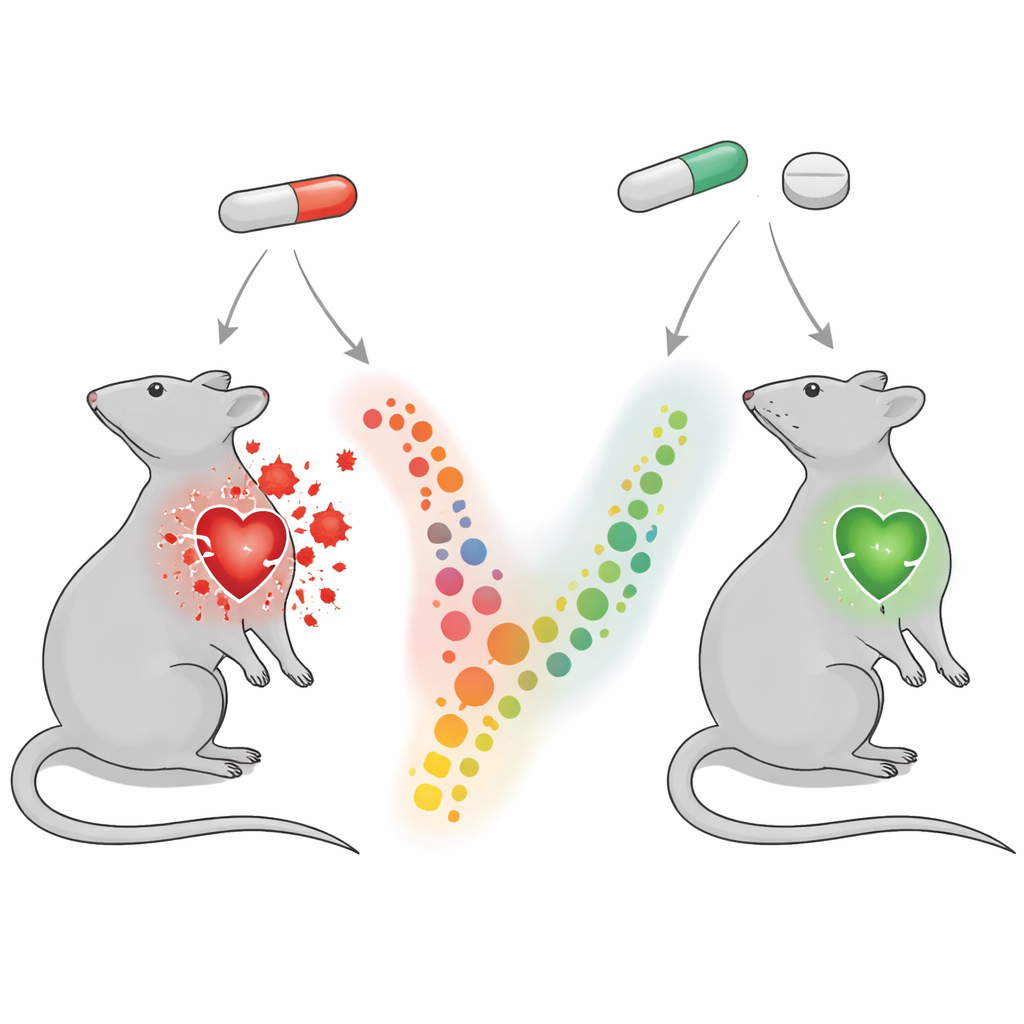
Tester un protecteur : le montélukast, médicament contre l’asthme
Le montélukast est surtout connu comme comprimé bloquant les leucotriènes — des messagers chimiques impliqués dans l’asthme et les allergies. Fait intéressant, des études animales antérieures suggéraient que le montélukast calme également l’inflammation et le stress oxydatif dans le cœur. Dans cette étude, des rats ont reçu du montélukast en même temps que du diclofénac. Comparés aux animaux traités uniquement par diclofénac, les rats co‑traités présentaient des niveaux bien plus faibles de marqueurs de lésion cardiaque dans le sang et un aspect tissulaire cardiaque plus sain au microscope. Leur rapport cœur/poids corporel était plus proche de la normale, suggérant moins d’enflure et d’épaississement. Dans le muscle cardiaque, les altérations oxydatives nocives étaient réduites : un marqueur de la peroxydation lipidique (le malondialdéhyde) a diminué, tandis que les défenses antioxydantes naturelles (glutathion et superoxyde dismutase) se sont rétablies.
Réduction de l’inflammation, de la fibrose et de la mort cellulaire
Le diclofénac seul a déclenché une hausse des médiateurs inflammatoires dans le cœur et augmenté l’activité de la caspase‑3, une protéine qui pousse les cellules vers l’autodestruction. Il a aussi réduit les niveaux de Bcl‑2, une protéine qui aide normalement à la survie cellulaire. Au niveau tissulaire, des fibres de collagène se sont accumulées entre les cellules du muscle cardiaque, un signe de fibrose pouvant rigidifier le cœur et compromettre sa capacité de pompage. Le co‑traitement par le montélukast a inversé bon nombre de ces changements : les cytokines inflammatoires ont diminué, les niveaux de caspase‑3 ont baissé, Bcl‑2 a augmenté, et l’accumulation de collagène était nettement moins prononcée. De manière importante, le même traitement a fortement atténué l’augmentation induite par le diclofénac de Wnt‑1, de la β‑caténine active et du récepteur FZD‑1, reliant ainsi l’effet protecteur du médicament à une diminution de la signalisation Wnt/β‑caténine dans les cellules cardiaques.
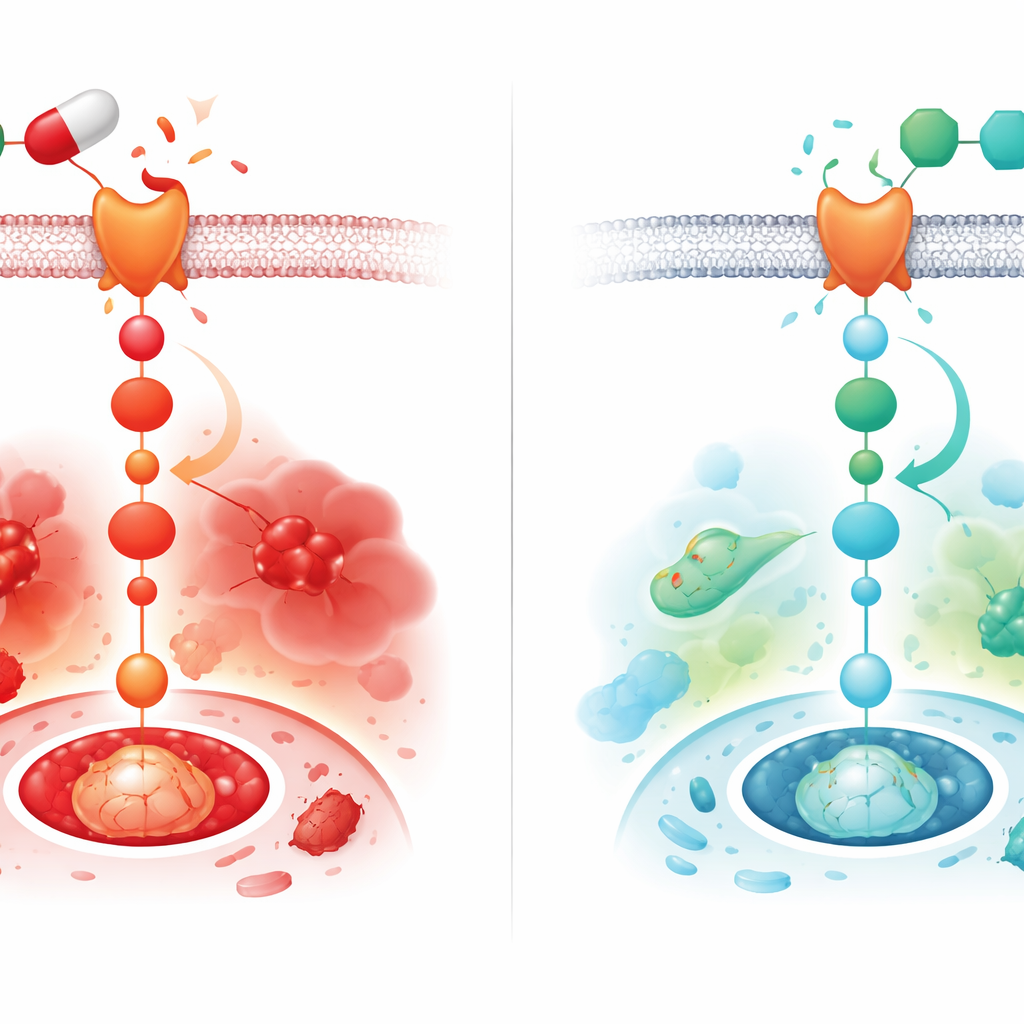
Ce que cela pourrait signifier pour les personnes prenant des antalgiques
Les résultats suggèrent que le diclofénac endommage le cœur en partie en activant l’interrupteur Wnt/β‑caténine, ce qui alimente ensuite le stress oxydatif, l’inflammation, la fibrose et la mort cellulaire. Chez le rat, le montélukast a désamorcé cet interrupteur et atténué les dommages sur plusieurs fronts. Étant donné que le montélukast est déjà largement utilisé chez l’homme et dispose d’un profil de sécurité connu, il apparaît ici comme un candidat prometteur pour protéger le cœur lors d’un traitement prolongé par AINS. Néanmoins, le travail a été réalisé chez des rats mâles et s’est concentré sur des changements moléculaires et tissulaires plutôt que sur la fonction cardiaque directe. Avant que les cliniciens puissent envisager d’associer ces médicaments chez les patients, des études futures devront confirmer le rôle de la voie en utilisant des bloqueurs spécifiques de Wnt, tester des femelles, mesurer la performance cardiaque et déterminer si des bénéfices similaires — et des doses sûres — se traduisent chez l’humain.
Citation: Alsanea, S., Albuhayri, S., Alkharashi, L. et al. Montelukast attenuates diclofenac sodium-induced cardiotoxicity in male rats via targeting Wnt/β-catenin pathway. Sci Rep 16, 11717 (2026). https://doi.org/10.1038/s41598-026-46514-w
Mots-clés: cardiotoxicité du diclofénac, montélukast, inflammation cardiaque, stress oxydatif, voie Wnt bêta-caténine