Clear Sky Science · zh
深度学习驱动的一体化流程用于新型抗菌肽的从头设计与合成
为什么需要新的抗菌分子
随着常用抗生素对日益强韧的细菌失去效力,医生在治疗常见感染时可用的选择正在减少。一种有前景的替代方案是抗菌肽——这种短蛋白片段通过在细菌膜上打孔而起作用,而不是针对单一酶。本文章描述了研究者如何利用人工智能(AI)自动设计并测试新的抗菌肽,其速度更快、成本更低、且比传统的反复试验更具针对性。

在广阔分子空间中寻找新途径
设计有用的抗菌肽就像在一堆随机数字中寻找几张中奖的彩票:氨基酸序列的可能组合天文数字般庞大,但真正安全有效的药物只占极小一部分。传统的实验室筛选既慢又昂贵,即便是计算模型也常难以在效力与发现真正新颖分子所需的多样性之间取得平衡。作者通过构建一个包含生成、评估和实验验证三步的流程来应对这一挑战——该流程让AI能在巨大的序列空间中探索,同时又能聚焦于看起来真实且有潜力的候选分子。
教会蛋白语言模型像肽设计者一样思考
第一步的核心是ProtGPT2,这是一种大型“蛋白质语言模型”,最初被训练用于像文本模型写句子那样生成可信的蛋白序列。研究团队没有对这个大模型进行全面再训练——这种做法代价高且容易在小规模的抗菌数据集上过拟合——而是采用一种称为软提示微调(soft prompt tuning)的策略。他们在每个序列前附加一个小的、可训练的输入提示,仅更新这个提示而保持模型内部权重不变。这种温和的引导足以将模型转向生成类似抗菌肽的序列,同时不牺牲其广泛的创造性。对生成序列的分析显示,它们在电荷、疏水性和结构模式等关键属性上与真实抗菌肽相匹配,且比完全再训练产生的序列更具多样性。
让多个AI“专家”为每个候选投票
在第二步,研究者面临相反的挑战:在3万条生成序列中,哪些值得投入化学合成和实验室测试?他们构建了名为MCL‑AMP的评估模型,该模型结合了三种不同的神经网络“专家”——一个关注局部模式,一个追踪序列中的长程关系,另一个整合整体特征。一个单独的投票网络学习在每个肽上应多大程度信任各个专家,且使用特殊的损失函数来抑制系统在错误时过度自信。利用另一种先进蛋白模型(ESM‑2)提取的丰富序列特征,这个集成方法在区分抗菌与非抗菌序列方面比现有工具具有更高的准确性,并为每个候选给出可解释的置信度评分。
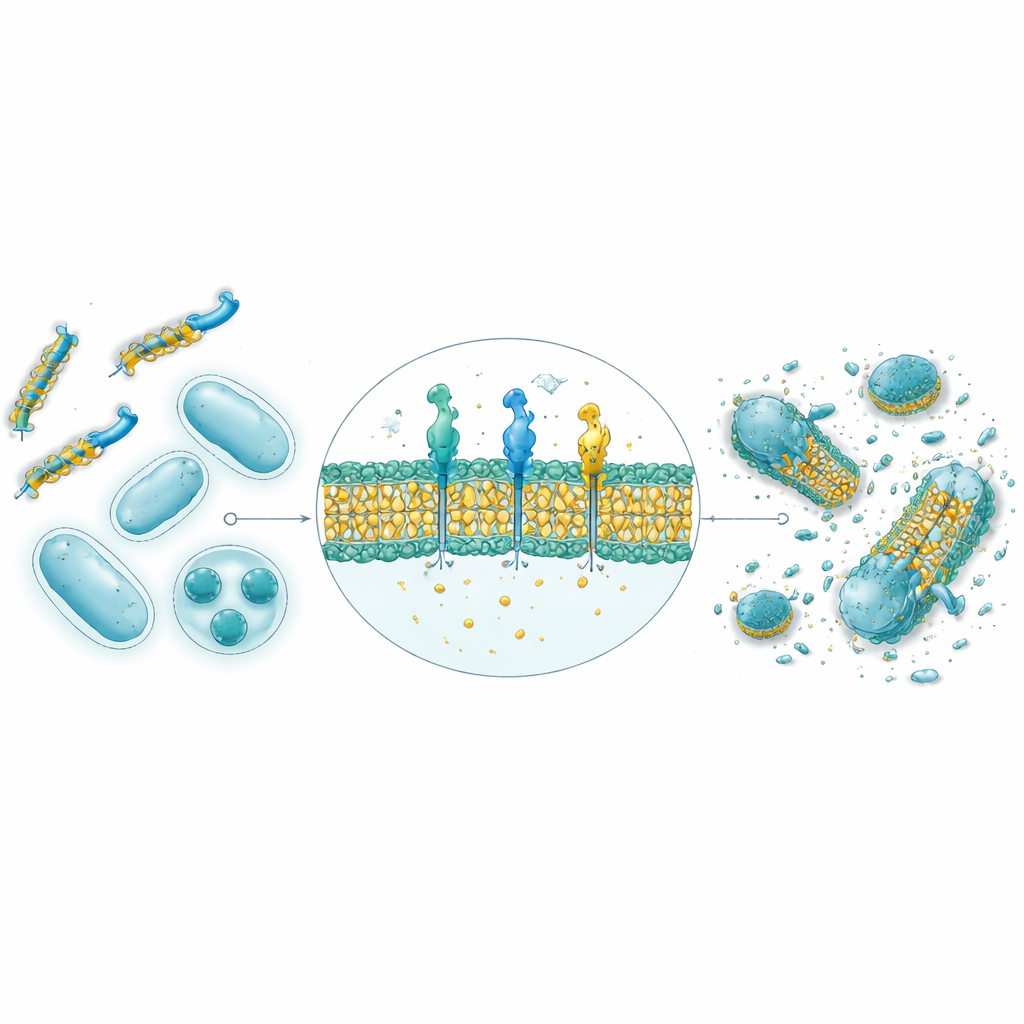
从计算预测到实验室中的真实细菌
在3万条AI生成的序列中,得分最高的九条肽被合成并在四种细菌菌株上测试,涵盖革兰氏阳性和革兰氏阴性物种。使用AlphaFold的结构预测表明,九条中的八条呈现出天然抗菌肽典型的两亲性螺旋形态,具有分开的亲水面和疏水面,有利于对膜的攻击。在培养皿实验中,九条肽中有四条表现出强抗菌活性,其中两条(命名为GW20和KI16)在抑制细菌生长方面接近已知抗生素的性能。显微观察显示这些肽明显损伤了细菌细胞表面,与膜破坏的作用机制一致。重要的是,在治疗相关浓度下,这两条肽对红细胞的损伤极小,并表现出强大的防止和分解细菌黏性生物膜的能力,往往优于一种标准抗生素。
这对未来药物意味着什么
对非专业读者而言,关键意思是作者构建了一个可运行的“设计—测试”闭环:AI提出大量新的杀菌肽,由模型委员会对其分流,再在实验室确认命中结果。尽管并非每个排名靠前的序列都奏效,但命中率——九个测试中有四个活性肽——远高于传统的盲筛。最有前景的两种分子已显示出效力、安全性与抗生物膜能力的有益组合,暗示它们可成为顽固感染的未来疗法。与此同样重要的是,这一模块化流程可以重新调试以设计其他医疗肽,例如靶向癌症的制剂或抗病毒分子,为面对不断上升的抗菌耐药性提供一个灵活的AI加速药物发现蓝图。
引用: Liu, J., Chen, Y., Tang, J. et al. Deep learning-driven integrated pipeline for de novo design and synthesis of antimicrobial peptides. npj Drug Discov. 3, 15 (2026). https://doi.org/10.1038/s44386-026-00045-6
关键词: 抗菌肽, 人工智能, 药物发现, 抗生素耐药性, 生物膜