Clear Sky Science · fr
Pipeline intégrée pilotée par l’apprentissage profond pour la conception de novo et la synthèse de peptides antimicrobiens
Pourquoi de nouvelles molécules antimicrobiennes sont importantes
À mesure que les antibiotiques courants perdent de leur efficacité face à des bactéries de plus en plus résistantes, les médecins manquent d’options pour traiter des infections banales. Une alternative prometteuse est constituée par les peptides antimicrobiens — de courts fragments protéiques qui perçoivent les membranes bactériennes plutôt que de cibler une seule enzyme. Cet article décrit comment des chercheurs ont utilisé l’intelligence artificielle (IA) pour concevoir et tester automatiquement de nouveaux peptides antimicrobiens de façon plus rapide, moins coûteuse et plus ciblée que les expériences traditionnelles par essais‑erreurs.

Une nouvelle façon d’explorer l’immense espace des molécules
Concevoir des peptides antimicrobiens utiles revient à chercher quelques billets gagnants dans une montagne de chiffres aléatoires : il existe un nombre astronomique de séquences d’acides aminés possibles, mais seule une infime fraction sera sûre et efficace comme médicament. Le criblage en laboratoire classique est lent et coûteux, et même les modèles informatiques peinent souvent à concilier puissance et diversité, nécessaires pour découvrir de véritables nouveautés. Les auteurs répondent à cela en construisant une pipeline en trois étapes — génération, évaluation et validation expérimentale — qui permet à l’IA d’explorer d’immenses régions de l’espace des séquences tout en se concentrant sur des candidats réalistes et prometteurs.
Apprendre à un modèle de langage protéique à penser comme un concepteur de peptides
Au cœur de la première étape se trouve ProtGPT2, un grand « modèle de langage protéique » initialement entraîné pour écrire des séquences protéiques plausibles comme les modèles de texte écrivent des phrases. Plutôt que de réentraîner entièrement ce modèle massif — une approche coûteuse et sujette au surapprentissage sur de petits jeux de données antimicrobiens — l’équipe utilise une stratégie appelée soft prompt tuning. Ils ajoutent une petite invite d’entrée entraînable devant chaque séquence et ne mettent à jour que cette invite en gardant fixes les poids internes du modèle. Cette orientation douce a suffi à pousser le modèle vers la génération de peptides de type antimicrobien sans sacrifier sa créativité générale. Les analyses des séquences générées montrent qu’elles correspondent aux peptides antimicrobiens réels sur des propriétés clés comme la charge, l’hydrophobicité et les motifs structurels, tout en restant plus diverses que les séquences produites par un réentraînement complet.
Laisser plusieurs « experts » IA voter pour chaque candidat
Dans la deuxième étape, les chercheurs font face au défi inverse : parmi 30 000 séquences générées, lesquelles méritent le coût de la synthèse chimique et des tests en laboratoire ? Ils construisent un modèle d’évaluation appelé MCL‑AMP qui combine trois « experts » en réseaux neuronaux différents — l’un se focalisant sur les motifs locaux, l’autre suivant les relations à longue portée le long de la séquence, et un troisième intégrant des caractéristiques globales. Un réseau de vote séparé apprend à quel point il faut faire confiance à chaque expert pour chaque peptide, et une fonction de perte spéciale décourage le système d’être trop confiant lorsqu’il se trompe. En utilisant des caractéristiques de séquence riches extraites par un autre modèle protéique avancé (ESM‑2), cet ensemble obtient une précision supérieure aux outils existants pour distinguer les séquences antimicrobiennes des non‑antimicrobiennes, et produit un score de confiance interprétable pour chaque candidat.
Des prédictions informatiques aux bactéries réelles en laboratoire
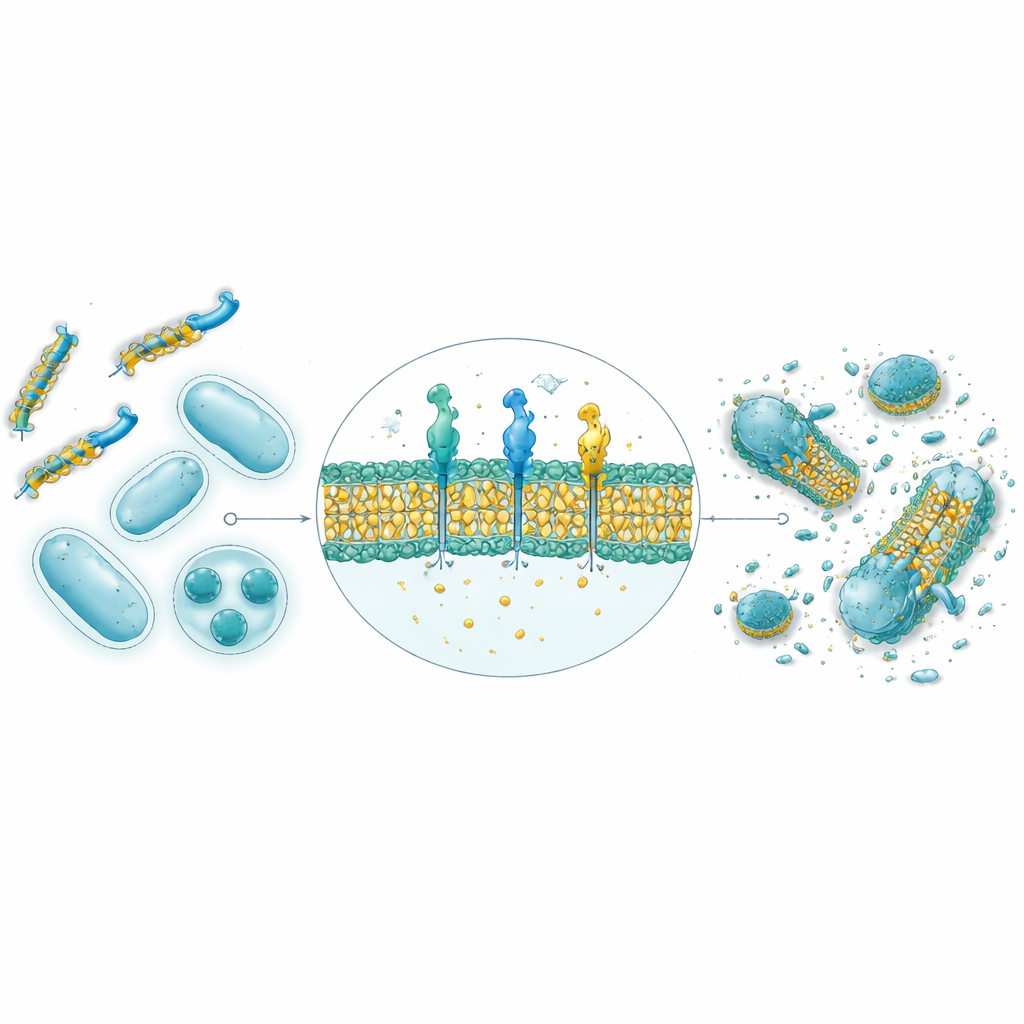
Parmi les 30 000 séquences générées par l’IA, les neuf peptides ayant obtenu les meilleurs scores ont été synthétisés et testés contre quatre souches bactériennes, incluant des espèces Gram‑positives et Gram‑négatives. Les prédictions structurelles réalisées avec AlphaFold suggèrent que huit des neuf adoptent des formes hélicoïdales amphipathiques typiques des peptides antimicrobiens naturels, avec des faces distinctes hydrophiles et hydrophobes favorisant l’attaque membranaire. Dans des tests en boîte de Pétri, quatre des neuf ont montré une forte activité antibactérienne, et deux en particulier — nommés GW20 et KI16 — se rapprochaient des performances d’antibiotiques établis pour arrêter la croissance bactérienne. La microscopie a révélé que ces peptides endommageaient visiblement la surface des cellules bactériennes, cohérent avec un mécanisme de perturbation membranaire. Fait important, les deux ont montré des dommages minimes aux globules rouges à des concentrations thérapeutiques pertinentes et ont démontré une grande capacité à prévenir et à dégrader des biofilms bactériens collants, surpassant souvent un antibiotique standard.
Ce que cela signifie pour les médicaments de demain
Pour un public non spécialiste, le message clé est que les auteurs ont construit une boucle fonctionnelle « concevoir‑tester » dans laquelle l’IA propose de nombreux nouveaux peptides tueurs de micro‑organismes, les trie à l’aide d’un comité de modèles, puis confirme les succès en laboratoire. Même si toutes les séquences mieux classées n’ont pas fonctionné, le taux de réussite — quatre peptides actifs sur neuf testés — est bien supérieur au criblage aveugle traditionnel. Les deux molécules les plus prometteuses présentent déjà un mélange utile de puissance, de sécurité et d’activité contre les biofilms, ce qui laisse entrevoir de futures thérapies pour des infections tenaces. Autre point important, la même pipeline modulaire pourrait être réajustée pour concevoir d’autres peptides médicaux, tels que des agents ciblant le cancer ou des molécules antivirales, offrant une feuille de route flexible pour la découverte de médicaments accélérée par l’IA face à l’augmentation de la résistance antimicrobienne.
Citation: Liu, J., Chen, Y., Tang, J. et al. Deep learning-driven integrated pipeline for de novo design and synthesis of antimicrobial peptides. npj Drug Discov. 3, 15 (2026). https://doi.org/10.1038/s44386-026-00045-6
Mots-clés: peptides antimicrobiens, intelligence artificielle, découverte de médicaments, résistance aux antibiotiques, biofilms