Clear Sky Science · ru
Интегрированный конвейер на основе глубокого обучения для de novo проектирования и синтеза антибактериальных пептидов
Почему важны новые антимикробные молекулы
По мере того как обычные антибиотики теряют эффективность против всё более устойчивых бактерий, у врачей остаётся всё меньше способов лечить повседневные инфекции. Одной из перспективных альтернатив являются антимикробные пептиды — короткие фрагменты белков, которые повреждают мембраны бактерий вместо того, чтобы нацеливаться на один фермент. В этой статье описывается, как исследователи использовали искусственный интеллект (ИИ) для автоматического проектирования и тестирования новых антимикробных пептидов быстрее, дешевле и более целенаправленно, чем в традиционных методах методом проб и ошибок.

Новый способ поиска в огромном пространстве молекул
Проектирование полезных антимикробных пептидов похоже на поиск нескольких выигрышных лотерейных билетов в груде случайных чисел: возможных последовательностей аминокислот астрономически много, но лишь малая доля из них будет безопасными и эффективными лекарствами. Традиционные лабораторные скрининги медленны и дороги, а даже компьютерные модели часто испытывают трудности с балансом между активностью и разнообразием, необходимым для обнаружения по‑настоящему новых молекул. Авторы решают эту задачу, построив трехэтапный конвейер — генерация, оценка и экспериментальная валидация — который позволяет ИИ исследовать огромные области пространства последовательностей, при этом отбирая реалистичные и перспективные кандидаты.
Обучение языковой модели белков думать как дизайнер пептидов
В основе первого шага лежит ProtGPT2 — крупная «языковая модель белков», изначально обученная генерировать правдоподобные белковые последовательности так же, как текстовые модели формируют предложения. Вместо полного дообучения этой массивной модели — подхода, дорогостоящего и склонного к переобучению на небольших наборах данных по антибактериальным пептидам — команда использует стратегию, называемую мягкой настройкой промта (soft prompt tuning). Они добавляют небольшой обучаемый входной промт перед каждой последовательностью и обновляют только этот промт, оставляя внутренние веса модели фиксированными. Такое мягкое направление оказалось достаточным, чтобы сдвинуть модель в сторону генерации пептидов, похожих на антимикробные, без потери широкой креативности. Анализы сгенерированных последовательностей показали, что они соответствуют реальным антимикробным пептидам по ключевым свойствам — заряду, гидрофобности и структурным паттернам — при этом оставаясь более разнообразными, чем последовательности, полученные при полном дообучении.
Когда несколько ИИ «экспертов» голосуют за каждый кандидат
На втором этапе перед исследователями встает обратная проблема: из 30 000 сгенерированных последовательностей какие заслуживают затрат на химический синтез и лабораторное тестирование? Они создают модель оценки под названием MCL‑AMP, которая объединяет три разных нейросетевых «эксперта» — один ориентируется на локальные паттерны, другой отслеживает дальнодействующие взаимосвязи вдоль последовательности, а третий интегрирует общие признаки. Отдельная голосующая сеть обучается тому, насколько доверять каждому эксперту для каждого пептида, а специальная функция потерь препятствует излишней уверенности системы, когда она ошибается. Используя богатые признаки последовательностей, извлечённые другой продвинутой моделью белков (ESM‑2), этот ансамбль достиг большей точности, чем существующие инструменты, в различении антимикробных и неантимикробных последовательностей и выдал интерпретируемую оценку уверенности для каждого кандидата.
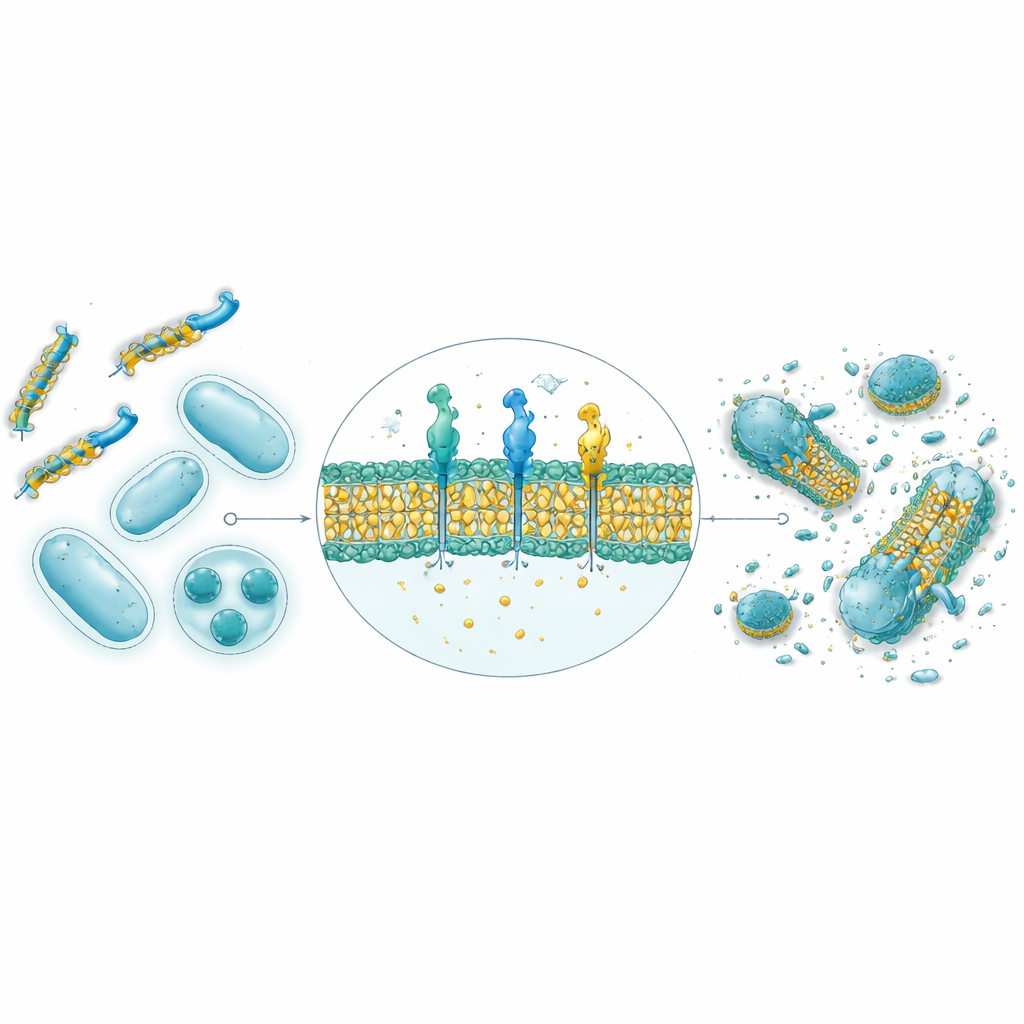
От компьютерных предсказаний к реальным бактериям в лаборатории
Из 30 000 сгенерированных ИИ последовательностей девять с наивысшими оценками были синтезированы и протестированы против четырёх штаммов бактерий, включая как грамположительные, так и грамотрицательные виды. Структурные предсказания с помощью AlphaFold показали, что восемь из девяти принимают амфипатические спиральные формы, типичные для природных антимикробных пептидов, с разделением на гидрофильную и гидрофобную стороны, что благоприятствует атаке мембраны. В опытах в чашках Питри четыре из девяти проявили сильную антибактериальную активность, и два из них — GW20 и KI16 — особенно близки по эффективности к установленным антибиотикам в подавлении роста бактерий. Микроскопия показала видимые повреждения поверхности бактериальных клеток, согласующиеся с механизмом нарушения мембраны. Важно, что оба пептида вызывали минимальный вред эритроцитам при терапевтически релевантных концентрациях и демонстрировали высокую способность предотвращать образование и разрушать липкие бактериальные биопленки, часто превосходя стандартный антибиотик.
Что это значит для будущих лекарств
Для неспециалистов ключевая мысль такова: авторы построили рабочую петлю «проектирование–тестирование», в которой ИИ предлагает множество новых убивающих микробы пептидов, отбирает их комитетом моделей и затем подтверждает находки в лаборатории. Хотя не каждая из лучших по ранжированию последовательностей оказалась успешной, доля «попаданий» — четыре активных пептида из девяти протестированных — значительно выше, чем при традиционном слепом скрининге. Два наиболее перспективных молекулы уже демонстрируют полезное сочетание мощности, безопасности и активности против биопленок, намекая на возможные терапии для упорных инфекций. Не менее важно то, что тот же модульный конвейер можно перенастроить для проектирования других лечебных пептидов, например, таргетных средств против рака или противовирусных молекул, предоставляя гибкую схему для ускоренного ИИ открытия лекарств в условиях роста устойчивости к антибиотикам.
Цитирование: Liu, J., Chen, Y., Tang, J. et al. Deep learning-driven integrated pipeline for de novo design and synthesis of antimicrobial peptides. npj Drug Discov. 3, 15 (2026). https://doi.org/10.1038/s44386-026-00045-6
Ключевые слова: антибактериальные пептиды, искусственный интеллект, поиск лекарств, устойчивость к антибиотикам, биопленки