Clear Sky Science · sv
Djupinlärningsdriven integrerad pipeline för de novo-design och syntes av antimikrobiella peptider
Varför nya bakteriedödande molekyler är viktiga
När vanliga antibiotika förlorar effekt mot allt tuffare bakterier får läkare färre verktyg för att behandla vardagliga infektioner. Ett lovande alternativ är antimikrobiella peptider — korta proteinkedjor som borrar hål i bakteriers membran i stället för att rikta in sig på ett enda enzym. Denna artikel beskriver hur forskare använde artificiell intelligens (AI) för att automatiskt designa och testa nya antimikrobiella peptider snabbare, billigare och mer riktat än traditionella prövningar genom försök och fel.

Ett nytt sätt att söka i det enorma molekylrummet
Att designa användbara antimikrobiella peptider är som att leta efter några få vinstlotter i en hög av slumpmässiga siffror: det finns astronomiskt många möjliga aminosyrasekvenser, men bara en liten bråkdel kommer att vara säkra och effektiva läkemedel. Konventionell laboratoriescreening är långsam och kostsam, och även datorbaserade modeller har ofta svårt att balansera potens med den mångfald som behövs för att hitta verkligt nya molekyler. Författarna tar itu med detta genom att bygga en trestegs‑pipeline — generering, utvärdering och experimentell validering — som låter AI utforska stora delar av sekvensrymden samtidigt som den zoomar in på kandidater som ser realistiska och lovande ut.
Att lära en protein‑språkmodell att tänka som en peptiddesigner
I kärnan av det första steget ligger ProtGPT2, en stor ”protein‑språkmodell” som ursprungligen tränades för att skriva trovärdiga proteinkedjor på samma sätt som textmodeller skriver meningar. Istället för att helt omträna denna massiva modell — en metod som är kostsam och benägen att överanpassa till små antimikrobiella datamängder — använder teamet en strategi som kallas mjuk prompt‑tuning. De fäster en liten, träningsbar input‑prompt framför varje sekvens och uppdaterar endast denna prompt medan modellens interna vikter förblir fasta. Denna försiktiga styrning visade sig räcka för att få modellen att producera peptider i riktning mot antimikrobiella egenskaper utan att offra dess breda kreativitet. Analyser av de genererade sekvenserna visade att de matchade verkliga antimikrobiella peptider i nyckelegenskaper såsom laddning, hydrofobicitet och strukturmönster, samtidigt som de förblev mer mångsidiga än sekvenser framställda genom fullständig omträning.
Låta flera AI ”experter” rösta om varje kandidat
I det andra steget ställs forskarna inför motsatt utmaning: av 30 000 genererade sekvenser, vilka förtjänar kostnaden för kemisk syntes och laboratorietester? De bygger en utvärderingsmodell kallad MCL‑AMP som kombinerar tre olika neurala nätverks‑”experter” — en som fokuserar på lokala mönster, en som följer långdistansrelationer längs sekvensen och en som integrerar övergripande egenskaper. Ett separat röstningsnätverk lär sig hur mycket man ska lita på varje expert för varje peptid, och en särskild förlustfunktion avskräcker systemet från att vara för självsäkert när det har fel. Med rika sekvensfunktioner extraherade av en annan avancerad proteinmodell (ESM‑2) uppnådde detta ensemble högre noggrannhet än befintliga verktyg vid skiljandet av antimikrobiella från icke‑antimikrobiella sekvenser, och det producerade en tolkbar konfidenspoäng för varje kandidat.
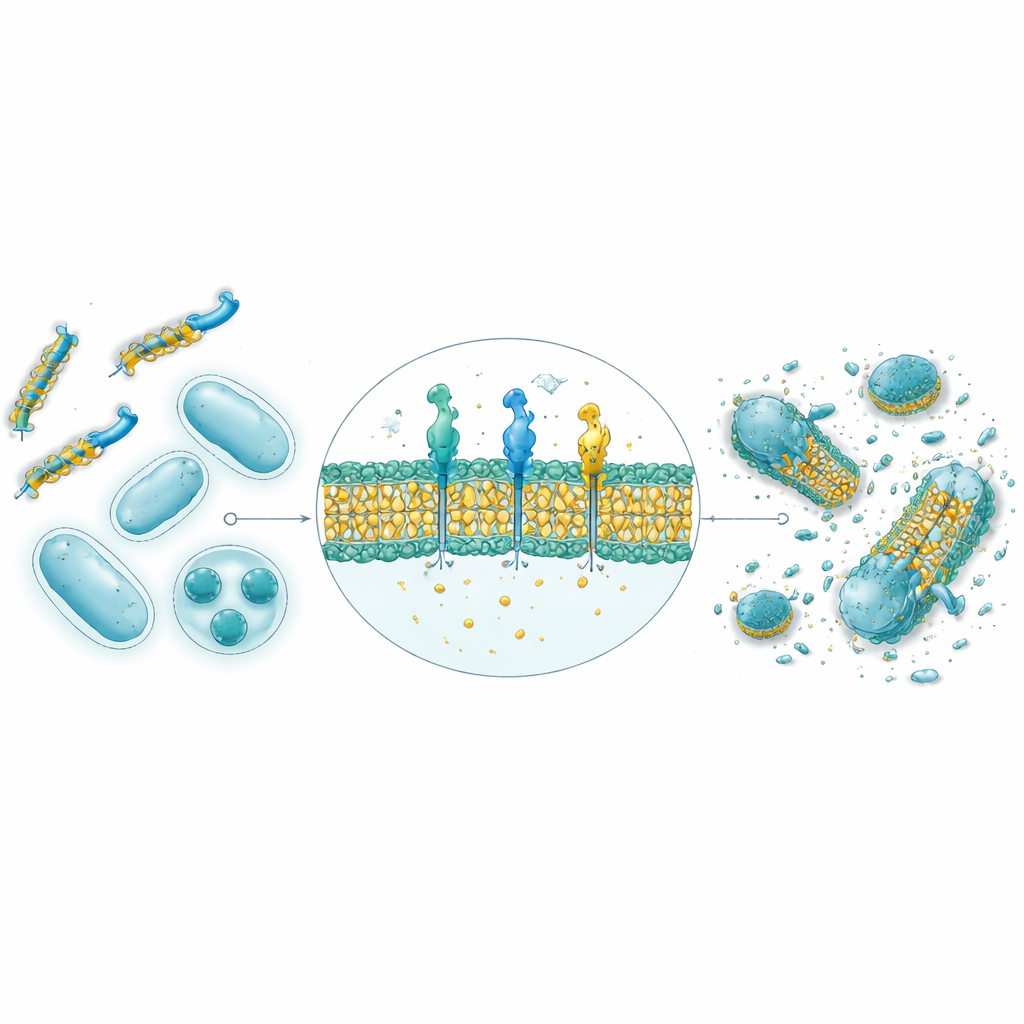
Från datorprognoser till verkliga bakterier i laboratoriet
Av de 30 000 AI‑genererade sekvenserna syntetiserades och testades de nio högst rankade peptiderna mot fyra bakteriella stammar, inklusive både Gram‑positiva och Gram‑negativa arter. Strukturella förutsägelser med AlphaFold antydde att åtta av de nio antar de amphipatiska helixformer som är typiska för naturliga antimikrobiella peptider, med separata vattenälskande och fettälskande sidor som gynnar membranangrepp. I petriskålstester visade fyra av de nio stark antibakteriell aktivitet, och två i synnerhet — kallade GW20 och KI16 — närmade sig prestandan hos etablerade antibiotika vid att stoppa bakterietillväxt. Mikroskopi visade att dessa peptider synligt skadade bakteriers cellytor, i linje med en mekanism för membran‑störning. Viktigt är att båda visade minimal skada på röda blodkroppar vid terapeutiskt relevanta koncentrationer och uppvisade stark förmåga att förhindra och bryta ned klibbiga bakteriella biofilmer, ofta med bättre resultat än ett standardantibiotikum.
Vad detta betyder för framtida läkemedel
För icke‑specialister är huvudbudskapet att författarna har byggt en fungerande ”design–test”-loop där AI föreslår många nya bakteriedödande peptider, sorterar dem med en kommitté av modeller och sedan bekräftar träffar i laboratoriet. Även om inte varje högt rankad sekvens fungerade är träfffrekvensen — fyra aktiva peptider av nio testade — långt högre än traditionell blindscreening. De två mest lovande molekylerna visar redan en användbar kombination av potens, säkerhet och förmåga att bekämpa biofilmer, vilket antyder framtida behandlingar för envisa infektioner. Lika viktigt är att samma modulära pipeline kan ställas om för att designa andra medicinska peptider, såsom cancerinriktade medel eller antivirala molekyler, och erbjuder en flexibel mall för AI‑accelererad läkemedelsupptäckt i ljuset av ökande antimikrobiell resistens.
Citering: Liu, J., Chen, Y., Tang, J. et al. Deep learning-driven integrated pipeline for de novo design and synthesis of antimicrobial peptides. npj Drug Discov. 3, 15 (2026). https://doi.org/10.1038/s44386-026-00045-6
Nyckelord: antimikrobiella peptider, artificiell intelligens, läkemedelsupptäckt, antibiotikaresistens, biofilmer