Clear Sky Science · nl
Door deep learning aangedreven geïntegreerde pijplijn voor de de novo-ontwerp en synthese van antimicrobiële peptiden
Waarom nieuwe kiem‑bestrijdende moleculen ertoe doen
Nu gangbare antibiotica hun werking verliezen tegen steeds taaiere bacteriën, raken artsen zonder opties om alledaagse infecties te behandelen. Een veelbelovende alternatieve benadering zijn antimicrobiële peptiden — korte eiwitfragmenten die gaten in bacteriële membranen slaan in plaats van één enkel enzym te blokkeren. Dit artikel beschrijft hoe onderzoekers kunstmatige intelligentie (AI) gebruikten om automatisch nieuwe antimicrobiële peptiden te ontwerpen en te testen, op een snellere, goedkopere en gerichtere manier dan traditionele proef‑en‑foutexperimenten.

Een nieuwe manier om de enorme molecuulruimte te doorzoeken
Het ontwerpen van bruikbare antimicrobiële peptiden is als het zoeken naar een paar winnende lotnummers in een berg willekeurige cijfers: er zijn astronomisch veel mogelijke aminozuursequenties, maar slechts een piepklein aandeel zal veilige en effectieve geneesmiddelen opleveren. Traditionele laboratoriumscreening is traag en duur, en zelfs computermodellen worstelen vaak met het afwegen van potentie tegen de diversiteit die nodig is om echt nieuwe moleculen te ontdekken. De auteurs pakken dit aan met een driedelige pijplijn — generatie, evaluatie en experimentele validatie — die AI in staat stelt enorme delen van de sequentieruimte te verkennen terwijl het toch inzoomt op kandidaten die realistisch en veelbelovend lijken.
Een eiwit‑taalmodel leren denken als een peptidenontwerper
Centraal in de eerste stap staat ProtGPT2, een groot “eiwit‑taalmodel” dat oorspronkelijk getraind is om plausibele eiwitsequenties te schrijven zoals taalmodellen zinnen genereren. In plaats van dit omvangrijke model volledig opnieuw te trainen — een aanpak die kostbaar is en de neiging heeft tot overfitting op kleine antimicrobiële datasets — gebruikt het team een strategie genaamd soft prompt tuning. Ze voegen een kleine, trainbare invoerprompt vóór elke sequentie toe en werken alleen aan die prompt terwijl de interne gewichten van het model vast blijven. Deze subtiele bijsturing bleek voldoende om het model te verschuiven richting het genereren van antimicrobieel‑achtige peptiden zonder de brede creativiteit te verliezen. Analyse van de gegenereerde sequenties liet zien dat ze overeenkwamen met echte antimicrobiële peptiden op cruciale eigenschappen zoals lading, hydrofobiciteit en structurele patronen, terwijl ze diverser bleven dan sequenties geproduceerd door volledige retraining.
Meerdere AI “experts” laten stemmen over elke kandidaat
In de tweede stap staan de onderzoekers voor de omgekeerde uitdaging: uit 30.000 gegenereerde sequenties, welke verdienen de kosten van chemische synthese en laboratoriumtesten? Ze bouwen een evaluatiemodel genaamd MCL‑AMP dat drie verschillende neurale netwerk‑“experts” combineert — één die zich richt op lokale patronen, één die langeafstandsrelaties langs de sequentie volgt, en één die algemene kenmerken integreert. Een apart stemnetwerk leert hoeveel vertrouwen het aan elke expert moet geven voor elk peptide, en een speciale verliesfunctie ontmoedigt het systeem om overmatig zelfverzekerd te zijn wanneer het fout zit. Met rijke sequentiekenmerken geëxtraheerd door een ander geavanceerd eiwitmodel (ESM‑2) behaalde dit ensemble een hogere nauwkeurigheid dan bestaande hulpmiddelen bij het onderscheiden van antimicrobiële en niet‑antimicrobiële sequenties, en het leverde een interpreteerbare betrouwbaarheidscore voor elke kandidaat op.
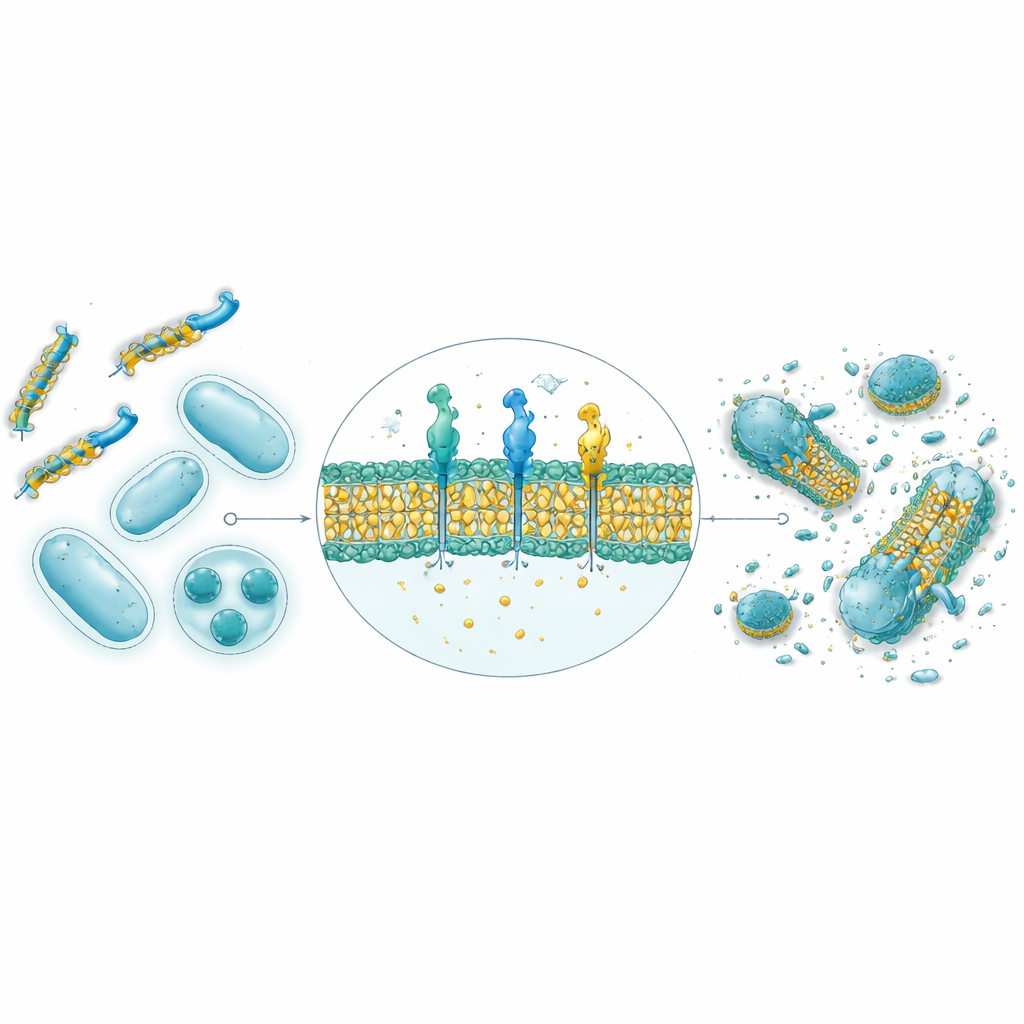
Van computer‑voorspellingen naar echte bacteriën in het laboratorium
Van de 30.000 door AI gegenereerde sequenties werden de negen hoogst scorende peptiden gesynthetiseerd en getest tegen vier bacteriestammen, waaronder zowel Gram‑positieve als Gram‑negatieve soorten. Structurele voorspellingen met AlphaFold suggereerden dat acht van de negen de amfipatische helixvormen aannemen die kenmerkend zijn voor natuurlijke antimicrobiële peptiden, met afzonderlijke waterminnende en vetminnende vlakken die membrane‑aanval bevorderen. In petrischaaltesten toonden vier van de negen sterke antibacteriële activiteit, en twee in het bijzonder — genoemd GW20 en KI16 — benaderden de prestaties van gevestigde antibiotica in het stoppen van bacteriële groei. Microscopen toonden aan dat deze peptiden zichtbaar schade aan de bacteriële celoppervlakken veroorzaakten, wat overeenkomt met een mechanisme van membraanschade. Belangrijk is dat beide minimale schade aan rode bloedcellen veroorzaakten bij therapeutisch relevante concentraties en sterke capaciteiten toonden om plakkerige bacteriële biofilms te voorkomen en af te breken, vaak beter presterend dan een standaardantibioticum.
Wat dit betekent voor toekomstige medicijnen
Voor niet‑specialisten is de kernboodschap dat de auteurs een werkende “ontwerp‑test” cyclus hebben gebouwd waarin AI veel nieuwe kiem‑dodende peptiden voorstelt, ze triageert met een commissie van modellen en vervolgens hits in het laboratorium bevestigt. Hoewel niet elke hoog gerangschikte sequentie werkte, is het hittarief — vier actieve peptiden van de negen geteste — veel hoger dan bij traditionele blinde screening. De twee meest veelbelovende moleculen vertonen al een nuttige mix van potentie, veiligheid en biofilm‑bestrijdende eigenschappen, wat wijst op toekomstige therapieën voor hardnekkige infecties. Even belangrijk is dat dezelfde modulaire pijplijn opnieuw kan worden afgestemd om andere medische peptiden te ontwerpen, zoals kanker‑gerichte agentia of antivirale moleculen, en zo een flexibel blauwdruk biedt voor AI‑versnelde geneesmiddelenontdekking in het licht van toenemende antimicrobiële resistentie.
Bronvermelding: Liu, J., Chen, Y., Tang, J. et al. Deep learning-driven integrated pipeline for de novo design and synthesis of antimicrobial peptides. npj Drug Discov. 3, 15 (2026). https://doi.org/10.1038/s44386-026-00045-6
Trefwoorden: antimicrobiële peptiden, kunstmatige intelligentie, geneesmiddelenontdekking, antibioticaresistentie, biofilms