Clear Sky Science · de
Deep-Learning-gesteuerter integrierter Ablauf für das de-novo-Design und die Synthese antimikrobieller Peptide
Warum neue keimtötende Moleküle wichtig sind
Da gängige Antibiotika gegenüber zunehmend widerstandsfähigen Bakterien an Wirkung verlieren, gehen Ärzten die Optionen aus, um alltägliche Infektionen zu behandeln. Eine vielversprechende Alternative sind antimikrobielle Peptide – kurze Proteinfragmente, die Löcher in bakterielle Membranen schlagen, anstatt ein einzelnes Enzym anzugreifen. Dieser Artikel beschreibt, wie Forscher künstliche Intelligenz (KI) einsetzten, um neue antimikrobielle Peptide automatisch zu entwerfen und zu testen — schneller, günstiger und gezielter als traditionelle Versuch‑und‑Irrtum-Experimente.

Ein neuer Weg, den gewaltigen Molekülraum zu durchsuchen
Das Entwerfen nützlicher antimikrobieller Peptide gleicht der Suche nach wenigen Gewinnscheinen in einem Berg zufälliger Zahlen: Es gibt astronomisch viele mögliche Aminosäuresequenzen, aber nur ein winziger Bruchteil davon wird sichere und wirksame Wirkstoffe sein. Konventionelle Laborscreenings sind langsam und teuer, und selbst Computermodelle tun sich oft schwer, Potenz mit der nötigen Vielfalt zu verbinden, um wirklich neue Moleküle zu entdecken. Die Autoren begegnen diesem Problem mit einer dreistufigen Pipeline — Erzeugung, Bewertung und experimentelle Validierung — die es der KI erlaubt, riesige Bereiche des Sequenzraums zu erkunden und gleichzeitig auf Kandidaten zu fokussieren, die realistisch und vielversprechend erscheinen.
Ein Protein-Sprachmodell so trainieren, dass es wie ein Peptiddesigner denkt
Kern des ersten Schritts ist ProtGPT2, ein großes „Protein-Sprachmodell“, das ursprünglich darauf trainiert wurde, plausible Proteinsequenzen zu erzeugen, ähnlich wie Sprachmodelle Sätze schreiben. Anstatt dieses enorme Modell vollständig neu zu trainieren — ein Vorgehen, das kostenintensiv ist und bei kleinen antimikrobiellen Datensätzen zur Überanpassung neigt — nutzt das Team eine Strategie namens Soft-Prompt-Tuning. Sie fügen vor jede Sequenz einen kleinen, trainierbaren Eingabeprompt an und aktualisieren nur diesen Prompt, während die internen Gewichte des Modells unverändert bleiben. Diese subtile Steuerung reichte aus, um das Modell in Richtung antimikrobiell-ähnlicher Peptide zu lenken, ohne seine breite Kreativität zu opfern. Analysen der erzeugten Sequenzen zeigten, dass sie reale antimikrobielle Peptide in Schlüsseleigenschaften wie Ladung, Hydrophobizität und Strukturmuster nachahmten, dabei aber diverser blieben als Sequenzen, die durch vollständiges Retraining entstanden.
Mehrere KI-„Experten“ über jeden Kandidaten abstimmen lassen
Im zweiten Schritt stehen die Forscher vor der umgekehrten Herausforderung: Aus 30.000 erzeugten Sequenzen — welche rechtfertigen die Kosten für chemische Synthese und Labortests? Sie bauen ein Bewertungsmodell namens MCL‑AMP, das drei verschiedene neuronale Netzwerk‑„Experten“ kombiniert — einen, der sich auf lokale Muster konzentriert, einen, der langreichweitige Beziehungen entlang der Sequenz erfasst, und einen, der übergeordnete Merkmale integriert. Ein separates Abstimmungsnetz lernt, wie viel Vertrauen jedem Experten für jedes Peptid zu schenken ist, und eine spezielle Verlustfunktion verhindert, dass das System bei Fehlentscheidungen übermäßig selbstsicher wird. Mit reichen Sequenzmerkmalen, extrahiert von einem weiteren fortgeschrittenen Proteinmodell (ESM‑2), erreichte dieses Ensemble eine höhere Genauigkeit als bestehende Werkzeuge bei der Unterscheidung von antimikrobiellen und nicht-antimikrobiellen Sequenzen und lieferte für jeden Kandidaten eine interpretierbare Vertrauensbewertung.
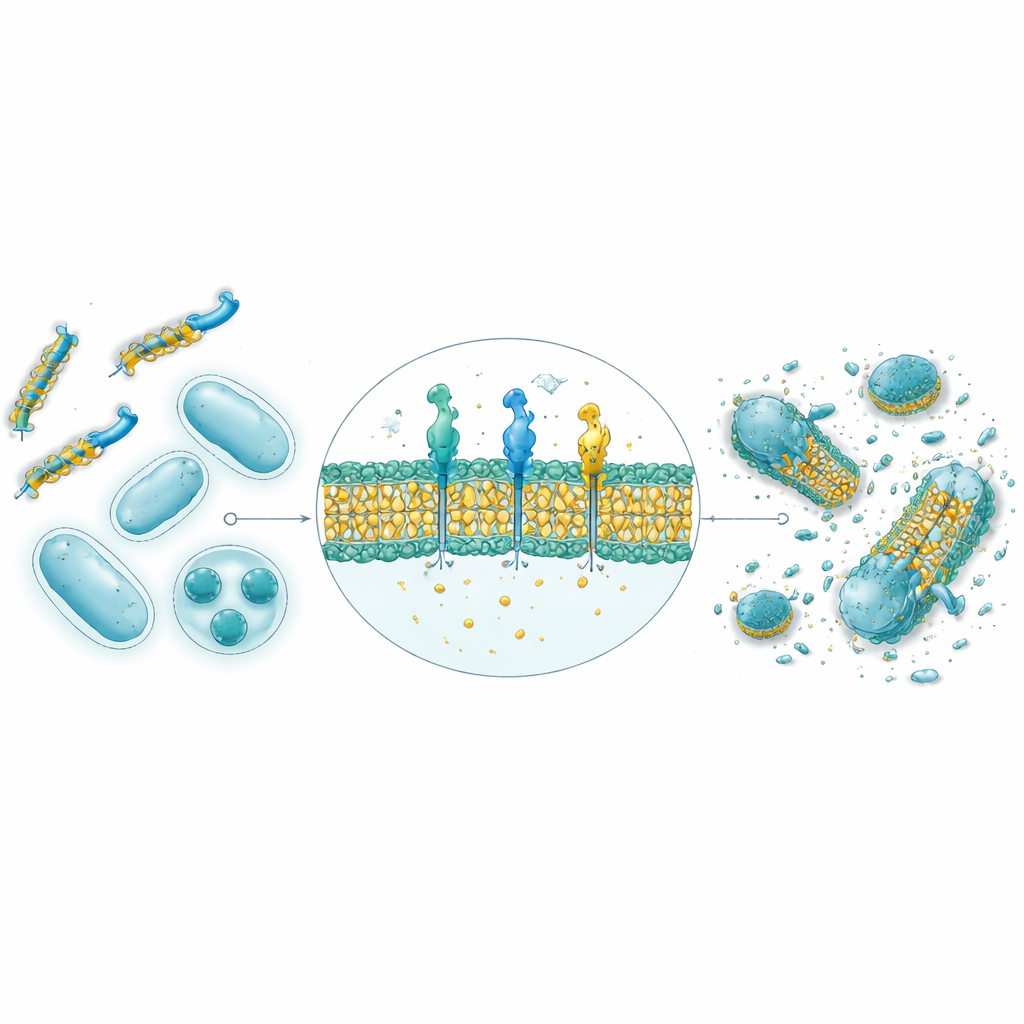
Von Computer‑Vorhersagen zu echten Bakterien im Labor
Aus den 30.000 KI-erzeugten Sequenzen wurden die neun höchstbewerteten Peptide synthetisiert und gegen vier Bakterienstämme getestet, darunter sowohl grampositive als auch gramnegative Arten. Strukturvorhersagen mit AlphaFold deuteten darauf hin, dass acht der neun die amphipathischen Helixformen annehmen, die für natürliche antimikrobielle Peptide typisch sind, mit getrennten wasserliebenden und fettliebenden Seiten, die einen Membranangriff begünstigen. In Petrischalentests zeigten vier der neun starke antibakterielle Aktivität, und zwei davon — bezeichnet als GW20 und KI16 — kamen der Leistung etablierter Antibiotika bei der Hemmung des Bakterienwachstums nahe. Mikroskopische Untersuchungen zeigten, dass diese Peptide die bakterielle Zelloberfläche sichtbar beschädigten, konsistent mit einem Mechanismus der Membrandestabilisierung. Wichtig ist, dass beide bei therapeutisch relevanten Konzentrationen nur minimale Schäden an roten Blutkörperchen verursachten und eine starke Fähigkeit zeigten, klebrige bakterielle Biofilme zu verhindern und abzubauen — oft besser als ein Standardantibiotikum.
Was das für zukünftige Medikamente bedeutet
Für Laien ist die Kernbotschaft: Die Autoren haben eine funktionierende „Design–Test“-Schleife aufgebaut, in der die KI viele neue keimtötende Peptide vorschlägt, sie mit einem Komitee von Modellen vorsortiert und Treffer dann im Labor bestätigt. Auch wenn nicht jede top‑rangige Sequenz wirkte, ist die Trefferquote — vier aktive Peptide von neun getesteten — deutlich höher als bei traditionellen Blindtests. Die zwei vielversprechendsten Moleküle zeigen bereits eine nützliche Mischung aus Wirksamkeit, Sicherheit und Biofilm‑Bekämpfungsfähigkeit, was auf künftige Therapien gegen hartnäckige Infektionen hindeutet. Ebenso wichtig ist, dass dieselbe modulare Pipeline neu justiert werden kann, um andere medizinische Peptide zu entwerfen, etwa krebszielende Wirkstoffe oder antivirale Moleküle, und so eine flexible Blaupause für KI-beschleunigte Wirkstoffforschung angesichts zunehmender antimikrobieller Resistenzen bietet.
Zitation: Liu, J., Chen, Y., Tang, J. et al. Deep learning-driven integrated pipeline for de novo design and synthesis of antimicrobial peptides. npj Drug Discov. 3, 15 (2026). https://doi.org/10.1038/s44386-026-00045-6
Schlüsselwörter: antimikrobielle Peptide, künstliche Intelligenz, Wirkstoffforschung, Antibiotikaresistenz, Biofilme