Clear Sky Science · es
Canalización integrada impulsada por aprendizaje profundo para el diseño de novo y la síntesis de péptidos antimicrobianos
Por qué importan nuevas moléculas contra gérmenes
A medida que los antibióticos comunes pierden eficacia frente a bacterias cada vez más resistentes, los médicos se quedan sin opciones para tratar infecciones rutinarias. Una alternativa prometedora son los péptidos antimicrobianos: fragmentos cortos de proteínas que perforan las membranas bacterianas en lugar de dirigirse a una sola enzima. Este artículo describe cómo los investigadores emplearon inteligencia artificial (IA) para diseñar y evaluar automáticamente nuevos péptidos antimicrobianos de forma más rápida, económica y dirigida que los experimentos tradicionales de prueba y error.

Una nueva forma de explorar el vasto espacio de moléculas
Diseñar péptidos antimicrobianos útiles es como buscar unos pocos billetes de lotería ganadores en una montaña de números aleatorios: hay secuencias de aminoácidos astronómicamente numerosas, pero solo una fracción minúscula será segura y eficaz como fármaco. El cribado de laboratorio convencional es lento y caro, e incluso los modelos informáticos suelen tener dificultades para equilibrar la potencia con la diversidad necesaria para descubrir moléculas genuinamente nuevas. Los autores abordan esto construyendo una canalización de tres pasos —generación, evaluación y validación experimental— que permite a la IA explorar enormes regiones del espacio de secuencias mientras converge hacia candidatas que parecen realistas y prometedoras.
Enseñar a un modelo de lenguaje proteico a pensar como un diseñador de péptidos
En el núcleo del primer paso está ProtGPT2, un gran «modelo de lenguaje proteico» originalmente entrenado para escribir secuencias de proteínas plausibles del mismo modo que los modelos de texto generan frases. En lugar de volver a entrenar completamente este modelo masivo —un enfoque costoso y propenso al sobreajuste con conjuntos reducidos de péptidos antimicrobianos—, el equipo usa una estrategia llamada ajuste de prompt suave (soft prompt tuning). Colocan un pequeño prompt de entrada entrenable delante de cada secuencia y actualizan solo ese prompt manteniendo fijos los pesos internos del modelo. Este direccionamiento suave fue suficiente para orientar al modelo hacia la producción de péptidos con características antimicrobianas sin sacrificar su creatividad general. Los análisis de las secuencias generadas mostraron que coincidían con los péptidos antimicrobianos reales en propiedades clave, como la carga, la hidrofobicidad y los patrones estructurales, al tiempo que mantenían mayor diversidad que las secuencias obtenidas mediante reentrenamiento completo.
Dejar que varios “expertos” de la IA voten por cada candidato
En el segundo paso, los investigadores afrontan el desafío opuesto: de 30.000 secuencias generadas, ¿cuáles justifican el coste de síntesis química y pruebas en laboratorio? Construyen un modelo de evaluación llamado MCL‑AMP que combina tres «expertos» de redes neuronales diferentes: uno que se centra en patrones locales, otro que rastrea relaciones de largo alcance a lo largo de la secuencia y uno que integra características globales. Una red de votación separada aprende cuánto confiar en cada experto para cada péptido, y una función de pérdida especial desincentiva que el sistema esté excesivamente confiado cuando se equivoca. Usando características de secuencia ricas extraídas por otro modelo proteico avanzado (ESM‑2), este conjunto alcanzó mayor precisión que las herramientas existentes para distinguir secuencias antimicrobianas de no antimicrobianas, y produjo una puntuación de confianza interpretable para cada candidato.
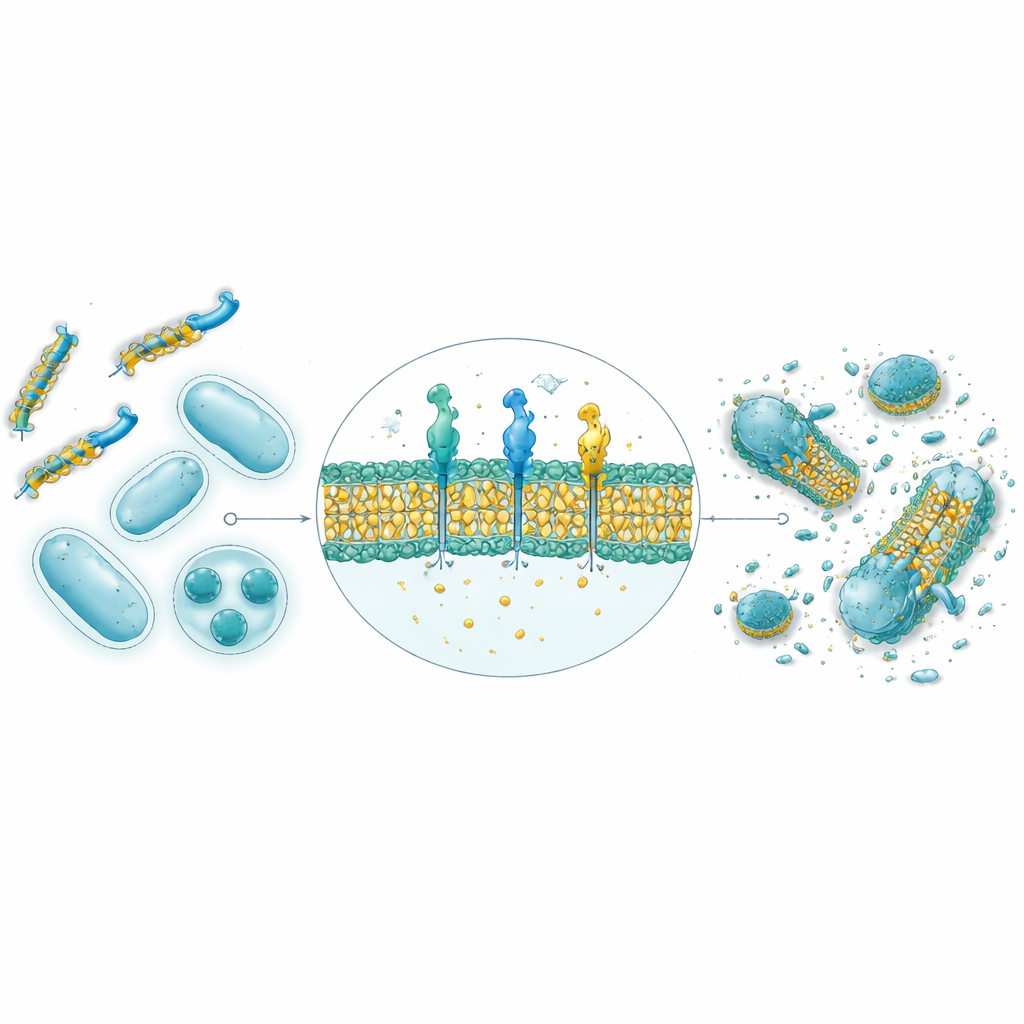
De las predicciones informáticas a bacterias reales en el laboratorio
De las 30.000 secuencias generadas por la IA, se sintetizaron y probaron las nueve péptidos mejor valorados contra cuatro cepas bacterianas, incluyendo especies Gram‑positivas y Gram‑negativas. Predicciones estructurales mediante AlphaFold sugirieron que ocho de los nueve adoptan las formas helicoidales anfipáticas típicas de los péptidos antimicrobianos naturales, con caras separadas hidrofílicas y lipofílicas que favorecen el ataque a la membrana. En pruebas en placa, cuatro de los nueve mostraron fuerte actividad antibacteriana, y dos en particular —denominados GW20 y KI16— se acercaron al rendimiento de antibióticos establecidos en la inhibición del crecimiento bacteriano. La microscopía reveló que estos péptidos dañaban visiblemente las superficies celulares bacterianas, coherente con un mecanismo de ruptura de membrana. Es importante destacar que ambos mostraron daño mínimo a los glóbulos rojos a concentraciones terapéuticas relevantes y demostraron gran capacidad para prevenir y descomponer biopelículas bacterianas adhesivas, a menudo superando a un antibiótico estándar.
Qué significa esto para los medicamentos del futuro
Para el público no especializado, el mensaje clave es que los autores han construido un ciclo operativo de «diseño–prueba» en el que la IA propone numerosos péptidos que matan gérmenes, los filtra mediante un comité de modelos y luego confirma los aciertos en laboratorio. Aunque no todas las secuencias mejor clasificadas funcionaron, la tasa de éxito —cuatro péptidos activos de nueve probados— es mucho mayor que la del cribado ciego tradicional. Las dos moléculas más prometedoras ya muestran una combinación útil de potencia, seguridad y capacidad anti‑biopelículas, lo que sugiere posibles terapias futuras para infecciones difíciles de tratar. Igualmente importante, la misma canalización modular podría reajustarse para diseñar otros péptidos médicos, como agentes dirigidos contra el cáncer o moléculas antivirales, ofreciendo un plan flexible para el descubrimiento de fármacos acelerado por IA frente al aumento de la resistencia antimicrobiana.
Cita: Liu, J., Chen, Y., Tang, J. et al. Deep learning-driven integrated pipeline for de novo design and synthesis of antimicrobial peptides. npj Drug Discov. 3, 15 (2026). https://doi.org/10.1038/s44386-026-00045-6
Palabras clave: péptidos antimicrobianos, inteligencia artificial, descubrimiento de fármacos, resistencia a los antibióticos, biopelículas